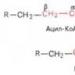
பால்மிடிக் அமிலத்தின் ஆக்சிஜனேற்றம். சம எண்ணிக்கையிலான கார்பன் அணுக்கள் கொண்ட நிறைவுற்ற கொழுப்பு அமிலங்களின் ஆக்சிஜனேற்றத்தின் ஆற்றல் சமநிலை. உங்கள் உணவில் கொழுப்பு அமிலங்களின் அளவை எவ்வாறு அதிகரிப்பது
100 ரூமுதல் ஆர்டருக்கான போனஸ்
வேலை வகையைத் தேர்ந்தெடு டிப்ளமோ வேலை பாடநெறிப் பயிற்சி அறிக்கை கட்டுரை அறிக்கை ஆய்வு சோதனை வேலை மோனோகிராஃப் சிக்கலைத் தீர்க்கும் வணிகத் திட்டம் கேள்விகளுக்கான பதில்கள் ஆக்கப்பூர்வமான வேலை கட்டுரை வரைதல் கட்டுரைகள் மொழிபெயர்ப்பு விளக்கக்காட்சிகள் தட்டச்சு செய்தல் மற்றவை உரையின் தனித்துவத்தை அதிகரிக்கும் முதுகலை ஆய்வகப் பணி.
விலையைக் கண்டறியவும்
கொழுப்பு அமிலங்கள் நிறைவுற்ற மற்றும் நிறைவுறாத உயர் கார்பாக்சிலிக் அமிலங்கள் ஆகும், இதில் ஹைட்ரோகார்பன் சங்கிலி 12 க்கும் மேற்பட்ட கார்பன் அணுக்களைக் கொண்டுள்ளது. உடலில், கொழுப்பு அமில ஆக்சிஜனேற்றம் ஒரு மிக முக்கியமான செயல்முறையாகும், மேலும் இது கார்பாக்சிலிக் அமில மூலக்கூறுகளின் α, β மற்றும் ω கார்பன் அணுக்களுக்கு அனுப்பப்படலாம். இந்த செயல்முறைகளில், β- ஆக்சிஜனேற்றம் அடிக்கடி நிகழ்கிறது. கொழுப்பு அமிலங்களின் ஆக்சிஜனேற்றம் கல்லீரல், சிறுநீரகங்கள், எலும்பு மற்றும் இதய தசைகள் மற்றும் கொழுப்பு திசுக்களில் ஏற்படுகிறது என்று நிறுவப்பட்டுள்ளது. மூளை திசுக்களில், கொழுப்பு அமில ஆக்சிஜனேற்ற விகிதம் மிகவும் குறைவாக உள்ளது; மூளை திசுக்களில் ஆற்றலின் முக்கிய ஆதாரம் குளுக்கோஸ் ஆகும்.
1904 ஆம் ஆண்டில், எஃப். நூப், நாய்களுக்கு பல்வேறு கொழுப்பு அமிலங்களை ஊட்டுவதற்கான சோதனைகளின் அடிப்படையில் கொழுப்பு அமிலங்களின் β-ஆக்சிஜனேற்றத்தின் கருதுகோளை முன்வைத்தார், இதில் டெர்மினல் மீதில் குழுவில் (ω-கார்பன் அணு) ஒரு ஹைட்ரஜன் அணு ஒரு தீவிரமான (C6H5–) மூலம் மாற்றப்பட்டது. )
விலங்குகள் மற்றும் தாவரங்களின் இயற்கையான கொழுப்புகளின் ஒரு பகுதியாக இருக்கும் கொழுப்பு அமிலங்கள், சம எண்ணிக்கையிலான கார்பன் அணுக்களைக் கொண்டுள்ளன. ஒரு ஜோடி கார்பன் அணுக்கள் வெளியேற்றப்படும் அத்தகைய அமிலம் இறுதியில் பியூட்ரிக் அமில நிலை வழியாக செல்கிறது. மற்றொரு β-ஆக்சிஜனேற்றத்திற்குப் பிறகு, பியூட்ரிக் அமிலம் அசிட்டோஅசிடிக் அமிலமாக மாறுகிறது. பிந்தையது பின்னர் அசிட்டிக் அமிலத்தின் இரண்டு மூலக்கூறுகளாக நீராற்பகுப்பு செய்யப்படுகிறது. F. Knoop ஆல் முன்மொழியப்பட்ட கொழுப்பு அமிலங்களின் β-ஆக்சிஜனேற்றக் கோட்பாடு, கொழுப்பு அமில ஆக்சிஜனேற்றத்தின் பொறிமுறையைப் பற்றிய நவீன கருத்துக்களுக்கு பெரும்பாலும் அடிப்படையாக இருந்தது.
கொழுப்பு அமிலங்களின் β-ஆக்சிஜனேற்றம். கொழுப்புகளின் நீராற்பகுப்பின் போது உருவாகும் கார்பாக்சிலிக் அமிலங்கள் மைட்டோகாண்ட்ரியாவில் β-ஆக்சிஜனேற்றத்திற்கு உட்படுகின்றன, அங்கு அவை தொடர்புடைய அசைல் கோஎன்சைம்கள் A. β-ஆக்சிஜனேற்றம் 4 தொடர்ச்சியான ORPகள் ஆகும்.
நான் எதிர்வினை. டிஹைட்ரஜனேற்றம்
//டீஹைட்ரோஜினேஸ் /
C15H31 – CH2 – CH2 – C + FAD C = C + FAD(2H)
SCoA H COSCoA
ஸ்டெரில் கோஎன்சைம் ஏ என்பது ஸ்டெரில் கோஎன்சைம் ஏ இன் டிரான்ஸ் ஐசோமர் ஆகும்
II எதிர்வினை நீரேற்றம்
/ ஹைட்ரேடேஸ் //
C = C + H2O C15H31 – CH – CH2 – C
எச் கோஸ்கோ ஓ ஓ எஸ் கோஏ
ஸ்டெரில் கோஎன்சைமின் டிரான்ஸ் ஐசோமர் A L-ஐசோமர் β-ஹைட்ராக்ஸிகார்பாக்சிலிக் அமிலம்
III எதிர்வினை டிஹைட்ரஜனேற்றம்
//டீஹைட்ரோஜினேஸ் //
C15H31 – CH – CH2 – C + NAD+ C15H31 – C – CH2 – C + NADH + H+
OH SCOA O SCOA
β-ஆக்சோ அமிலம்
IV எதிர்வினை. பிளவு
// தியோலேஸ் //
C15H31 – C – CH2 – C + HSCoA C15H31 – C CH3 – C
SCoA ScoA ScoA பற்றி
பால்மிடோகோஎன்சைம் ஏ அசிடைல்கோஎன்சைம் ஏ
கிரெப்ஸ் சுழற்சியில் புதிதாக என்ன இருக்கிறது
இறுதியின் β-ஆக்சிஜனேற்றம்
ஆக்சிஜனேற்றம்
CO2 மற்றும் H2O க்கு
β-ஆக்சிஜனேற்ற செயல்முறையின் நான்கு எதிர்வினைகள் ஒரு சுழற்சியைக் குறிக்கின்றன, இதன் போது கார்பன் சங்கிலி இரண்டு கார்பன் அணுக்களால் சுருக்கப்படுகிறது. பால்மிட்டோகோஎன்சைம் A மீண்டும் β-ஆக்சிஜனேற்றத்திற்கு உட்படுகிறது, இந்த சுழற்சியை மீண்டும் செய்கிறது. ஸ்டீரிக் அமிலத்தின் ஒரு மூலக்கூறின் β-ஆக்சிஜனேற்றத்தின் போது, கிரெப்ஸ் சுழற்சி உட்பட 40 ஏடிபி மூலக்கூறுகள் உருவாகின்றன, இதன் விளைவாக அசிடைல் கோஎன்சைம் ஏ - 146 ஏடிபி மூலக்கூறுகளை ஆக்சிஜனேற்றம் செய்கிறது. உடலின் ஆற்றலின் பார்வையில் கொழுப்பு அமில ஆக்சிஜனேற்றத்தின் செயல்முறைகளின் முக்கியத்துவத்தை இது குறிக்கிறது.
α- கொழுப்பு அமிலங்களின் ஆக்சிஜனேற்றம்.தாவரங்களில், என்சைம்களின் செயல்பாட்டின் கீழ், கொழுப்பு அமிலங்கள் α- கார்பன் அணுவில் ஆக்ஸிஜனேற்றப்படுகின்றன - α- ஆக்சிஜனேற்றம். இது இரண்டு எதிர்வினைகளைக் கொண்ட ஒரு சுழற்சி.
நான் எதிர்வினை ஹைட்ரஜன் பெராக்சைடுடன் ஒரு கொழுப்பு அமிலத்தின் ஆக்சிஜனேற்றம், அதனுடன் தொடர்புடைய பெராக்சிடேஸின் பங்கேற்புடன் தொடர்புடைய ஆல்டிஹைடு மற்றும் CO2 ஆகும்.
பெராக்ஸிடேஸ் //
R – CH2 – COOH + 2 H2O2 R – C + CO2
இந்த எதிர்வினையின் விளைவாக, கார்பன் சங்கிலி ஒரு கார்பன் அணுவால் சுருக்கப்படுகிறது.
II எதிர்வினை ஆல்டிஹைட் டீஹைட்ரோஜினேஸின் செயல்பாட்டின் கீழ் விளைந்த ஆல்டிஹைட்டின் நீரேற்றம் மற்றும் ஆக்சிஜனேற்றம் ஆகியவற்றைக் கொண்டுள்ளது.
//ஆல்டிஹைட்-//
R – C + H2O + NAD+ dehydrogenase R – C + NAD(H) + H+
α-ஆக்சிஜனேற்ற சுழற்சி தாவரங்களின் சிறப்பியல்பு.
ω- கொழுப்பு அமிலங்களின் ஆக்சிஜனேற்றம்.விலங்குகள் மற்றும் சில நுண்ணுயிரிகளின் கல்லீரலில் ω- ஆக்சிஜனேற்றத்தை வழங்கும் என்சைம் அமைப்பு உள்ளது, அதாவது. முனையம் CH3 குழுவில் ஆக்சிஜனேற்றம். முதலில், மோனோஆக்சிஜனேஸின் செயல்பாட்டின் கீழ், ஹைட்ராக்ஸைலேஷன் ஒரு ω-ஹைட்ராக்ஸி அமிலத்தை உருவாக்குகிறது:
ω மோனோஆக்சிஜனேஸ்
CH3 - R - COOH + "O" HOCH2 - R - COOH
HOCH2 – R – COOH + H2O + 2NAD+ டீஹைட்ரஜனேஸ் HOOC– R – COOH + 2 NAD (H) + 2H+
ω-டிகார்பாக்சிலிக் அமிலம்
இதன் விளைவாக உருவாகும் ω-டைகார்பாக்சிலிக் அமிலம் β-ஆக்சிஜனேற்ற வினையால் இரு முனைகளிலும் சுருக்கப்படுகிறது.
ஒரு கார்பாக்சிலிக் அமிலம் கிளைகளைக் கொண்டிருந்தால், அதன் உயிரியல் ஆக்சிஜனேற்றம் சங்கிலிக் கிளையை அடையும் போது நின்றுவிடும்.
கொழுப்பு அமில ஆக்சிஜனேற்றம் செயல்முறை பின்வரும் முக்கிய நிலைகளைக் கொண்டுள்ளது.
கொழுப்பு அமிலங்களை செயல்படுத்துதல். இலவச கொழுப்பு அமிலம், ஹைட்ரோகார்பன் சங்கிலியின் நீளத்தைப் பொருட்படுத்தாமல், வளர்சிதை மாற்றத்தில் செயலற்றது மற்றும் அது செயல்படுத்தப்படும் வரை ஆக்சிஜனேற்றம் உட்பட எந்த உயிர்வேதியியல் மாற்றங்களுக்கும் உட்படாது. ஏடிபி, கோஎன்சைம் ஏ (எச்எஸ்-கோஏ) மற்றும் எம்ஜி 2+ அயனிகளின் பங்கேற்புடன் மைட்டோகாண்ட்ரியல் மென்படலத்தின் வெளிப்புற மேற்பரப்பில் கொழுப்பு அமிலத்தை செயல்படுத்துகிறது. இந்த எதிர்வினை அசைல்-கோஏ சின்தேடேஸ் என்ற நொதியால் வினையூக்கப்படுகிறது:
எதிர்வினையின் விளைவாக, அசில்-கோஏ உருவாகிறது, இது கொழுப்பு அமிலத்தின் செயலில் உள்ள வடிவமாகும்.
டீஹைட்ரஜனேற்றத்தின் முதல் நிலை. மைட்டோகாண்ட்ரியாவில் உள்ள Acyl-CoA முதலில் நொதி டீஹைட்ரஜனேற்றத்திற்கு உட்படுகிறது, மேலும் அசைல்-CoA ஆனது α- மற்றும் β-நிலைகளில் 2 ஹைட்ரஜன் அணுக்களை இழந்து, நிறைவுறா அமிலத்தின் CoA எஸ்டர் ஆக மாறுகிறது.

நீரேற்றம் நிலை. நிறைவுறா அசைல்-கோஏ (எனாய்ல்-கோஏ), என்சைம் ஈனாய்ல்-கோஏ ஹைட்ராடேஸின் பங்கேற்புடன், நீர் மூலக்கூறை இணைக்கிறது. இதன் விளைவாக, β-ஹைட்ராக்ஸிசைல்-கோஏ (அல்லது 3-ஹைட்ராக்ஸிசைல்-கோஏ) உருவாகிறது:

டீஹைட்ரஜனேற்றத்தின் இரண்டாம் நிலை. இதன் விளைவாக β-ஹைட்ராக்ஸிசைல்-கோஏ (3-ஹைட்ராக்ஸிசைல்-கோஏ) பின்னர் டிஹைட்ரஜனேற்றம் செய்யப்படுகிறது. இந்த எதிர்வினை NAD+-சார்ந்த டீஹைட்ரஜனேஸ்களால் வினையூக்கப்படுகிறது:

தியோலேஸ் எதிர்வினை. இரண்டாவது CoA மூலக்கூறின் thiol குழுவால் 3-oxoacyl-CoA இன் பிளவு ஆகும். இதன் விளைவாக, இரண்டு கார்பன் அணுக்களால் சுருக்கப்பட்ட அசைல்-கோஏ மற்றும் அசிடைல்-கோஏ வடிவத்தில் இரண்டு கார்பன் துண்டு உருவாகிறது. இந்த எதிர்வினை அசிடைல்-கோஏ அசைல்ட்ரான்ஸ்ஃபெரேஸ் (β-கெட்டோதியோலேஸ்) மூலம் வினையூக்கப்படுகிறது:

இதன் விளைவாக அசிடைல்-கோஏ டிரைகார்பாக்சிலிக் அமில சுழற்சியில் ஆக்சிஜனேற்றத்திற்கு உட்படுகிறது, மேலும் இரண்டு கார்பன் அணுக்களால் சுருக்கப்பட்ட அசைல்-கோஏ, பியூட்டில்-கோஏ (4-கார்பன் கலவை) உருவாகும் வரை மீண்டும் மீண்டும் முழு β-ஆக்சிஜனேற்ற பாதை வழியாக செல்கிறது. அசிடைல்-கோஏவின் 2 மூலக்கூறுகள் வரை ஆக்சிஜனேற்றம் செய்யப்படுகிறது.
ஆற்றல் சமநிலை. β-ஆக்சிஜனேற்றத்தின் ஒவ்வொரு சுழற்சியும் FADH 2 இன் ஒரு மூலக்கூறையும் NADH இன் ஒரு மூலக்கூறையும் உருவாக்குகிறது. பிந்தையது, சுவாச சங்கிலி மற்றும் அதனுடன் தொடர்புடைய பாஸ்போரிலேஷன் ஆகியவற்றில் ஆக்ஸிஜனேற்றத்தின் செயல்பாட்டில், கொடுக்கிறது: FADH 2 - 2 ATP மூலக்கூறுகள் மற்றும் NADH - 3 ATP மூலக்கூறுகள், அதாவது. மொத்தத்தில், ஒரு சுழற்சியில் 5 ATP மூலக்கூறுகள் உருவாகின்றன. பால்மிடிக் அமிலத்தின் ஆக்சிஜனேற்றம் 5 x 7 = 35 ATP மூலக்கூறுகளை உருவாக்குகிறது. பால்மிடிக் அமிலத்தின் β-ஆக்சிஜனேற்றத்தின் செயல்பாட்டில், அசிடைல்-கோஏவின் 8 மூலக்கூறுகள் உருவாகின்றன, ஒவ்வொன்றும், ட்ரைகார்பாக்சிலிக் அமில சுழற்சியில் "எரியும்", ATP இன் 12 மூலக்கூறுகளை அளிக்கிறது, மேலும் 8 அசிடைல்-CoA மூலக்கூறுகள் 12 x ஐக் கொடுக்கும். ஏடிபியின் 8 = 96 மூலக்கூறுகள்.
இவ்வாறு, மொத்தத்தில், பால்மிடிக் அமிலத்தின் முழுமையான β- ஆக்சிஜனேற்றத்துடன், 35 + 96 = 131 ஏடிபி மூலக்கூறுகள் உருவாகின்றன. பால்மிடிக் அமிலத்தின் (பால்மிடோயில்-கோஏ) செயலில் உள்ள வடிவத்தை உருவாக்குவதற்கு ஆரம்பத்தில் செலவழிக்கப்பட்ட ஒரு ஏடிபி மூலக்கூறைக் கணக்கில் எடுத்துக் கொண்டால், விலங்கு நிலைமைகளின் கீழ் ஒரு பால்மிடிக் அமில மூலக்கூறின் முழுமையான ஆக்சிஜனேற்றத்திற்கான மொத்த ஆற்றல் விளைச்சல் 131 - 1 = 130 ஆக இருக்கும். ஏடிபி மூலக்கூறுகள்.
நீராற்பகுப்பு ட்ரைகிளிசரைடுகள் கணைய லிபேஸ் மூலம் மேற்கொள்ளப்படுகிறது. அதன் உகந்த pH = 8, இது TG ஐ முக்கியமாக 1 மற்றும் 3 நிலைகளில் ஹைட்ரோலைஸ் செய்கிறது, 2 இலவச கொழுப்பு அமிலங்கள் மற்றும் 2-monoacylglycerol (2-MG) உருவாகிறது. 2-MG ஒரு நல்ல குழம்பாக்கி. 2-MG இல் 28% ஐசோமரேஸ் மூலம் 1-MG ஆக மாற்றப்படுகிறது. 1-MG இன் பெரும்பாலானவை கணைய லிபேஸால் கிளிசரால் மற்றும் கொழுப்பு அமிலமாக ஹைட்ரோலைஸ் செய்யப்படுகிறது.கணையத்தில், கணைய லிபேஸ் புரதம் கோலிபேஸுடன் இணைந்து ஒருங்கிணைக்கப்படுகிறது. கோலிபேஸ் ஒரு செயலற்ற வடிவத்தில் உருவாகிறது மற்றும் பகுதி புரோட்டியோலிசிஸ் மூலம் டிரிப்சின் மூலம் குடலில் செயல்படுத்தப்படுகிறது. கோலிபேஸ், அதன் ஹைட்ரோபோபிக் டொமைனுடன், லிப்பிட் துளியின் மேற்பரப்பில் பிணைக்கிறது, மேலும் அதன் ஹைட்ரோஃபிலிக் டொமைன் கணைய லிபேஸின் செயலில் உள்ள மையத்தை TG க்கு முடிந்தவரை நெருக்கமாக கொண்டு வர உதவுகிறது, இது அவற்றின் நீராற்பகுப்பை துரிதப்படுத்துகிறது.
|
பழுப்பு கொழுப்பு திசு |
|
|
அளவு |
பெரியவர்களில் சிறியவர், புதிதாகப் பிறந்தவர்களில் அதிகம் |
|
உள்ளூர்மயமாக்கல் |
அதன் தூய வடிவத்தில்: சிறுநீரகங்கள் மற்றும் தைராய்டு சுரப்பிக்கு அருகில். கலப்பு கொழுப்பு திசு: தோள்பட்டை கத்திகளுக்கு இடையில், மார்பு மற்றும் தோள்களில். |
|
இரத்த வழங்கல் |
மிகவும் நல்லது |
|
அடிபோசைட்டுகளின் அமைப்பு |
சைட்டோபிளாஸில் கொழுப்பின் பல சிறிய துளிகள் உள்ளன, கரு மற்றும் உறுப்புகள் செல்லின் மையத்தில் அமைந்துள்ளன, பல மைட்டோகாண்ட்ரியா மற்றும் சைட்டோக்ரோம்கள் உள்ளன. |
|
வெப்ப உருவாக்கம் |
|
மைட்டோகாண்ட்ரியல் மேட்ரிக்ஸில் ஆக்ஸிஜனேற்றம் ஏற்படுகிறது. முதலில், கொழுப்பு அமிலம் செயல்படுத்தப்படுகிறது: 1 .ஒவ்வொரு அமிலத்தின் சைட்டோபிளாஸிலும் CoA-8H மற்றும் ATP ஆற்றலைப் பயன்படுத்தி செயல்படுத்தப்படுகிறது. 2. செயலில் உள்ள கொழுப்பு அமிலம், அசைல்-கோஏ, சைட்டோசோலில் இருந்து மைட்டோகாண்ட்ரியல் மேட்ரிக்ஸுக்கு (எம்சி) கொண்டு செல்லப்படுகிறது. CoA-8H சைட்டோசோலில் உள்ளது, மேலும் கொழுப்பு அமில எச்சம் - அசைல் - கார்னைடைனுடன் இணைந்து (லத்தீன் - கார்னைடைன் - இறைச்சி - கார்னைடைன் தசை திசுக்களில் இருந்து தனிமைப்படுத்தப்படுகிறது) அசைல்-கார்னைடைனை உருவாக்குகிறது, இது மைட்டோகாண்ட்ரியாவின் இடைச்சவ்வு இடைவெளியில் நுழைகிறது. மைட்டோகாண்ட்ரியாவின் இன்டர்மெம்பிரேன் இடத்திலிருந்து, அசைல்-கார்னைடைன் வளாகம் மைட்டோகாண்ட்ரியல் மேட்ரிக்ஸுக்கு மாற்றப்படுகிறது. இந்த வழக்கில், கார்னைடைன் இடைச்சவ்வு இடத்தில் உள்ளது. மேட்ரிக்ஸில், அசைல் CoA-8H உடன் இணைகிறது. 3. ஆக்சிஜனேற்றம். செயலில் உள்ள கொழுப்பு அமிலம் MC மேட்ரிக்ஸில் உருவாகிறது, இது இறுதி தயாரிப்புகளுக்கு ஆக்சிஜனேற்ற எதிர்வினைகளுக்கு உட்படுகிறது. பீட்டா ஆக்சிஜனேற்றத்தில், கொழுப்பு அமிலத்தின் பீட்டா நிலையில் உள்ள CH2- குழுவானது C- குழுவிற்கு ஆக்சிஜனேற்றம் செய்யப்படுகிறது. இந்த வழக்கில், டீஹைட்ரஜனேற்றம் இரண்டு நிலைகளில் நிகழ்கிறது: அசைல் டீஹைட்ரஜனேஸ் (ஃபிளேவின் என்சைம், ஹைட்ரஜன் எபிக்வினோனுக்கு மாற்றப்படுகிறது) மற்றும் பீட்டா-ஹைட்ராக்ஸிசைல் டீஹைட்ரஜனேஸ் (ஹைட்ரஜன் ஏற்பி NAD +) ஆகியவற்றின் பங்கேற்புடன். பின்னர் பீட்டா-கெட்டோஅசில்-கோஏ, தியோலேஸ் என்ற நொதியின் செயல்பாட்டின் கீழ், அசிடைல் கோஏ மற்றும் அசைல்-கோஏ என உடைந்து, அசல் உடன் ஒப்பிடும்போது 2 கார்பன் அணுக்களால் சுருக்கப்படுகிறது. இந்த அசைல்-கோஏ மீண்டும் பீட்டா-ஆக்சிஜனேற்றத்திற்கு உட்படுகிறது. இந்த செயல்முறையை மீண்டும் மீண்டும் செய்வது, கொழுப்பு அமிலம் அசைல்-CoA க்கு முழுமையான முறிவுக்கு வழிவகுக்கிறது. கொழுப்பு அமிலங்களின் ஆக்சிஜனேற்றம். 2 நிலைகளை உள்ளடக்கியது: 1. அமிலத்தின் சி-டெர்மினஸிலிருந்து அசிடைல்-கோஏ வடிவில் இரண்டு கார்பன் துண்டின் தொடர்ச்சியான பிளவு; 2. கிரெப்ஸ் சுழற்சியில் அசிடைல்-CoA இன் ஆக்சிஜனேற்றம் CO2 மற்றும் H2O. கொழுப்பு அமில ஆக்சிஜனேற்றத்தின் ஆற்றல் மதிப்பு. ஸ்டீரிக் அமிலம் (C 18) 9 அசிடைல்-CoA உருவாக்கத்துடன் 8 ஆக்சிஜனேற்ற சுழற்சிகளுக்கு உட்படுகிறது. ஒவ்வொரு ஆக்சிடேஷன் சுழற்சியிலும், 8 * 5 ATP = 40 ATP உருவாகிறது, அசிடைல்-CoA 9 * 12 ATP = 108 ATP ஐ உருவாக்குகிறது. மொத்தம்: 148 ஏடிபி, ஆனால் 1 ஏடிபி சைட்டோசோலில் கொழுப்பு அமிலத்தை செயல்படுத்துவதற்கு செலவிடப்படுகிறது, எனவே மொத்தம் 147 ஏடிபி
β - அதிக கொழுப்பு அமிலங்களின் ஆக்சிஜனேற்றம் (HFAs). செயல்முறையின் ஆற்றல் திறன் (நிறைவுற்ற மற்றும் நிறைவுறா கொழுப்பு அமிலங்களுக்கு). திசுக்களால் குளுக்கோஸின் பயன்பாட்டில் IVFA இன் திசு ஆக்சிஜனேற்றத்தின் தாக்கம்.
β-ஆக்சிஜனேற்றம் - கிளைக்கப்படாத நடுத்தர மற்றும் குறுகிய ஹைட்ரோகார்பன் சங்கிலிகள் கொண்ட கொழுப்பு அமிலங்களின் வினையூக்கத்தின் ஒரு குறிப்பிட்ட பாதை. மைட்டோகாண்ட்ரியல் மேட்ரிக்ஸில் β-ஆக்சிஜனேற்றம் ஏற்படுகிறது, இதன் போது 2 C அணுக்கள் அசிடைல்-CoA வடிவத்தில் FA இன் C முனையிலிருந்து தொடர்ச்சியாக பிரிக்கப்படுகின்றன. FA இன் β-ஆக்சிஜனேற்றம் ஏரோபிக் நிலைமைகளின் கீழ் மட்டுமே நிகழ்கிறது மற்றும் அதிக அளவு ஆற்றலின் மூலமாகும். FA இன் β-ஆக்சிஜனேற்றம் சிவப்பு எலும்பு தசைகள், இதய தசை, சிறுநீரகங்கள் மற்றும் கல்லீரல் ஆகியவற்றில் தீவிரமாக நிகழ்கிறது. FAகள் நரம்பு திசுக்களுக்கு ஆற்றல் ஆதாரமாக செயல்படாது, ஏனென்றால் மற்ற ஹைட்ரோபோபிக் பொருட்களைப் போல FAகள் இரத்த-மூளைத் தடையின் வழியாக செல்லாது.உண்ணாவிரதம் மற்றும் உடல் உழைப்பின் போது உறிஞ்சப்பட்ட பிந்தைய காலத்தில் FA களின் β-ஆக்சிஜனேற்றம் அதிகரிக்கிறது. அதே நேரத்தில், கொழுப்பு திசுக்களில் இருந்து FA களை அணிதிரட்டுவதன் விளைவாக இரத்தத்தில் FA களின் செறிவு அதிகரிக்கிறது.
எல்சிடி செயல்படுத்தல்
Acyl-CoA உருவாக்கத்துடன் FA மற்றும் HSCoA க்கு இடையே உயர் ஆற்றல் பிணைப்பை உருவாக்குவதன் விளைவாக FA செயல்படுத்தப்படுகிறது. இந்த எதிர்வினை அசைல்-கோஏ சின்தேடேஸ் என்ற நொதியால் வினையூக்கப்படுகிறது:
RCOOH + HSKoA + ATP → RCO~ScoA + AMP+ PPn
பைரோபாஸ்பேட் பைரோபாஸ்பேடேஸ் என்ற நொதியால் ஹைட்ரோலைஸ் செய்யப்படுகிறது: H 4 P 2 O 7 + H 2 O → 2H 3 PO 4
சைட்டோசோல் (மைட்டோகாண்ட்ரியாவின் வெளிப்புற மென்படலத்தில்) மற்றும் மைட்டோகாண்ட்ரியல் மேட்ரிக்ஸில் அசைல்-கோஏ சின்தேடேஸ்கள் காணப்படுகின்றன. இந்த நொதிகள் வெவ்வேறு ஹைட்ரோகார்பன் சங்கிலி நீளம் கொண்ட FA களுக்கான தனித்தன்மையில் வேறுபடுகின்றன.
போக்குவரத்து எல்சிடி. மைட்டோகாண்ட்ரியல் மேட்ரிக்ஸில் FAகளின் போக்குவரத்து கார்பன் சங்கிலியின் நீளத்தைப் பொறுத்தது.
குறுகிய மற்றும் நடுத்தர சங்கிலி நீளம் கொண்ட FAகள் (4 முதல் 12 C அணுக்கள் வரை) பரவல் மூலம் மைட்டோகாண்ட்ரியல் மேட்ரிக்ஸில் ஊடுருவ முடியும். மைட்டோகாண்ட்ரியல் மேட்ரிக்ஸில் உள்ள அசைல்-கோஏ சின்தேடேஸ்களால் இந்த எஃப்ஏக்கள் செயல்படுத்தப்படுகிறது.நீண்ட சங்கிலி எஃப்ஏக்கள் முதலில் சைட்டோசோலில் செயல்படுத்தப்படுகின்றன (வெளிப்புற மைட்டோகாண்ட்ரியல் சவ்வில் உள்ள அசைல்-கோஏ சின்தேடேஸ்கள் மூலம்), பின்னர் மைட்டோகாண்ட்ரியல் சிஸ்டம் மேட்ரிக்ஸ் மூலம் மைட்டோகாண்ட்ரியல் அமைப்புக்கு மாற்றப்படுகிறது. கார்னைடைன் பயன்படுத்தி. கார்னைடைன் உணவில் இருந்து வருகிறது அல்லது வைட்டமின் சி பங்கேற்புடன் லைசின் மற்றும் மெத்தியோனைனிலிருந்து ஒருங்கிணைக்கப்படுகிறது.
மைட்டோகாண்ட்ரியாவின் வெளிப்புற சவ்வில், கார்னைடைன் அசைல்ட்ரான்ஸ்ஃபெரேஸ் I (கார்னைடைன் பால்மிடோல்ட்ரான்ஸ்ஃபெரேஸ் I) என்ற நொதியானது, அசில்கார்னைடைனை உருவாக்குவதற்கு CoA இலிருந்து கார்னைடைனுக்கு அசைலை மாற்றுகிறது;
அசில்கார்னிடைன் இடைச்சவ்வு இடைவெளி வழியாக உள் சவ்வின் வெளிப்புறத்திற்கு செல்கிறது மற்றும் கார்னைடைன் அசைல்கார்னைடைன் டிரான்ஸ்லோகேஸ் மூலம் உள் மைட்டோகாண்ட்ரியல் சவ்வின் உள் மேற்பரப்புக்கு கொண்டு செல்லப்படுகிறது;
கார்னைடைன் அசைல்ட்ரான்ஸ்ஃபெரேஸ் II என்ற நொதியானது, கார்னைடைனில் இருந்து இன்ட்ராமிட்டோகாண்ட்ரியல் HSCoA க்கு அசைல்-கோஏவை உருவாக்குவதற்கு அசைலை மாற்றுவதற்கு ஊக்கமளிக்கிறது;
இலவச கார்னைடைன் உள் மைட்டோகாண்ட்ரியல் மென்படலத்தின் சைட்டோசோலிக் பக்கத்திற்கு அதே டிரான்ஸ்லோகேஸ் மூலம் திருப்பி அனுப்பப்படுகிறது.
எதிர்வினைகள் FA இன் β-ஆக்சிஜனேற்றம்
1. β-ஆக்சிஜனேற்றம் FAD-சார்ந்த அசைல்-CoA டீஹைட்ரோஜினேஸால் அசைல்-CoA இன் டீஹைட்ரஜனேற்றத்துடன் தொடங்குகிறது, இது Enoyl-CoA இன் α- மற்றும் β-C அணுக்களுக்கு இடையே இரட்டைப் பிணைப்பை (டிரான்ஸ்) உருவாக்குகிறது. குறைக்கப்பட்ட FADN 2, CPE இல் ஆக்ஸிஜனேற்றம், 2 ATP மூலக்கூறுகளின் தொகுப்பை உறுதி செய்கிறது;
2. Enoyl-CoA ஹைட்ராடேஸ், Enoyl-CoA இன் இரட்டைப் பிணைப்பில் தண்ணீரைச் சேர்த்து β-ஹைட்ராக்ஸிசைல்-CoA ஐ உருவாக்குகிறது;
3. β-ஹைட்ராக்ஸிசைல்-CoA ஆனது NAD-சார்ந்த டீஹைட்ரோஜினேஸால் β-ketoacyl-CoA ஆக ஆக்சிஜனேற்றப்படுகிறது. குறைக்கப்பட்ட NADH 2, CPE ஆக ஆக்ஸிஜனேற்றம், 3 ATP மூலக்கூறுகளின் தொகுப்பை உறுதி செய்கிறது;
4. HCoA பங்கேற்புடன் தியோலேஸ் β-ketoacyl-CoA இலிருந்து அசிடைல்-கோஏவை பிளவுபடுத்துகிறது. 4 எதிர்வினைகளின் விளைவாக, Acyl-CoA உருவாகிறது, இது முந்தைய Acyl-CoA ஐ விட 2 கார்பன்களால் குறைவாக உள்ளது. உருவான அசிடைல்-கோஏ, டிசிஏ சுழற்சியில் ஆக்ஸிஜனேற்றப்பட்டது, சிபிஇயில் 12 ஏடிபி மூலக்கூறுகளின் தொகுப்பை உறுதி செய்கிறது.
Acyl-CoA மீண்டும் β-ஆக்சிஜனேற்ற எதிர்வினைகளில் நுழைகிறது. Acyl-CoA ஆனது 2 C அணுக்களுடன் அசிடைல்-CoA ஆக மாறும் வரை (FA சம எண்ணிக்கையில் C அணுக்கள் இருந்தால்) அல்லது 3 C அணுக்கள் கொண்ட Butyryl-CoA ஆக மாறும் வரை (FA இல் ஒற்றைப்படை எண்ணிக்கையிலான C அணுக்கள் இருந்தால்).
சம எண்ணிக்கையிலான கார்பன் அணுக்கள் கொண்ட நிறைவுற்ற கொழுப்பு அமிலங்களின் ஆக்சிஜனேற்றத்தின் ஆற்றல் சமநிலை
FA செயல்படுத்தப்படும் போது, ATP இன் 2 மேக்ரோஜெர்ஜிக் பிணைப்புகள் செலவிடப்படுகின்றன.
சம எண்ணிக்கையிலான C அணுக்கள் கொண்ட நிறைவுற்ற FA ஆக்சிஜனேற்றத்தின் போது, FADH 2, NADH 2 மற்றும் அசிடைல்-CoA மட்டுமே உருவாகின்றன.
β-ஆக்சிஜனேற்றத்தின் 1 சுழற்சியின் போது, 1 FADH 2, 1 NADH 2 மற்றும் 1 அசிடைல்-CoA உருவாகிறது, இது ஆக்சிஜனேற்றத்தின் போது 2 + 3 + 12 = 17 ATP ஐ உருவாக்குகிறது.
FA இன் β-ஆக்சிஜனேற்றத்தின் போது சுழற்சிகளின் எண்ணிக்கை = (FA/2)-1 இல் உள்ள C அணுக்களின் எண்ணிக்கை. β-ஆக்சிஜனேற்றத்தின் போது, பால்மிடிக் அமிலம் (16/2)-1 = 7 சுழற்சிகளுக்கு உட்படுகிறது. 7 சுழற்சிகளில், 17*7=119 ATP உருவாகிறது.
β-ஆக்சிஜனேற்றத்தின் கடைசி சுழற்சியானது கூடுதல் அசிடைல்-கோஏ உருவாக்கத்துடன் சேர்ந்துள்ளது, இது ஆக்சிஜனேற்றத்தின் போது 12 ஏடிபியை உருவாக்குகிறது.
இவ்வாறு, பால்மிடிக் அமிலத்தின் ஆக்சிஜனேற்றம் உற்பத்தி செய்கிறது: -2+119+12=129 ATP.
β-ஆக்சிஜனேற்றத்திற்கான சுருக்கச் சமன்பாடு, palmitoyl-CoA:
C 15 H 31 CO-CoA + 7 FAD + 7 NAD + + 7 HSKoA → 8 CH 3 -CO-KoA + 7 FADH 2 + 7 NADH 2
ஒற்றைப்படை எண்ணிக்கையிலான கார்பன் அணுக்கள் கொண்ட நிறைவுற்ற கொழுப்பு அமிலங்களின் ஆக்சிஜனேற்றத்தின் ஆற்றல் சமநிலை
தொடக்கத்தில் ஒற்றைப்படை எண்ணிக்கையிலான C அணுக்கள் கொண்ட நிறைவுற்ற FA இன் β-ஆக்சிஜனேற்றம் இரட்டை எண்ணைப் போலவே தொடர்கிறது. ஏடிபியின் 2 மேக்ரோஜெர்ஜிக் பிணைப்புகள் செயல்படுத்துவதற்கு செலவிடப்படுகின்றன.
17 C அணுக்கள் கொண்ட FA ஆனது β-ஆக்சிஜனேற்றம் 17/2-1 = 7 சுழற்சிகளுக்கு உட்படுகிறது. 1 சுழற்சியில், 2+3+12=17 ATP ஆனது 1 FADN 2, 1 NADH 2 மற்றும் 1 Acetyl-CoA ஆகியவற்றிலிருந்து உருவாகிறது. 7 சுழற்சிகளில், 17*7=119 ATP உருவாகிறது.
β-ஆக்சிஜனேற்றத்தின் கடைசி சுழற்சியானது அசிடைல்-கோஏ அல்ல, ஆனால் 3 சி அணுக்கள் கொண்ட ப்ரோபியோனைல்-கோஏ உருவாக்கத்துடன் சேர்ந்துள்ளது.
ப்ரோபியோனைல்-கோஏ 1 ஏடிபி விலையில் ப்ரோபியோனைல்-கோஏ கார்பாக்சிலேஸ் மூலம் டி-மெத்தில்மலோனைல்-கோஏவை உருவாக்குகிறது, இது ஐசோமரைசேஷனுக்குப் பிறகு முதலில் எல்-மெத்தில்மலோனைல்-கோஏவாகவும் பின்னர் சுசினில்-கோஏவாகவும் மாற்றப்படுகிறது. Succinyl-CoA TCA சுழற்சியில் சேர்க்கப்பட்டுள்ளது மற்றும் ஆக்சிஜனேற்றத்தின் போது, PCA மற்றும் 6 ATP ஐ உருவாக்குகிறது. PIKE குளுக்கோஸ் தொகுப்புக்கான குளுக்கோனோஜெனீசிஸில் நுழைய முடியும். வைட்டமின் பி 12 குறைபாடு இரத்தத்தில் மெத்தில்மலோனைல் மற்றும் சிறுநீரில் வெளியேற்றத்திற்கு வழிவகுக்கிறது. FA ஆக்சிஜனேற்றத்தின் போது, பின்வருபவை உருவாகின்றன: -2+119-1+6=122 ATP.
17 C அணுக்கள் கொண்ட FAகளின் β-ஆக்சிஜனேற்றத்திற்கான ஒட்டுமொத்த சமன்பாடு:
C 16 H 33 CO-CoA + 7 FAD + 7 NAD + + 7 HSKoA → 7 CH 3 -CO-KoA + 1 C 2 H 5 -CO-KoA + 7 FADH 2 + 7 NADH 2
சம எண்ணிக்கையிலான கார்பன் அணுக்கள் கொண்ட நிறைவுறா கொழுப்பு அமிலங்களின் ஆக்சிஜனேற்றத்தின் ஆற்றல் சமநிலை
மனித உடலில் உள்ள FAகளில் பாதி நிறைவுறாதவை. இந்த அமிலங்களின் β-ஆக்சிஜனேற்றமானது இரட்டைப் பிணைப்பு C அணுக்கள் 3 மற்றும் 4 க்கு இடையில் இருக்கும் வரை வழக்கமான முறையில் தொடர்கிறது. என்சைம் enoyl-CoA ஐசோமரேஸ் பின்னர் இரட்டைப் பிணைப்பை 3-4 நிலையிலிருந்து 2-3 நிலைக்கு நகர்த்துகிறது. டிரான்ஸுக்கு இரட்டைப் பிணைப்பு, இது β-ஆக்சிஜனேற்றத்திற்கு அவசியம். இந்த β-ஆக்சிஜனேற்ற சுழற்சியில், இரட்டைப் பிணைப்பு ஏற்கனவே FA இல் இருப்பதால், முதல் டீஹைட்ரஜனேற்ற எதிர்வினை ஏற்படாது மற்றும் FADH 2 உருவாகாது. மேலும், β-ஆக்சிஜனேற்ற சுழற்சிகள் தொடர்கின்றன, வழக்கமான பாதையில் இருந்து வேறுபட்டவை அல்ல.
இரட்டைப் பிணைப்பு 1 FADN 2 மற்றும் அதற்கேற்ப, 2 ATP இல்லாவிட்டாலும், இரட்டைப் பிணைப்பு 1 FADN 2க்கு மட்டுமே, சம எண்ணிக்கையிலான C அணுக்களைக் கொண்ட நிறைவுற்ற FAக்களைப் போலவே ஆற்றல் சமநிலையும் கணக்கிடப்படுகிறது.
பால்மிட்டோலைல்-CoA இன் β-ஆக்சிஜனேற்றத்திற்கான ஒட்டுமொத்த சமன்பாடு:
C 15 H 29 CO-CoA + 6 FAD + 7 NAD + + 7 HSKoA → 8 CH 3 -CO-KoA + 6 FADH 2 + 7 NADH 2
பால்மிடோலிக் அமிலத்தின் β-ஆக்சிஜனேற்றத்தின் ஆற்றல் சமநிலை: -2+8*12+6*2+7*3=127 ATP.
பசி, உடல் செயல்பாடு → குளுகோகன், அட்ரினலின் → அடிபோசைட்டுகளில் டிஜி லிபோலிசிஸ் → இரத்தத்தில் எஃப்ஏ → β-ஆக்சிஜனேற்றம் தசைகளில் ஏரோபிக் நிலைமைகளின் கீழ், கல்லீரல் → 1) ஏடிபி; 2) ATP, NADH 2, அசிடைல்-CoA, (FA) → ↓ கிளைகோலிசிஸ் → நரம்பு திசு, இரத்த சிவப்பணுக்கள் போன்றவற்றிற்கு தேவையான குளுக்கோஸ் சேமிப்பு.
உணவு → இன்சுலின் → கிளைகோலிசிஸ் → அசிடைல்-கோஏ → மாலோனைல்-கோஏ மற்றும் எஃப்ஏ ஆகியவற்றின் தொகுப்பு
கல்லீரலில் உள்ள மலோனைல்-கோஏ → மலோனைல்-கோஏ → ↓ கார்னைடைன் அசைல்ட்ரான்ஸ்ஃபெரேஸ் I இன் தொகுப்பு
IVFA இன் உயிரியக்கவியல். பால்மிடேட் சின்தேஸ் வளாகத்தின் அமைப்பு. செயல்முறையின் வேதியியல் மற்றும் ஒழுங்குமுறை.
பால்மிடிக் அமில தொகுப்பு
மலோனைல்-கோஏ உருவாக்கம்
FA தொகுப்பின் முதல் எதிர்வினை அசிடைல்-கோஏவை மலோனைல்-கோஏவாக மாற்றுவதாகும். FA தொகுப்பில் இந்த ஒழுங்குமுறை எதிர்வினை அசிடைல்-CoA கார்பாக்சிலேஸால் வினையூக்கப்படுகிறது.
அசிடைல்-கோஏ கார்பாக்சிலேஸ் பயோட்டின் கொண்ட பல துணைக்குழுக்களைக் கொண்டுள்ளது.
எதிர்வினை 2 நிலைகளில் நிகழ்கிறது:
1) CO 2 + பயோட்டின் + ATP → biotin-COOH + ADP + Fn
2) அசிடைல்-CoA + பயோட்டின்-COOH → மலோனைல்-CoA + பயோட்டின்
அசிடைல்-கோஏ கார்பாக்சிலேஸ் பல வழிகளில் கட்டுப்படுத்தப்படுகிறது:
3) என்சைம் சப்யூனிட் வளாகங்களின் சங்கம்/விலகல். அதன் செயலற்ற வடிவத்தில், அசிடைல்-கோஏ கார்பாக்சிலேஸ் என்பது 4 துணை அலகுகளைக் கொண்ட ஒரு சிக்கலானது. சிட்ரேட் வளாகங்களின் ஒன்றியத்தைத் தூண்டுகிறது, இதன் விளைவாக நொதி செயல்பாடு அதிகரிக்கிறது. Palmitoyl-CoA வளாகங்களின் விலகல் மற்றும் என்சைம் செயல்பாட்டில் குறைவு ஏற்படுகிறது;
2) அசிடைல்-கோஏ கார்பாக்சிலேஸின் பாஸ்போரிலேஷன்/டிஃபோஸ்ஃபோரிலேஷன். குளுகோகன் அல்லது அட்ரினலின், அடினிலேட் சைக்லேஸ் அமைப்பின் மூலம், அசிடைல்-கோஏ கார்பாக்சிலேஸின் துணை அலகுகளின் பாஸ்போரிலேஷனைத் தூண்டுகிறது, இது அதன் செயலிழக்க வழிவகுக்கிறது. இன்சுலின் பாஸ்போபுரோட்டீன் பாஸ்பேடேஸை செயல்படுத்துகிறது, அசிடைல்-கோஏ கார்பாக்சிலேஸ் டிஃபோஸ்ஃபோரிலேட்டட் ஆகும். பின்னர், சிட்ரேட்டின் செல்வாக்கின் கீழ், என்சைம் புரோட்டோமர்களின் பாலிமரைசேஷன் ஏற்படுகிறது, மேலும் அது செயலில் உள்ளது;
3) கார்போஹைட்ரேட்டுகள் நிறைந்த உணவுகளை நீண்ட காலமாக உட்கொள்வது மற்றும் கொழுப்புச் சத்து குறைவாக இருப்பதால், இன்சுலின் சுரப்பு அதிகரிக்கிறது, இது அசிடைல்-கோஏ கார்பாக்சிலேஸ், பால்மிடேட் சின்தேஸ், சிட்ரேட் லைஸ், ஐசோசிட்ரேட் டீஹைட்ரஜனேஸ் ஆகியவற்றின் தொகுப்பைத் தூண்டுகிறது மற்றும் எஃப்ஏ மற்றும் தொகுப்பை துரிதப்படுத்துகிறது. டி.ஜி. உண்ணாவிரதம் அல்லது கொழுப்பு நிறைந்த உணவை சாப்பிடுவது என்சைம்களின் தொகுப்பு குறைவதற்கு வழிவகுக்கிறது, அதன்படி, FA மற்றும் TG.
பால்மிடிக் அமிலத்தின் உருவாக்கம்
மலோனைல்-கோஏ உருவான பிறகு, பால்மிடிக் அமிலத்தின் தொகுப்பு மல்டிஎன்சைம் வளாகத்தில் தொடர்கிறது - கொழுப்பு அமிலம் சின்தேஸ் (பால்மிடோயில் சின்தேடேஸ்) .
பால்மிடோயில் சின்தேஸ் என்பது இரண்டு ஒத்த பாலிபெப்டைட் சங்கிலிகளைக் கொண்ட ஒரு டைமர் ஆகும். ஒவ்வொரு சங்கிலியிலும் 7 செயலில் உள்ள தளங்கள் மற்றும் ஒரு அசைல் பரிமாற்ற புரதம் (ACP) உள்ளது. ஒவ்வொரு சங்கிலியிலும் 2 SH குழுக்கள் உள்ளன: ஒரு SH குழு சிஸ்டைனுக்கு சொந்தமானது, மற்றொன்று பாஸ்போபாந்தெதிக் அமில எச்சத்திற்கு சொந்தமானது. ஒரு மோனோமரின் சிஸ்டைன் எஸ்ஹெச் குழு மற்ற புரோட்டோமரின் 4-பாஸ்போபான்டெதீனேட் எஸ்எச் குழுவுக்கு அடுத்ததாக அமைந்துள்ளது. இவ்வாறு, நொதியின் புரோட்டோமர்கள் "தலையிலிருந்து வால்" வரை ஏற்பாடு செய்யப்பட்டுள்ளன. ஒவ்வொரு மோனோமரும் அனைத்து வினையூக்கி தளங்களையும் கொண்டிருந்தாலும், 2 புரோட்டோமர்களின் சிக்கலானது செயல்பாட்டில் உள்ளது. எனவே, 2 LCக்கள் உண்மையில் ஒரே நேரத்தில் ஒருங்கிணைக்கப்படுகின்றன.
இந்த வளாகம் தொடர்ச்சியாக FA ரேடிக்கலை 2 C அணுக்களால் விரிவுபடுத்துகிறது, இதன் நன்கொடையாளர் மலோனைல்-CoA ஆகும்.
பால்மிடிக் அமிலம் தொகுப்பு எதிர்வினைகள்
1) அசிடைல் டிரான்ஸ்சைலேஸ் மையம் மூலம் அசிடைலை CoA இலிருந்து சிஸ்டைனின் SH குழுவிற்கு மாற்றுதல்;
2) மலோனைலை CoA இலிருந்து ACP இன் SH குழுவிற்கு மலோனைல் டிரான்சைலேஸ் மையம் மூலம் மாற்றுதல்;
3) கெட்டோஅசில் சின்தேஸ் மையத்தில், அசிடைல் குழு மலோனைல் குழுவுடன் ஒடுங்கி கெட்டோஅசைலை உருவாக்கி CO 2 ஐ வெளியிடுகிறது.
4) கீட்டோஅசைல் ஹைட்ராக்ஸிசைலுக்கு கெட்டோஅசில் ரிடக்டேஸால் குறைக்கப்படுகிறது;
5) ஆக்ஸிசைல் ஹைட்ராடேஸால் ஈனோயிலாக நீரிழப்பு செய்யப்படுகிறது;
6) ஈனாய்ல் ரிடக்டேஸால் அசைலுக்கு குறைக்கப்படுகிறது.
எதிர்வினைகளின் முதல் சுழற்சியின் விளைவாக, 4 C அணுக்கள் (பியூட்டில்) கொண்ட ஒரு அசைல் உருவாகிறது. அடுத்து, ப்யூடிரில் நிலை 2 இலிருந்து 1 வது இடத்திற்கு மாற்றப்படுகிறது (எங்கு எதிர்வினைகளின் முதல் சுழற்சியின் தொடக்கத்தில் அசிடைல் அமைந்திருந்தது). ப்யூடிரில் பின்னர் அதே மாற்றங்களுக்கு உட்படுகிறது மற்றும் 2 C அணுக்களால் (மலோனைல்-CoA இலிருந்து) நீட்டிக்கப்படுகிறது.
ஒரு பால்மிடிக் அமிலம் ரேடிக்கல் உருவாகும் வரை இதேபோன்ற எதிர்வினைகள் மீண்டும் மீண்டும் செய்யப்படுகின்றன, இது தியோஸ்டெரேஸ் மையத்தின் செயல்பாட்டின் கீழ், நொதி வளாகத்திலிருந்து ஹைட்ரோலைட்டிகல் முறையில் பிரிக்கப்பட்டு, இலவச பால்மிடிக் அமிலமாக மாறும்.
அசிடைல்-கோஏ மற்றும் மலோனைல்-கோஏ ஆகியவற்றிலிருந்து பால்மிடிக் அமிலத்தின் தொகுப்புக்கான ஒட்டுமொத்த சமன்பாடு பின்வருமாறு:
CH 3 -CO-SKoA + 7 HOOC-CH 2 -CO-SKoA + 14 NADPH 2 → C 15 H 31 COOH + 7 CO 2 + 6
H 2 O + 8 HSKoA + 14 NADP +
பால்மிட்டிக் மற்றும் பிற FAகளில் இருந்து FAகளின் தொகுப்பு
நீளமான எதிர்வினைகளில் FAகளின் நீட்சி
கொழுப்பு அமிலத்தின் நீளம் நீட்டுதல் என்று அழைக்கப்படுகிறது. ER இல் பால்மிடிக் அமிலம் மற்றும் பிற நீண்ட FAகளின் நீட்சியின் விளைவாக FAகள் ஒருங்கிணைக்கப்படலாம். ஒவ்வொரு LC நீளத்திற்கும் நீள்வட்டங்கள் உள்ளன. எதிர்வினைகளின் வரிசை பால்மிடிக் அமிலத்தின் தொகுப்புக்கு ஒத்ததாக இருக்கிறது, ஆனால் இந்த விஷயத்தில் தொகுப்பு ACP உடன் அல்ல, ஆனால் CoA உடன் நிகழ்கிறது. கல்லீரலில் முக்கிய நீட்டல் தயாரிப்பு ஸ்டீரிக் அமிலம் ஆகும். நரம்பு திசுக்களில், நீண்ட சங்கிலி FA கள் (C = 20-24) உருவாகின்றன, அவை ஸ்பிங்கோலிப்பிட்களின் தொகுப்புக்கு அவசியமானவை.
டெசாச்சுரேஸ் எதிர்வினைகளில் நிறைவுறா FAகளின் தொகுப்பு
FA ரேடிக்கல்களில் இரட்டைப் பிணைப்புகளைச் சேர்ப்பது டெசாச்சுரேஷன் எனப்படும். டெசாச்சுரேஸ்களால் வினையூக்கப்படும் மோனோஆக்சிஜனேஸ் எதிர்வினைகளில் எஃப்ஏக்களின் தேய்மானம் ER இல் ஏற்படுகிறது.
ஸ்டீரோயில்-கோஏ டெசாச்சுரேஸ்- ஒருங்கிணைந்த நொதி, ஹீம் அல்லாத இரும்பு கொண்டிருக்கிறது. FA இல் 9 மற்றும் 10 கார்பன் அணுக்களுக்கு இடையில் 1 இரட்டைப் பிணைப்பை உருவாக்குகிறது. Stearoyl-CoA desaturase எலக்ட்ரான்களை சைட்டோக்ரோம் b 5 இலிருந்து 1 ஆக்ஸிஜன் அணுவிற்கு மாற்றுகிறது, புரோட்டான்களின் பங்கேற்புடன் இந்த ஆக்ஸிஜன் தண்ணீரை உருவாக்குகிறது. இரண்டாவது ஆக்ஸிஜன் அணு ஸ்டீரிக் அமிலத்துடன் இணைக்கப்பட்டு அதன் ஹைட்ராக்ஸிசைலை உருவாக்குகிறது, இது ஒலிக் அமிலமாக டீஹைட்ரஜனேற்றுகிறது.
மனித உடலில் இருக்கும் FA desaturases ஒன்பதாவது கார்பன் அணுவிற்கு தொலைவில் உள்ள FA களில் இரட்டைப் பிணைப்புகளை உருவாக்க முடியாது, எனவே ω-3 மற்றும் ω-6 குடும்பங்களின் FAகள் உடலில் ஒருங்கிணைக்கப்படுவதில்லை, அவை அவசியமானவை மற்றும் அவை உணவுடன் வழங்கப்பட வேண்டும். முக்கியமான ஒழுங்குமுறை செயல்பாடுகளைச் செய்யவும். தேய்மானத்தின் விளைவாக மனித உடலில் உருவாகும் முக்கிய FAகள் பால்மிடோலிக் மற்றும் ஒலிக் ஆகும்.
α-ஹைட்ராக்ஸி FAகளின் தொகுப்பு
பிற FAகளின் தொகுப்பு, α-ஹைட்ராக்ஸி அமிலங்கள், நரம்பு திசுக்களிலும் நிகழ்கின்றன. கலப்பு-செயல்பாட்டு ஆக்சிடேஸ்கள் ஹைட்ராக்சைலேட் C22 மற்றும் C24 அமிலங்கள் செரிப்ரோனிக் அமிலத்தை உருவாக்குகின்றன, இது மூளை கொழுப்புகளில் மட்டுமே காணப்படுகிறது.
கார்போஹைட்ரேட்டுகள் மனித உணவின் பெரும்பகுதியை உருவாக்குகின்றன மற்றும் உடலின் ஆற்றல் தேவைகளில் குறிப்பிடத்தக்க பகுதியை வழங்குகின்றன. ஒரு சீரான உணவுடன், கார்போஹைட்ரேட்டுகளின் தினசரி அளவு புரதங்கள் மற்றும் கொழுப்புகளின் அளவை விட சராசரியாக 4 மடங்கு அதிகமாகும்.
ஊட்டச்சத்தில் கார்போஹைட்ரேட்டின் பங்கு:
1. கார்போஹைட்ரேட் செய்கிறது ஆற்றல் செயல்பாடு. 1 கிராம் கார்போஹைட்ரேட்டுகள் ஆக்ஸிஜனேற்றப்படும்போது, 4.1 கிலோகலோரி ஆற்றல் வெளியிடப்படுகிறது. குளுக்கோஸ், இதில் கார்போஹைட்ரேட்டுகளின் பெரும்பகுதி உடைக்கப்படுகிறது, இது உடலின் முக்கிய ஆற்றல் அடி மூலக்கூறு ஆகும்.
2. தசை செயல்பாடுகுறிப்பிடத்தக்க குளுக்கோஸ் நுகர்வு சேர்ந்து. உடல் வேலையின் போது, கார்போஹைட்ரேட்டுகள் முதலில் உட்கொள்ளப்படுகின்றன, மேலும் அவற்றின் இருப்புக்கள் (கிளைகோஜன்) குறைக்கப்படும்போது மட்டுமே கொழுப்புகள் பரிமாற்றத்தில் சேர்க்கப்படுகின்றன.
3. சாதாரண செயல்பாட்டிற்கு கார்போஹைட்ரேட்டுகள் அவசியம் மத்திய நரம்பு அமைப்பு,இரத்தத்தில் உள்ள குளுக்கோஸ் குறைபாட்டிற்கு செல்கள் மிகவும் உணர்திறன் கொண்டவை.
4. கார்போஹைட்ரேட் செய்கிறது கட்டமைப்பு செயல்பாடு.எளிய கார்போஹைட்ரேட்டுகள் கிளைகோபுரோட்டின்களை உருவாக்குவதற்கான ஆதாரமாக செயல்படுகின்றன, இது இணைப்பு திசுக்களின் அடிப்படையை உருவாக்குகிறது.
5. கார்போஹைட்ரேட்டுகள் ஈடுபட்டுள்ளன புரதங்கள் மற்றும் கொழுப்புகளின் வளர்சிதை மாற்றத்தில்.கார்போஹைட்ரேட்டுகளிலிருந்து கொழுப்புகள் உருவாகலாம்.
6. தாவர தோற்றத்தின் கார்போஹைட்ரேட்டுகள் (செல்லுலோஸ், பெக்டின் பொருட்கள்) குடல் இயக்கத்தைத் தூண்டுகிறது மற்றும் அதில் குவிந்துள்ள நச்சுப் பொருட்களின் நீக்குதலை ஊக்குவிக்கிறது.
ஆதாரங்கள்கார்போஹைட்ரேட்டுகள் முக்கியமாக சேவை செய்கின்றன தாவர பொருட்கள்,குறிப்பாக மாவு பொருட்கள், தானியங்கள், இனிப்புகள். பெரும்பாலான உணவுகளில், கார்போஹைட்ரேட்டுகள் ஸ்டார்ச் வடிவத்திலும், குறைந்த அளவிற்கு, டிசாக்கரைடுகள் (பால், சர்க்கரைவள்ளிக்கிழங்குகள், பழங்கள் மற்றும் பெர்ரி) வடிவத்திலும் வழங்கப்படுகின்றன. கார்போஹைட்ரேட்டுகளை சிறப்பாக உறிஞ்சுவதற்கு, அவற்றில் பெரும்பாலானவை ஸ்டார்ச் வடிவத்தில் உடலில் நுழைவது அவசியம்.
ஸ்டார்ச் படிப்படியாக இரைப்பைக் குழாயில் குளுக்கோஸாக உடைக்கப்படுகிறது, இது சிறிய பகுதிகளாக இரத்தத்தில் நுழைகிறது, இது அதன் பயன்பாட்டை மேம்படுத்துகிறது மற்றும் நிலையான இரத்த சர்க்கரை அளவை பராமரிக்கிறது. அதிக அளவு சர்க்கரை ஒரே நேரத்தில் நிர்வகிக்கப்படும் போது, இரத்தத்தில் குளுக்கோஸின் செறிவு கூர்மையாக அதிகரிக்கிறது, மேலும் அது சிறுநீரில் வெளியேற்றத் தொடங்குகிறது. 64% கார்போஹைட்ரேட்டுகள் ஸ்டார்ச் வடிவத்திலும், 36% சர்க்கரை வடிவிலும் உட்கொள்ளும்போது மிகவும் சாதகமான நிலைமைகள் கருதப்படுகின்றன.
நுகர்வு விகிதம்கார்போஹைட்ரேட்டுகள் வேலையின் தீவிரத்தைப் பொறுத்தது. உடல் வேலையின் போது, கார்போஹைட்ரேட்டுகள் அதிக அளவில் தேவைப்படுகின்றன. சராசரியாக, 1 கிலோ உடல் எடைக்கு தேவைப்படுகிறது 4-6-8 ஒரு நாளைக்கு கிராம் கார்போஹைட்ரேட், அதாவது. புரதங்கள் மற்றும் கொழுப்புகளை விட சுமார் 4 மடங்கு அதிகம்.
அதிகப்படியான கார்போஹைட்ரேட் உட்கொள்ளல்உடல் பருமன் மற்றும் இரைப்பைக் குழாயின் அதிகப்படியான சுமைக்கு வழிவகுக்கும், ஏனெனில் கார்போஹைட்ரேட்டுகள் நிறைந்த தாவர உணவுகள் பொதுவாக அதிக அளவு கொண்டவை, கனமான உணர்வை ஏற்படுத்துகின்றன மற்றும் உணவின் ஒட்டுமொத்த செரிமானத்தை பாதிக்கின்றன.
கார்போஹைட்ரேட் பற்றாக்குறைஇரத்தச் சர்க்கரைக் குறைவு நிலைமைகளை உருவாக்கும் ஆபத்து காரணமாக உணவிலும் விரும்பத்தகாதது. கார்போஹைட்ரேட் குறைபாடு, ஒரு விதியாக, பொதுவான பலவீனம், தூக்கமின்மை, நினைவாற்றல் குறைதல், மன மற்றும் உடல் செயல்திறன், தலைவலி, புரதங்களின் செரிமானம் குறைதல், வைட்டமின்கள், அமிலத்தன்மை போன்றவை. இது சம்பந்தமாக, தினசரி உணவில் கார்போஹைட்ரேட் அளவு கூடாது 300 கிராம் குறைவாக இருக்க வேண்டும்
கார்போஹைட்ரேட்டுகளின் குழுவுடன் நெருக்கமாக தொடர்புடையது, மனித உடலால் மோசமாக ஜீரணிக்கக்கூடிய பெரும்பாலான தாவர உணவுகளில் காணப்படும் பொருட்கள் - பெக்டின் பொருட்கள் (செரிமான கார்போஹைட்ரேட்டுகள்) மற்றும் ஃபைபர்.
பெக்டிக் பொருட்கள் ஆகும்அதிக உறிஞ்சும் (உறிஞ்சும்) திறன் கொண்ட காய்கறி ஜெல்லிங் பொருட்கள். செரிமான அமைப்பு, தீக்காயங்கள் மற்றும் புண்களின் நோய்களுக்கு சிகிச்சையளிப்பதில் அவை ஒரு நன்மை பயக்கும், மேலும் சில நச்சுப் பொருட்களை நடுநிலையாக்கும் திறனைக் கொண்டுள்ளன (அவை உடலில் இருந்து ஈய கலவைகள் போன்ற கனரக உலோக உப்புகளை அகற்றுவதில் குறிப்பாக செயலில் உள்ளன).
ஆரஞ்சு, ஆப்பிள், கருப்பு திராட்சை வத்தல் மற்றும் பிற பழங்கள் மற்றும் பெர்ரிகளில் பெக்டின் பொருட்கள் நிறைய உள்ளன.
செல்லுலோஸ்(மற்ற பெயர்கள் - கரடுமுரடான காய்கறி, அல்லது ஜீரணிக்க முடியாத, அல்லது உணவு, அல்லது உணவு நார்ச்சத்து) என்பது தாவர உணவுகளின் பாரிய செல் சுவர்களின் ஒரு பகுதியாக இருக்கும் பாலிசாக்கரைடு ஆகும். இது ஒரு நார்ச்சத்து, மாறாக கரடுமுரடான அமைப்பைக் கொண்டுள்ளது.
உணவு நார்ச்சத்தின் பொதுவான ஆதாரங்கள் தவிடு, ரொட்டி மற்றும் தானியங்கள் (குறிப்பாக பக்வீட் மற்றும் ஓட்ஸ்). பல காய்கறிகள், பழங்கள், இலைகள் மற்றும் தாவரங்களின் தண்டுகளில் பெரிய அளவில் காணப்படுகின்றன; குறிப்பாக தானியங்களின் ஓடுகளிலும் பழங்களின் தோல்களிலும் இது நிறைய உள்ளது. காய்கறிகள் மற்றும் பழங்கள் பதப்படுத்தல் போது, உணவு நார் முற்றிலும் பாதுகாக்கப்படுகிறது (கூழ் இல்லாமல் சாறுகள் தவிர).
அதிக கலோரி உள்ளடக்கம் இல்லாமல், பெரும்பாலான காய்கறிகள் மற்றும் பழங்கள், இருப்பினும், ஜீரணிக்க முடியாத கார்போஹைட்ரேட்டுகளின் அதிக உள்ளடக்கம் காரணமாக, விரைவான மற்றும் நிலையான திருப்தி உணர்வுக்கு பங்களிக்கின்றன: உணவு நார்ச்சத்து நிறைய திரவத்தை உறிஞ்சும் திறனைக் கொண்டிருப்பதால், அவை வீங்குகின்றன. வயிறு, அதன் அளவின் ஒரு பகுதியை நிரப்பவும் - இதன் விளைவாக செறிவு வேகமாக நிகழ்கிறது. நார்ச்சத்துகள் ஒரு கலோரியை கூட உடலுக்குள் கொண்டு செல்வதில்லை.
இழைகளின் மதிப்பு, தினசரி ஊட்டச்சத்தின் மிகவும் பெரிய அங்கமாக இருப்பதால், அவை மனித உடலால் செரிக்கப்படுவதில்லை. அதிக அளவு நார்ச்சத்து இருப்பது உணவின் ஒட்டுமொத்த செரிமானத்தை ஓரளவு குறைக்கிறது. இருப்பினும், அதன் முழுமையான இல்லாமை இரைப்பைக் குழாயின் செயல்பாட்டில் ஒரு தீங்கு விளைவிக்கும்.
நார்ச்சத்து குடலின் சரியான பெரிஸ்டால்சிஸை (சுவர்களின் இயக்கம்) ஏற்படுத்துகிறது மற்றும் அதன் மூலம் செரிமான கால்வாய் வழியாக உணவின் இயக்கத்தை ஊக்குவிக்கிறது மற்றும் உடலில் இருந்து செரிக்கப்படாத ஊட்டச்சத்துக்களை அகற்றுகிறது.
தினசரி உணவில் விலங்கு மற்றும் தாவர பொருட்களின் சரியான கலவையால் உணவில் தேவையான அளவு நார்ச்சத்து உறுதி செய்யப்படுகிறது.
முறிவுக்குப் பிறகு, ஃபைபர், மற்ற பாலிசாக்கரைடுகளைப் போலவே, சர்க்கரைகளாக மாறும். இருப்பினும், மனித செரிமான மண்டலத்தில் அத்தகைய முறிவைச் செய்யக்கூடிய நொதிகள் இல்லை. குடலில் உள்ள நுண்ணுயிரிகளின் செல்வாக்கின் கீழ் அதன் ஒரு சிறிய பகுதியை மட்டுமே ஜீரணிக்க முடியும், ஆனால் மாற்றங்கள் இல்லாமல் உடலில் இருந்து மொத்தமாக அகற்றப்படும். இந்த வெளிப்புற பயனற்ற தன்மைக்கு நன்றி, ஃபைபர் மற்றும் பெக்டின்கள் பேலஸ்ட் பொருட்கள் என்று அழைக்கப்படுகின்றன.
பேலாஸ்ட் பொருட்கள் செரிமான செயல்பாட்டில் ஒரு முக்கிய செயல்பாட்டைச் செய்கின்றன: இழைகள் குடல் பாக்டீரியாவால் புளிக்கவைக்கப்படுகின்றன மற்றும் உண்மையில் உணவை அரைக்க உதவுகின்றன; குடல் சுவர்களின் நரம்பு முடிவுகளை எரிச்சலூட்டுவதன் மூலம், அவை பெரிஸ்டால்சிஸை அதிகரிக்கின்றன. பேலஸ்ட் பொருட்களில் உணவு மோசமாக இருந்தால், குடல் இயக்கம் பாதிக்கப்படுகிறது, எனவே, இந்த கோளாறுகளைத் தவிர்க்க, நார்ச்சத்து நிறைந்த கரடுமுரடான உணவுகளைப் பயன்படுத்த பரிந்துரைக்கப்படுகிறது.
கூடுதலாக, உணவு நார்ச்சத்து வளர்சிதை மாற்றத்தைத் தூண்டும் திறனைக் கொண்டுள்ளது, ஏனெனில் நார்ச்சத்து உணவுடன் வரும் அல்லது அதன் செயலாக்கத்தின் போது உருவாகும் நச்சுகளை உறிஞ்சுவதைத் தடுக்கிறது, மேலும் இது ஒரு வகையான துடைப்பமாக செயல்படுகிறது: செரிமான பாதையில் நகர்ந்து, அவை அனைத்தையும் எடுத்துச் செல்கின்றன. சுவர்களில் ஒட்டிக்கொண்டு உடலில் இருந்து நீக்குகிறது.
உணவு நார்ச்சத்தின் மற்றொரு நன்மை என்னவென்றால், இது எண்டோஜெனஸ் கொழுப்பின் அளவைக் குறைக்கும் திறனைக் கொண்டுள்ளது (இது உணவுடன் நமக்குள் நுழையாத கொலஸ்ட்ரால், ஆனால் குடலில் இருந்து கல்லீரலில் நுழையும் பித்த அமிலங்களிலிருந்து கல்லீரலில் உடலால் உற்பத்தி செய்யப்படுகிறது. )
ஹெமிசெல்லுலோஸ்:ஃபைபர், அல்லது செல்லுலோஸ் போன்றவை, தானியப் பொருட்களின் செல் சுவர்களின் ஒரு பகுதியாகும், மேலும் பழங்கள் மற்றும் காய்கறிகளின் கூழில் சிறிய அளவுகள் காணப்படுகின்றன. இது தண்ணீரைத் தக்கவைத்து உலோகங்களை பிணைக்க வல்லது.
கொழுப்பு அமிலங்களின் ஆக்சிஜனேற்றம் (பீட்டா ஆக்சிஜனேற்றம்). பங்கு எச்.எஸ். – கோ இந்த செயல்பாட்டில். ஸ்டீரிக் அமிலத்தின் முழுமையான ஆக்சிஜனேற்றத்தின் ஆற்றல் CO 2 c எச் 2 ஓ . ஆக்சிஜனேற்றத்தின் போது உருவாகும் ஏடிபி மூலக்கூறுகளின் எண்ணிக்கையைக் கணக்கிடுங்கள்.
FA செயல்படுத்தல் சைட்டோபிளாஸில் நிகழ்கிறது, மேலும் பீட்டா-ஆக்சிஜனேற்றம் மைட்டோகாண்ட்ரியாவில் நிகழ்கிறது.
Acyl-CoA மைட்டோகாண்ட்ரியல் சவ்வு வழியாக செல்ல முடியாது. எனவே, "கார்னைடைன்" என்ற பொருளின் பங்கேற்புடன் சைட்டோபிளாஸத்திலிருந்து மைட்டோகாண்ட்ரியனுக்குள் FA களை கொண்டு செல்வதற்கு ஒரு சிறப்பு வழிமுறை உள்ளது. மைட்டோகாண்ட்ரியாவின் உள் மென்படலத்தில் ஒரு சிறப்பு போக்குவரத்து புரதம் உள்ளது, இது பரிமாற்றத்தை உறுதி செய்கிறது. இதற்கு நன்றி, அசில்கார்னிடைன் மைட்டோகாண்ட்ரியல் சவ்வுக்குள் எளிதில் ஊடுருவுகிறது.
சைட்டோபிளாஸ்மிக் மற்றும் மைட்டோகாண்ட்ரியல் கார்னைடைன் அசைல்ட்ரான்ஸ்ஃபெரேஸ்கள் கட்டமைப்பில் வேறுபட்டவை, மேலும் அவை இயக்க பண்புகளிலும் ஒருவருக்கொருவர் வேறுபடுகின்றன. சைட்டோபிளாஸ்மிக் அசைல்கார்னைடைன் டிரான்ஸ்ஃபெரேஸின் Vmax மைட்டோகாண்ட்ரியல் என்சைமின் Vmax ஐ விட குறைவாக உள்ளது, மேலும் β-ஆக்சிஜனேற்ற நொதிகளின் Vmax ஐ விடவும் குறைவாக உள்ளது. எனவே, சைட்டோபிளாஸ்மிக் அசைல்கார்னைடைன் டிரான்ஸ்ஃபெரேஸ் என்பது கொழுப்பு அமிலங்களின் முறிவில் ஒரு முக்கிய நொதியாகும்.
ஒரு கொழுப்பு அமிலம் மைட்டோகாண்ட்ரியாவில் நுழைந்தால், அது அவசியமாக அசிடைல்-CoA க்கு வினையூக்கத்திற்கு உட்படும்.
உடலின் ஆற்றல் தேவைகளை பூர்த்தி செய்யும் மிகவும் கச்சிதமான "எரிபொருள்" கொழுப்பு அமிலங்கள் ஆகும், இது அவற்றின் வேதியியல் கட்டமைப்பின் பண்புகளால் தீர்மானிக்கப்படுகிறது. 1 மோலுக்கு, கொழுப்பு அமிலங்களின் முழுமையான ஆக்சிஜனேற்றம் கார்போஹைட்ரேட்டுகளின் ஆக்சிஜனேற்றத்தை விட பல மடங்கு பயன்படுத்தக்கூடிய இரசாயன ஆற்றலை வெளியிடுகிறது; எடுத்துக்காட்டாக, 1 மோல் பால்மிடிக் அமிலத்தின் ஆக்சிஜனேற்றம் 130 மோல் ஏடிபியை உருவாக்குகிறது, அதே சமயம் 1 மோல் குளுக்கோஸின் ஆக்சிஜனேற்றம் 38 மோல் ஏடிபியை உருவாக்குகிறது. ஒரு யூனிட் எடைக்கு, ஆற்றல் வெளியீடு இரண்டு மடங்குக்கும் அதிகமாக வேறுபடுகிறது (1 கிராம் கொழுப்புக்கு 9 கிலோகலோரி மற்றும் 1 கிராம் கார்போஹைட்ரேட்டுகள் அல்லது புரதங்களுக்கு 4 கிலோகலோரி). இந்த உயர் ஆற்றல் மகசூல், பெட்ரோல், பெட்ரோலியம் மற்றும் பிற பெட்ரோலியப் பொருட்களை வெப்ப மற்றும் இயந்திர ஆற்றலை உருவாக்குவதற்கான பயனுள்ள எரிபொருளாக மாற்றும் அதே காரணத்தை அடிப்படையாகக் கொண்டது, அதாவது நீண்ட அல்கைல் சங்கிலிகளில் அதிக அளவு கார்பன் குறைப்பு. கொழுப்பு அமில மூலக்கூறின் முக்கிய பகுதி மீண்டும் மீண்டும் வரும் அலகுகளைக் கொண்டுள்ளது (CH2)n, அதாவது அதிகபட்சமாக ஹைட்ரஜனில் செறிவூட்டப்பட்ட ஒரு அமைப்பு. முந்தைய விளக்கக்காட்சியில் இருந்து நாம் பார்த்தது போல, உயிரியல் ஆக்ஸிஜனேற்ற செயல்முறைகளின் போது சேமிக்கப்படும் ஆற்றல் முக்கியமாக சுவாச சங்கிலியின் ஹைட்ரஜன் அணுக்களிலிருந்து எலக்ட்ரான்களின் கட்டுப்படுத்தப்பட்ட பரிமாற்றம் தொடர்பாக உருவாகிறது, மேலும் ADP இன் பாஸ்போரிலேஷனுடன் ATP க்கு ஏடிபி. கொழுப்பு அமிலங்கள் முதன்மையாக கார்பன் மற்றும் ஹைட்ரஜனால் ஆனது மற்றும் கார்போஹைட்ரேட்டுகளை விட கணிசமாக குறைவான ஆக்ஸிஜன் அணுக்களைக் கொண்டிருப்பதால், கொழுப்பு அமிலங்களின் ஆக்சிஜனேற்றம் விகிதாசாரத்தில் அதிக ஆக்ஸிஜனை உறிஞ்சுவதோடு, எனவே, ஆக்ஸிஜனேற்ற பாஸ்போரிலேஷனின் போது அதிக ஏடிபி உருவாகிறது.
கொழுப்பு அமிலங்களின் ஆக்சிஜனேற்றம் கல்லீரல், சிறுநீரகங்கள், எலும்பு மற்றும் இதய தசைகள் மற்றும் கொழுப்பு திசுக்களில் மிகவும் தீவிரமாக நிகழ்கிறது என்பது நிறுவப்பட்டுள்ளது. மூளை திசுக்களில், கொழுப்பு அமில ஆக்சிஜனேற்ற விகிதம் மிகவும் குறைவாக உள்ளது, ஏனெனில் மூளை திசுக்களில் ஆற்றலின் முக்கிய ஆதாரம் குளுக்கோஸ் ஆகும்.
β-ஆக்சிஜனேற்றம் என்பது கொழுப்பு அமில வினையூக்கத்தின் ஒரு குறிப்பிட்ட பாதையாகும், இதில் 2 கார்பன் அணுக்கள் அசிடைல்-கோஏ வடிவத்தில் ஒரு கொழுப்பு அமிலத்தின் கார்பாக்சைல் முனையிலிருந்து தொடர்ச்சியாக பிரிக்கப்படுகின்றன. வளர்சிதை மாற்ற பாதை - β-ஆக்சிஜனேற்றம் - கொழுப்பு அமில ஆக்சிஜனேற்ற எதிர்வினைகள் β-கார்பன் அணுவில் ஏற்படுவதால் இவ்வாறு பெயரிடப்பட்டது. TCA சுழற்சியில் β-ஆக்சிஜனேற்றம் மற்றும் அசிடைல்-CoA இன் ஆக்சிஜனேற்றத்தின் எதிர்வினைகள் ஆக்ஸிஜனேற்ற பாஸ்போரிலேஷன் பொறிமுறையின் மூலம் ATP தொகுப்புக்கான முக்கிய ஆற்றல் ஆதாரங்களில் ஒன்றாகச் செயல்படுகின்றன. கொழுப்பு அமிலங்களின் β-ஆக்சிஜனேற்றம் ஏரோபிக் நிலைமைகளின் கீழ் மட்டுமே நிகழ்கிறது.
கொழுப்பு அமிலங்களை செயல்படுத்துதல்
பல்வேறு எதிர்விளைவுகளில் நுழைவதற்கு முன், கொழுப்பு அமிலங்கள் செயல்படுத்தப்பட வேண்டும், அதாவது. கோஎன்சைம் ஏ உடன் மேக்ரோஜெர்ஜிக் பிணைப்பால் இணைக்கப்பட்டுள்ளது:
RCOOH + HSKoA + ATP → RCO ~ CoA + AMP + PPi.
இந்த எதிர்வினை அசைல்-கோஏ சின்தேடேஸ் என்ற நொதியால் வினையூக்கப்படுகிறது. எதிர்வினையின் போது வெளியிடப்படும் பைரோபாஸ்பேட் பைரோபாஸ்பேடேஸ் என்ற நொதியால் ஹைட்ரோலைஸ் செய்யப்படுகிறது: H 4 P 2 O 7 + H 2 O → 2 H 3 PO 4.
பைரோபாஸ்பேட்டின் உயர்-ஆற்றல் பிணைப்பின் நீராற்பகுப்பின் போது ஆற்றலின் வெளியீடு எதிர்வினையின் சமநிலையை வலதுபுறமாக மாற்றுகிறது மற்றும் செயல்படுத்தும் எதிர்வினையின் முழுமையை உறுதி செய்கிறது.
அசைல்-கோஏ சின்தேடேஸ்சைட்டோசோல் மற்றும் மைட்டோகாண்ட்ரியல் மேட்ரிக்ஸ் இரண்டிலும் காணப்படுகின்றன. இந்த நொதிகள் வெவ்வேறு ஹைட்ரோகார்பன் சங்கிலி நீளம் கொண்ட கொழுப்பு அமிலங்களுக்கான தனித்தன்மையில் வேறுபடுகின்றன. குறுகிய மற்றும் நடுத்தர சங்கிலி நீளம் கொண்ட கொழுப்பு அமிலங்கள் (4 முதல் 12 கார்பன் அணுக்கள் வரை) பரவல் மூலம் மைட்டோகாண்ட்ரியல் மேட்ரிக்ஸில் ஊடுருவ முடியும். இந்த கொழுப்பு அமிலங்களின் செயல்பாடு மைட்டோகாண்ட்ரியல் மேட்ரிக்ஸில் நிகழ்கிறது. மனித உடலில் (12 முதல் 20 கார்பன் அணுக்கள்) ஆதிக்கம் செலுத்தும் நீண்ட சங்கிலி கொழுப்பு அமிலங்கள், மைட்டோகாண்ட்ரியாவின் வெளிப்புற மென்படலத்தில் அமைந்துள்ள அசைல்-கோஏ சின்தேடேஸ்களால் செயல்படுத்தப்படுகின்றன.
செயல்படுத்தப்பட்ட கொழுப்பு அமிலங்களின் முறிவு கருதுகோளுக்கு ஏற்ப நிகழ்கிறது b - ஆக்சிஜனேற்றம் F. Knoop, 1904 இல் முன்மொழியப்பட்டது b - மைட்டோகாண்ட்ரியாவிற்குள் ஆக்ஸிஜனேற்றம் ஏற்படுகிறது
β- கொழுப்பு அமில ஆக்சிஜனேற்றம்- கொழுப்பு அமில வினையூக்கத்தின் ஒரு குறிப்பிட்ட பாதை, மைட்டோகாண்ட்ரியல் மேட்ரிக்ஸில் ஏரோபிக் நிலைமைகளின் கீழ் மட்டுமே நிகழ்கிறது மற்றும் அசிடைல்-கோஏ உருவாவதோடு முடிவடைகிறது. β-ஆக்சிஜனேற்ற எதிர்வினைகளிலிருந்து ஹைட்ரஜன் CPE க்குள் நுழைகிறது, மேலும் அசிடைல்-CoA சிட்ரேட் சுழற்சியில் ஆக்ஸிஜனேற்றப்படுகிறது, இது CPE க்கு ஹைட்ரஜனையும் வழங்குகிறது. எனவே, கொழுப்பு அமிலங்களின் β-ஆக்சிஜனேற்றம் என்பது சுவாசச் சங்கிலியில் ATP தொகுப்பை வழங்கும் மிக முக்கியமான வளர்சிதை மாற்றப் பாதையாகும்.
β-ஆக்சிஜனேற்றமானது, எஃப்ஏடி-சார்ந்த அசைல்-கோஏ டீஹைட்ரோஜினேஸால் அசைல்-கோஏவின் டீஹைட்ரஜனேற்றத்துடன் தொடங்குகிறது, இது ஈனாய்ல்-கோஏ என்ற எதிர்வினை தயாரிப்பில் α மற்றும் β கார்பன் அணுக்களுக்கு இடையே இரட்டைப் பிணைப்பை உருவாக்குகிறது. இந்த எதிர்வினையில் மீட்டமைக்கப்பட்ட கோஎன்சைம் FADH 2, CPE இல் உள்ள ஹைட்ரஜன் அணுக்களை கோஎன்சைம் Qக்கு மாற்றுகிறது. இதன் விளைவாக, 2 ATP மூலக்கூறுகள் ஒருங்கிணைக்கப்படுகின்றன (படம் 8-27). பின்வரும் p-ஆக்சிஜனேற்ற எதிர்வினையில், இரட்டைப் பிணைப்பின் இடத்தில் ஒரு நீர் மூலக்கூறு சேர்க்கப்படுகிறது, இதனால் OH குழுவானது அசைலின் β-கார்பன் அணுவில் அமைந்து β-ஹைட்ராக்ஸிசைல்-CoA ஐ உருவாக்குகிறது. β-ஹைட்ராக்ஸிசைல்-CoA பின்னர் NAD+-சார்ந்த டீஹைட்ரோஜினேஸால் ஆக்சிஜனேற்றப்படுகிறது. குறைக்கப்பட்ட NADH, CPE இல் ஆக்ஸிஜனேற்றப்பட்டது, 3 ATP மூலக்கூறுகளின் தொகுப்புக்கான ஆற்றலை வழங்குகிறது. இதன் விளைவாக உருவாகும் β-ketoacyl-CoA ஆனது தியோலேஸ் என்ற நொதியால் தியோலிடிக் பிளவுக்கு உட்படுகிறது, ஏனெனில் C-C பிணைப்பின் பிளவு தளத்தில், கோஎன்சைம் A இன் மூலக்கூறு ஒரு சல்பர் அணு வழியாக சேர்க்கப்படுகிறது. இந்த 4 எதிர்வினைகளின் விளைவாக, ஒரு இரண்டு கார்பன் எச்சம், அசிடைல்-CoA, அசைல்-CoA இலிருந்து பிரிக்கப்படுகிறது. 2 கார்பன் அணுக்களால் சுருக்கப்பட்ட ஒரு கொழுப்பு அமிலம் மீண்டும் டீஹைட்ரஜனேற்றம், நீரேற்றம், டீஹைட்ரஜனேற்றம் மற்றும் அசிடைல்-கோஏவை நீக்குதல் ஆகியவற்றின் எதிர்வினைகளுக்கு உட்படுகிறது. இந்த எதிர்வினைகளின் வரிசை பொதுவாக "β-ஆக்சிஜனேற்ற சுழற்சி" என்று அழைக்கப்படுகிறது, அதாவது அனைத்து அமிலங்களும் அசிடைல் எச்சங்களாக மாற்றப்படும் வரை அதே எதிர்வினைகள் கொழுப்பு அமில தீவிரத்துடன் மீண்டும் மீண்டும் செய்யப்படுகின்றன.
β - கொழுப்பு அமிலங்களின் ஆக்சிஜனேற்றம்.
பி-ஆக்சிஜனேற்ற செயல்முறை சுழற்சியானது.சுழற்சியின் ஒவ்வொரு சுழற்சிக்கும், 2 கார்பன் அணுக்கள் கொழுப்பு அமிலத்திலிருந்து அசிடைல் எச்ச வடிவில் பிரிக்கப்படுகின்றன.
இதற்குப் பிறகு, 2 கார்பன் அணுக்களால் சுருக்கப்பட்ட அசைல்-கோஏ மீண்டும் ஆக்சிஜனேற்றத்திற்கு உட்படுகிறது (பி-ஆக்சிஜனேற்ற எதிர்வினைகளின் புதிய சுழற்சியில் நுழைகிறது). இதன் விளைவாக வரும் அசிடைல்-கோஏ மேலும் ட்ரைகார்பாக்சிலிக் அமில சுழற்சியில் நுழைய முடியும்.கொழுப்பு அமிலங்களின் முறிவின் ஆற்றல் விளைச்சலை நீங்கள் கணக்கிட வேண்டும். n கார்பன் அணுக்களைக் கொண்ட எந்த நிறைவுற்ற கொழுப்பு அமிலத்திற்கும் வழங்கப்பட்ட சூத்திரம் உண்மையாகும். நிறைவுறா கொழுப்பு அமிலங்களின் முறிவு குறைந்த ATP ஐ உருவாக்குகிறது. ஒரு கொழுப்பு அமிலத்தில் உள்ள ஒவ்வொரு இரட்டைப் பிணைப்பும் 2 ஏடிபி மூலக்கூறுகளின் இழப்பைக் குறிக்கிறது. பி-ஆக்சிஜனேற்றம் தசை திசு, சிறுநீரகம் மற்றும் கல்லீரலில் மிகவும் தீவிரமாக நிகழ்கிறது. FA இன் b-ஆக்சிஜனேற்றத்தின் விளைவாக, அசிடைல்-CoA உருவாகிறது. ஆக்ஸிஜனேற்ற விகிதம் லிபோலிசிஸ் செயல்முறைகளின் விகிதத்தால் தீர்மானிக்கப்படுகிறது. லிபோலிசிஸின் முடுக்கம் என்பது கார்போஹைட்ரேட் பட்டினி மற்றும் தீவிர தசை வேலை ஆகியவற்றின் சிறப்பியல்பு ஆகும். பி-ஆக்சிஜனேற்றத்தின் முடுக்கம் கல்லீரல் உட்பட பல திசுக்களில் காணப்படுகிறது. கல்லீரல் தேவைக்கு அதிகமாக அசிடைல்-கோஏவை உற்பத்தி செய்கிறது. கல்லீரல் ஒரு "பரோபகார உறுப்பு" எனவே கல்லீரல் மற்ற திசுக்களுக்கு குளுக்கோஸை அனுப்புகிறது.
கல்லீரல் அதன் சொந்த அசிடைல்-கோஏவை மற்ற திசுக்களுக்கு அனுப்ப முயற்சிக்கிறது, ஆனால் உயிரணு சவ்வுகள் அசிடைல்-கோஏவுக்கு ஊடுருவ முடியாதவை என்பதால் முடியாது. எனவே, "கீட்டோன் உடல்கள்" என்று அழைக்கப்படும் சிறப்பு பொருட்கள் அசிடைல்-கோஏவிலிருந்து கல்லீரலில் ஒருங்கிணைக்கப்படுகின்றன. கீட்டோன் உடல்கள் அசிடைல்-கோஏவின் சிறப்பு போக்குவரத்து வடிவமாகும்.
அசிடைல் கோஎன்சைம் ஏ (அசிடைல்-கோஏ) வடிவத்தில் இரண்டு கார்பன் துண்டுகளை படிப்படியாக நீக்குவதன் மூலம் கொழுப்பு அமில மூலக்கூறு மைட்டோகாண்ட்ரியாவாக உடைக்கப்படுகிறது.
C17H35COOH + 26 O2 = 18 CO2 + 18 H2O.
ஸ்டீரிக் அமிலம் ஆக்ஸிஜனேற்றப்படும்போது, செல் 146 ஏடிபி மூலக்கூறுகளைப் பெறும்.
கொழுப்பு அமிலங்களில் உள்ள ஆற்றலை ஏடிபி பிணைப்புகளின் ஆற்றலாக மாற்ற, கொழுப்பு அமிலங்களின் ஆக்சிஜனேற்றம் CO 2 மற்றும் தண்ணீருக்கு வளர்சிதை மாற்ற பாதை உள்ளது, இது ட்ரைகார்பாக்சிலிக் அமில சுழற்சி மற்றும் சுவாச சங்கிலியுடன் நெருக்கமாக தொடர்புடையது. இந்த பாதை அழைக்கப்படுகிறது β-ஆக்சிஜனேற்றம், ஏனெனில் கொழுப்பு அமிலத்தின் (β-நிலை) 3 வது கார்பன் அணுவை கார்பாக்சைல் குழுவாக ஆக்சிஜனேற்றம் செய்யப்படுகிறது, அதே நேரத்தில் அசல் கொழுப்பு அமிலத்தின் C 1 மற்றும் C 2 உட்பட அசிடைல் குழு அமிலத்திலிருந்து பிளவுபடுகிறது.
β-ஆக்சிஜனேற்றத்தின் அடிப்படை வரைபடம்
β-ஆக்சிஜனேற்ற எதிர்வினைகள் ஏற்படுகின்றன மைட்டோகாண்ட்ரியாஉடலில் உள்ள பெரும்பாலான செல்கள் (நரம்பு செல்கள் தவிர). இரத்தத்தில் இருந்து சைட்டோசோலில் நுழையும் கொழுப்பு அமிலங்கள் அல்லது அவற்றின் சொந்த செல்லுலார் TAGகளின் லிபோலிசிஸின் போது தோன்றும் ஆக்சிஜனேற்றத்திற்குப் பயன்படுத்தப்படுகின்றன. பால்மிடிக் அமிலத்தின் ஆக்சிஜனேற்றத்திற்கான ஒட்டுமொத்த சமன்பாடு பின்வருமாறு:
Palmitoyl-ScoA + 7FAD + 7NAD + + 7H 2 O + 7HS-KoA → 8Acetyl-ScoA + 7FADH 2 + 7NADH
கொழுப்பு அமில ஆக்சிஜனேற்றத்தின் நிலைகள்
1. மைட்டோகாண்ட்ரியல் மேட்ரிக்ஸில் ஊடுருவி ஆக்ஸிஜனேற்றத்திற்கு முன், கொழுப்பு அமிலம் அவசியம் செயல்படுத்தசைட்டோசோலில். acyl-ScoA ஐ உருவாக்குவதற்கு கோஎன்சைம் A ஐ சேர்ப்பதன் மூலம் இது நிறைவேற்றப்படுகிறது. Acyl-ScoA ஒரு உயர் ஆற்றல் கலவை ஆகும். பாஸ்போரிக் அமிலத்தின் இரண்டு மூலக்கூறுகளாக டைபாஸ்பேட்டை நீராற்பகுப்பு செய்வதன் மூலம் எதிர்வினையின் மீளமுடியாத தன்மை அடையப்படுகிறது.
Acyl-ScoA சின்தேடேஸ்கள் எண்டோபிளாஸ்மிக் ரெட்டிகுலத்தில், மைட்டோகாண்ட்ரியாவின் வெளிப்புற சவ்வு மற்றும் அவற்றுள் காணப்படுகின்றன. வெவ்வேறு கொழுப்பு அமிலங்களுக்கு குறிப்பிட்ட பலவிதமான சின்தேடேஸ்கள் உள்ளன.
கொழுப்பு அமிலம் செயல்படுத்தும் எதிர்வினை
2. Acyl-ScoA மைட்டோகாண்ட்ரியல் சவ்வு வழியாக செல்ல முடியாது, எனவே அதை வைட்டமின் போன்ற பொருள் கார்னைடைனுடன் இணைந்து கொண்டு செல்ல ஒரு வழி உள்ளது. மைட்டோகாண்ட்ரியாவின் வெளிப்புற மென்படலத்தில் ஒரு நொதி உள்ளது கார்னைடைன் அசைல்ட்ரான்ஸ்ஃபெரேஸ் I.

மைட்டோகாண்ட்ரியனுக்குள் கொழுப்பு அமிலங்களின் கார்னைடைன் சார்ந்த போக்குவரத்து
கார்னைடைன் கல்லீரல் மற்றும் சிறுநீரகங்களில் தொகுக்கப்பட்டு பின்னர் மற்ற உறுப்புகளுக்கு கொண்டு செல்லப்படுகிறது. இல் கருப்பைக்குள்காலம் மற்றும் உள்ளே ஆரம்ப ஆண்டுகளில்வாழ்க்கையில், உடலுக்கு கார்னைடைனின் முக்கியத்துவம் மிகவும் பெரியது. நரம்பு மண்டலத்திற்கு ஆற்றல் வழங்கல் குழந்தைகள்உடல் மற்றும், குறிப்பாக, மூளை இரண்டு இணையான செயல்முறைகளால் மேற்கொள்ளப்படுகிறது: கொழுப்பு அமிலங்களின் கார்னைடைன் சார்ந்த ஆக்சிஜனேற்றம் மற்றும் குளுக்கோஸின் ஏரோபிக் ஆக்சிஜனேற்றம். மூளை மற்றும் முள்ளந்தண்டு வடத்தின் வளர்ச்சிக்கு, இயக்கம் மற்றும் தசை தொடர்புக்கு பொறுப்பான நரம்பு மண்டலத்தின் அனைத்து பகுதிகளின் தொடர்புக்கும் கார்னைடைன் அவசியம். கார்னைடைன் குறைபாட்டை இணைக்கும் ஆய்வுகள் உள்ளன பெருமூளை வாதம்மற்றும் நிகழ்வு" தொட்டிலில் மரணம்".
இளம் குழந்தைகள், முன்கூட்டிய குழந்தைகள் மற்றும் குறைந்த எடை கொண்ட குழந்தைகள் கார்னைடைன் குறைபாட்டிற்கு குறிப்பாக உணர்திறன் உடையவர்கள். பல்வேறு மன அழுத்த சூழ்நிலைகளில் (தொற்று நோய்கள், இரைப்பை குடல் கோளாறுகள், உணவு சீர்குலைவுகள்) அவற்றின் எண்டோஜெனஸ் இருப்புக்கள் விரைவாக குறைக்கப்படுகின்றன. குறைந்த தசை வெகுஜனத்தின் காரணமாக கார்னைடைன் உயிரியக்கவியல் கூர்மையாக மட்டுப்படுத்தப்படுகிறது, மேலும் வழக்கமான உணவுகளில் இருந்து உட்கொள்ளும் இரத்தம் மற்றும் திசுக்களில் போதுமான அளவுகளை பராமரிக்க முடியவில்லை.
3. கார்னைடைனுடன் பிணைக்கப்பட்ட பிறகு, கொழுப்பு அமிலம் டிரான்ஸ்லோகேஸ் மூலம் சவ்வு முழுவதும் கொண்டு செல்லப்படுகிறது. இங்கே, மென்படலத்தின் உள் பக்கத்தில், கார்னைடைன் அசைல்ட்ரான்ஸ்ஃபெரேஸ் II என்சைம் மீண்டும் அசைல்-எஸ்சிஓஏவை உருவாக்குகிறது, இது β-ஆக்சிஜனேற்ற பாதையில் நுழைகிறது.
4. செயல்முறை தன்னை β-ஆக்சிஜனேற்றம்சுழற்சி முறையில் மீண்டும் மீண்டும் 4 எதிர்வினைகளைக் கொண்டுள்ளது. அவை வரிசையாக நடக்கும் ஆக்சிஜனேற்றம்(அசில்-எஸ்சிஓஏ டீஹைட்ரஜனேஸ்), நீரேற்றம்(enoyl-ScoA hydratase) மற்றும் மீண்டும் ஆக்சிஜனேற்றம் 3வது கார்பன் அணு (ஹைட்ராக்ஸிசைல்-எஸ்சிஓஏ டிஹைட்ரோஜினேஸ்). கடைசி, பரிமாற்ற எதிர்வினையில், அசிடைல்-எஸ்சிஓஏ கொழுப்பு அமிலத்திலிருந்து பிரிக்கப்படுகிறது. HS-CoA மீதமுள்ள (இரண்டு கார்பன்களால் சுருக்கப்பட்டது) கொழுப்பு அமிலத்துடன் சேர்க்கப்படுகிறது, மேலும் அது முதல் எதிர்வினைக்குத் திரும்புகிறது. கடைசி சுழற்சி இரண்டு அசிடைல்-எஸ்சிஓஏக்களை உருவாக்கும் வரை இது மீண்டும் மீண்டும் செய்யப்படுகிறது.

கொழுப்பு அமிலங்களின் β- ஆக்சிஜனேற்றத்தின் எதிர்வினைகளின் வரிசை
β-ஆக்சிஜனேற்றத்தின் ஆற்றல் சமநிலையின் கணக்கீடு
முன்னதாக, ஆக்சிஜனேற்றத் திறனைக் கணக்கிடும் போது, NADHக்கான P/O குணகம் FADH 2 - 2.0க்கு 3.0க்கு சமமாக எடுக்கப்பட்டது.
நவீன தரவுகளின்படி, NADH க்கான P/O குணகத்தின் மதிப்பு FADH 2 - 1.5 க்கு 2.5 க்கு ஒத்திருக்கிறது.
கொழுப்பு அமிலங்களின் β- ஆக்சிஜனேற்றத்தின் போது உருவாகும் ஏடிபியின் அளவைக் கணக்கிடும்போது, கணக்கில் எடுத்துக்கொள்ள வேண்டியது அவசியம்:
- கொழுப்பு அமிலத்தில் உள்ள கார்பன் அணுக்களின் எண்ணிக்கையை 2 ஆல் வழக்கமான பிரிப்பதன் மூலம் உருவாக்கப்பட்ட அசிடைல்-எஸ்சிஓஏ அளவு தீர்மானிக்கப்படுகிறது.
- எண் β-ஆக்சிஜனேற்ற சுழற்சிகள். இரண்டு கார்பன் அலகுகளின் சங்கிலியாக கொழுப்பு அமிலத்தின் கருத்தின் அடிப்படையில் β- ஆக்சிஜனேற்ற சுழற்சிகளின் எண்ணிக்கை தீர்மானிக்க எளிதானது. அலகுகளுக்கு இடையிலான இடைவெளிகளின் எண்ணிக்கை β- ஆக்சிஜனேற்ற சுழற்சிகளின் எண்ணிக்கையுடன் ஒத்துள்ளது. அதே மதிப்பை சூத்திரத்தைப் பயன்படுத்தி கணக்கிடலாம் (n/2 -1), இங்கு n என்பது அமிலத்தில் உள்ள கார்பன் அணுக்களின் எண்ணிக்கை.
- ஒரு கொழுப்பு அமிலத்தில் இரட்டைப் பிணைப்புகளின் எண்ணிக்கை. முதல் β-ஆக்சிஜனேற்ற எதிர்வினையில், FAD இன் பங்கேற்புடன் இரட்டைப் பிணைப்பு உருவாகிறது. கொழுப்பு அமிலத்தில் ஏற்கனவே இரட்டைப் பிணைப்பு இருந்தால், இந்த எதிர்வினை தேவையில்லை மற்றும் FADN 2 உருவாகாது. இழந்த FADN 2 இன் எண்ணிக்கை இரட்டைப் பிணைப்புகளின் எண்ணிக்கையுடன் ஒத்துள்ளது. சுழற்சியின் மீதமுள்ள எதிர்வினைகள் மாற்றங்கள் இல்லாமல் தொடர்கின்றன.
- செயல்படுத்துவதில் செலவழிக்கப்பட்ட ATP ஆற்றலின் அளவு (எப்போதும் இரண்டு உயர் ஆற்றல் பிணைப்புகளுக்கு ஒத்திருக்கும்).
உதாரணமாக. பால்மிடிக் அமிலத்தின் ஆக்சிஜனேற்றம்
- 16 கார்பன் அணுக்கள் இருப்பதால், β-ஆக்சிஜனேற்றம் ஏற்படுகிறது 8 அசிடைல்-எஸ்சிஓஏ மூலக்கூறுகள். பிந்தையது TCA சுழற்சியில் நுழைகிறது; சுழற்சியின் ஒரு திருப்பத்தில் இது ஆக்ஸிஜனேற்றப்படும்போது, NADH இன் 3 மூலக்கூறுகள் (7.5 ATP), FADH 2 இன் 1 மூலக்கூறு (1.5 ATP) மற்றும் 1 GTP மூலக்கூறு உருவாகின்றன, இது 10 மூலக்கூறுகளுக்கு சமமானதாகும். ATP இன். எனவே, அசிடைல்-எஸ்சிஓஏவின் 8 மூலக்கூறுகள் 8 × 10 = உருவாக்கத்தை வழங்கும். 80 ஏடிபி மூலக்கூறுகள்.
- பால்மிடிக் அமிலத்திற்கு β-ஆக்சிஜனேற்ற சுழற்சிகளின் எண்ணிக்கை 7 ஆகும். ஒவ்வொரு சுழற்சியிலும், FADH 2 (1.5 ATP) இன் 1 மூலக்கூறும் NADH இன் 1 மூலக்கூறும் (2.5 ATP) உற்பத்தி செய்யப்படுகின்றன. சுவாச சங்கிலியில் நுழைந்து, மொத்தத்தில் அவை 4 ஏடிபி மூலக்கூறுகளை "கொடுக்கின்றன". இவ்வாறு, 7 சுழற்சிகளில் 7 × 4 = 28 ATP மூலக்கூறுகள் உருவாகின்றன.
- பால்மிடிக் அமிலத்தில் இரட்டைப் பிணைப்புகள் இல்லை.
- கொழுப்பு அமிலத்தை செயல்படுத்த ATP இன் 1 மூலக்கூறு பயன்படுத்தப்படுகிறது, இருப்பினும், AMP ஆக ஹைட்ரோலைஸ் செய்யப்படுகிறது, அதாவது, அது செலவழிக்கப்படுகிறது. 2 மேக்ரோர்ஜிக் இணைப்புகள்அல்லது இரண்டு ஏடிபி.
இவ்வாறு, சுருக்கமாக, நாம் பெறுகிறோம் 80+28-2 =106 பால்மிடிக் அமிலத்தின் ஆக்சிஜனேற்றத்தின் போது ஏடிபி மூலக்கூறுகள் உருவாகின்றன.
- செங்குத்து அச்சைச் சுற்றி கப்பலின் சீரான சுழற்சி
- சிப்லென்கோவ், டெனிஸ் இவனோவிச், டி சிப்லென்கோவிடமிருந்து ஆயுதங்களை உயர்த்துவதற்கான ரகசியங்கள்
- பதப்படுத்தப்பட்ட சீஸ் பிறந்த நாடு எது?
- ஸ்னிக்கர்ஸ் பட்டையின் எடை எவ்வளவு?
- ஓட்கா எத்தனை டிகிரி இருக்க வேண்டும்?
- பாஸ்தாவை சமைக்கும் வகைகள், நேரங்கள் மற்றும் முறைகள்
- உங்கள் ஆரோக்கியத்திற்கான கடல் உணவு
- வான்கோழி ஃபில்லட்டை எவ்வளவு நேரம் சமைக்க வேண்டும்?
- குழம்பு கொண்டு மாட்டிறைச்சி goulash மாட்டிறைச்சி goulash குண்டு எப்படி
- அடுப்பில் வீட்டில் ஒரு கப்கேக் சுட்டுக்கொள்ள - ஒரு எளிய செய்முறை
- கோழி கல்லீரல் கபாப்பிற்கான சரியான கோழி கல்லீரல் இறைச்சியை தயாரிப்பதற்கான ஐந்து விதிகள்
- ஒரு ரெப் அதிகபட்சம் (1ஆர்எம்) ஒரு ரெப் அதிகபட்சத்தை தீர்மானிக்கவும்
- சம எண்ணிக்கையிலான கார்பன் அணுக்கள் கொண்ட நிறைவுற்ற கொழுப்பு அமிலங்களின் ஆக்சிஜனேற்றத்தின் ஆற்றல் சமநிலை
- பயன்படுத்தப்பட்ட இலக்கியங்களின் பட்டியல் தசை செயல்பாட்டின் உயிர்வேதியியல்
- தசை செயல்பாட்டின் உயிர்வேதியியல்
- கோஜி பெர்ரி: நன்மைகள், தீங்கு, எப்படி எடுத்துக்கொள்வது
- சேரி முதல் விளையாட்டு வரை! செர்ஜி மிரோனோவ். தடகள வீரர் செர்ஜி மிரோனோவ் (உடலமைப்பு): சுயசரிதை, அளவுருக்கள், தொழில் செர்ஜி மிரோனோவ் உடற்பயிற்சி மாதிரி சுயசரிதை
- வீடியோ விமர்சனம்! மிகைல் ப்ரிகுனோவ். மைக்கேல் ப்ரிகுனோவ் உடனான நேர்காணல் தடகளத்தில் நீங்கள் என்ன துறையை செய்தீர்கள்?
- அதிகபட்ச ஆக்ஸிஜன் நுகர்வு தீர்மானித்தல்
- தூரத்தில் பந்து வீசுதல்