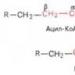
أكسدة حمض البالمتيك. توازن الطاقة لأكسدة الأحماض الدهنية المشبعة مع عدد زوجي من ذرات الكربون. كيفية زيادة كمية الأحماض الدهنية في نظامك الغذائي
100 روبيةمكافأة للطلب الأول
حدد نوع العمل عمل الدبلوم عمل الدورة ملخص أطروحة الماجستير تقرير الممارسة تقرير المقال مراجعة العمل الاختباري دراسة حل المشكلات خطة العمل إجابات على الأسئلة العمل الإبداعي مقال الرسم المقالات ترجمة العروض التقديمية الكتابة أخرى زيادة تفرد النص أطروحة الماجستير العمل المختبري المساعدة عبر الإنترنت
تعرف على السعر
الأحماض الدهنية هي أحماض كربوكسيلية عالية مشبعة وغير مشبعة، وتحتوي السلسلة الهيدروكربونية منها على أكثر من 12 ذرة كربون. تعد أكسدة الأحماض الدهنية في الجسم عملية مهمة للغاية، ويمكن توجيهها إلى ذرات الكربون α و β و ω في جزيئات حمض الكربوكسيل. ومن بين هذه العمليات، تحدث أكسدة بيتا في أغلب الأحيان. لقد ثبت أن أكسدة الأحماض الدهنية تحدث في الكبد والكلى والعضلات الهيكلية والقلبية وفي الأنسجة الدهنية. في أنسجة المخ، يكون معدل أكسدة الأحماض الدهنية منخفضًا جدًا؛ المصدر الرئيسي للطاقة في أنسجة المخ هو الجلوكوز.
في عام 1904، طرح ف. نوب فرضية أكسدة الأحماض الدهنية β بناءً على تجارب في تغذية الكلاب بأحماض دهنية مختلفة حيث تم استبدال ذرة هيدروجين واحدة في مجموعة الميثيل الطرفية (ذرة الكربون ω) بجذر (C6H5– ).
تحتوي الأحماض الدهنية، وهي جزء من الدهون الطبيعية للحيوانات والنباتات، على عدد زوجي من ذرات الكربون. أي حمض يتم إزالة زوج من ذرات الكربون منه يمر في النهاية عبر مرحلة حمض البيوتريك. بعد أكسدة بيتا أخرى، يصبح حمض البيوتيريك حمض أسيتو أسيتيك. ثم يتم تحلل الأخير إلى جزيئين من حمض الأسيتيك. كانت نظرية أكسدة الأحماض الدهنية، التي اقترحها ف. نوب، بمثابة الأساس للأفكار الحديثة حول آلية أكسدة الأحماض الدهنية.
β- أكسدة الأحماض الدهنية. تخضع الأحماض الكربوكسيلية المتكونة أثناء التحلل المائي للدهون إلى أكسدة β في الميتوكوندريا، حيث تدخل في شكل أنزيمات الأسيل المقابلة A. β-Oxidation هي 4 ORPs متتالية.
أنا رد فعل. نزع الهيدروجين
// ديهيدروجينيز /
C15H31 – CH2 – CH2 – C + FAD C = C + FAD(2H)
سكوا ح كوسكوا
أنزيم ستيريل A هو أيزومر متحول لأنزيم ستيريل A
رد الفعل الثاني الترطيب
/ هيدراتاز //
C = C + H2O C15H31 – CH – CH2 – C
H COSCoA OH SCoA
أيزومر ترانس لأنزيم ستيريل A أيزومر L لحمض بيتا هيدروكسي كربوكسيل
رد الفعل الثالث نزع الهيدروجين
// ديهيدروجينيز //
C15H31 – CH – CH2 – C + NAD+ C15H31 – C – CH2 – C + NADH + H+
يا سكوا يا سكوا
حمض بيتا أوكسو
رد الفعل الرابع. ينقسم
// ثيوليز // //
C15H31 – C – CH2 – C + HSCoA C15H31 – C CH3 – C
حول SCoA SCoA SCoA
بالميتوكوإنزيم أ، أسيتيل أنزيم أ
حول الجديد في دورة كريبس لـ
β-أكسدة النهائي
أكسدة
إلى ثاني أكسيد الكربون وH2O
تمثل التفاعلات الأربعة لعملية الأكسدة β التي تم النظر فيها دورة يتم خلالها تقصير سلسلة الكربون بواسطة ذرتين كربون. يخضع الإنزيم المساعد بالميتو A لأكسدة بيتا مرة أخرى، ويكرر هذه الدورة. أثناء أكسدة β لجزيء واحد من حمض دهني، يتم تشكيل 40 جزيء ATP، بما في ذلك دورة كريبس، التي تؤكسد جزيئات أنزيم الأسيتيل A - 146 ATP الناتجة. وهذا يدل على أهمية عمليات أكسدة الأحماض الدهنية من حيث طاقة الجسم.
α- أكسدة الأحماض الدهنية.في النباتات، تحت تأثير الإنزيمات، تتأكسد الأحماض الدهنية في ذرة الكربون ألفا - أكسدة ألفا. هذه دورة تتكون من تفاعلين.
أنا رد فعل يتكون من أكسدة حمض دهني مع بيروكسيد الهيدروجين بمشاركة البيروكسيديز المقابل في الألدهيد وثاني أكسيد الكربون المقابل.
البيروكسيديز //
R – CH2 – COOH + 2 H2O2 R – C + CO2
ونتيجة لهذا التفاعل، يتم تقصير سلسلة الكربون بمقدار ذرة كربون واحدة.
رد الفعل الثاني يتكون من ترطيب وأكسدة الألدهيد الناتج إلى حمض الكربوكسيل المقابل تحت تأثير هيدروجيناز الألدهيد مع الشكل المؤكسد لـ NAD+:
// ألدهيد- //
R – C + H2O + NAD+ ديهيدروجينيز R – C + NAD(H) + H+
دورة الأكسدة α مميزة فقط للنباتات.
ω- أكسدة الأحماض الدهنية.يوجد في كبد الحيوانات وبعض الكائنات الحية الدقيقة نظام إنزيم يوفر الأكسدة، أي. الأكسدة في مجموعة CH3 الطرفية. أولاً، تحت تأثير أحادي الأكسجيناز، تحدث عملية الهيدروكسيل لتكوين حمض ω-هيدروكسي:
ω أحادي الأكسجين
CH3 – R – COOH + “O” HOCH2 – R – COOH
HOCH2 – R – COOH + H2O + 2NAD+ ديهيدروجيناز HOOC– R – COOH + 2 NAD (H) + 2H+
ω-حمض ثنائي الكربوكسيل
يتم تقصير حمض ω-ثنائي الكربوكسيل الناتج عند كلا الطرفين بواسطة تفاعل أكسدة β.
إذا كان للحمض الكربوكسيلي فروع، فإن أكسدته البيولوجية تتوقف عندما يصل إلى نقطة التفرع التسلسلي.
تتكون عملية أكسدة الأحماض الدهنية من المراحل الرئيسية التالية.
تفعيل الأحماض الدهنية. الأحماض الدهنية الحرة، بغض النظر عن طول السلسلة الهيدروكربونية، خاملة من الناحية الأيضية ولا يمكن أن تخضع لأي تحولات كيميائية حيوية، بما في ذلك الأكسدة، حتى يتم تنشيطها. يحدث تنشيط الأحماض الدهنية على السطح الخارجي لغشاء الميتوكوندريا بمشاركة ATP والإنزيم المساعد A (HS-KoA) وأيونات Mg 2+. يتم تحفيز التفاعل بواسطة إنزيم إنزيم أسيل-CoA:
ونتيجة للتفاعل، يتم تشكيل أسيل مرافق الإنزيم أ، وهو الشكل النشط للحمض الدهني.
المرحلة الأولى من نزع الهيدروجين. يخضع Acyl-CoA في الميتوكوندريا أولاً لعملية نزع الهيدروجين الأنزيمية، ويفقد Acyl-CoA ذرتين هيدروجين في الموضعين α و β، ويتحول إلى إستر CoA للحمض غير المشبع.

مرحلة الترطيب. أسيل CoA غير المشبع (enoyl-CoA)، بمشاركة إنزيم enoyl-CoA hydratase، يربط جزيء الماء. ونتيجة لذلك، يتم تشكيل β-هيدروكسي أسيل-CoA (أو 3-هيدروكسي أسيل-CoA):

المرحلة الثانية من نزع الهيدروجين. يتم بعد ذلك نزع الهيدروجين من β-hydroxyacyl-CoA (3-hydroxyacyl-CoA) الناتج. يتم تحفيز هذا التفاعل بواسطة نازعات الهيدروجين المعتمدة على NAD+:

تفاعل الثيوليز. هو انقسام 3-oxoacyl-CoA بواسطة مجموعة الثيول في جزيء CoA الثاني. ونتيجة لذلك، يتم تشكيل أسيل CoA الذي تم اختصاره بواسطة ذرتي كربون وجزء ثنائي الكربون على شكل أسيتيل CoA. يتم تحفيز هذا التفاعل بواسطة أسيتيل CoA acyltransferase (β-ketothiolase):

يخضع الأسيتيل CoA الناتج للأكسدة في دورة حمض ثلاثي الكربوكسيل، ويمر أسيل CoA، الذي تم اختصاره بواسطة ذرتي كربون، مرة أخرى بشكل متكرر عبر مسار الأكسدة β بأكمله حتى تكوين بيوتيريل CoA (مركب رباعي الكربون)، والذي في يتأكسد بدوره ما يصل إلى جزيئين من أسيتيل CoA.
توازن الطاقة. تنتج كل دورة من أكسدة β جزيءًا واحدًا من FADH 2 وجزيءًا واحدًا من NADH. الأخير، في عملية الأكسدة في السلسلة التنفسية وما يرتبط بها من الفسفرة، يعطي: FADH 2 - 2 جزيئات ATP وNADH - 3 جزيئات ATP، أي. في المجموع، يتم تشكيل 5 جزيئات ATP في دورة واحدة. تنتج أكسدة حمض البالمتيك 5 × 7 = 35 جزيء ATP. في عملية أكسدة حمض البالمتيك β، يتم تكوين 8 جزيئات من أسيتيل CoA، كل منها، "يحترق" في دورة حمض ثلاثي الكربوكسيل، يعطي 12 جزيء ATP، و 8 جزيئات من أسيتيل CoA تعطي 12 × 8 = 96 جزيء من ATP.
وهكذا، في المجموع، مع الأكسدة الكاملة لحمض البالمتيك، يتم تشكيل 35 + 96 = 131 جزيء ATP. مع الأخذ في الاعتبار جزيء ATP واحد تم إنفاقه في البداية على تكوين الشكل النشط لحمض البالمتيك (palmitoyl-CoA)، فإن إجمالي إنتاج الطاقة للأكسدة الكاملة لجزيء واحد من حمض البالمتيك في الظروف الحيوانية سيكون 131 – 1 = 130 جزيئات ATP.
التحلل المائي الدهون الثلاثية يتم تنفيذها بواسطة الليباز البنكرياسي. درجة الحموضة المثالية له = 8، فهو يتحلل TG بشكل رئيسي في الموضعين 1 و3، مع تكوين 2 من الأحماض الدهنية الحرة و2-أحادي الجلسرين (2-MG). 2-MG مستحلب جيد . يتم تحويل 28% من 2-MG إلى 1-MG بواسطة الأيزوميراز. يتم تحلل معظم الـ 1-MG بواسطة الليباز البنكرياسي إلى جلسرين وحمض دهني، وفي البنكرياس يتم تصنيع الليباز البنكرياسي مع بروتين كوليباز. يتشكل الكوليباز بشكل غير نشط ويتم تنشيطه في الأمعاء عن طريق التربسين من خلال التحلل الجزئي للبروتينات. يرتبط كوليباز، بمجاله الكاره للماء، بسطح قطرة الدهون، ويساعد مجاله المحب للماء على تقريب المركز النشط لليباز البنكرياسي قدر الإمكان من TG، مما يسرع التحلل المائي.
|
الأنسجة الدهنية البنية |
|
|
كمية |
قليل عند البالغين، مرتفع عند الأطفال حديثي الولادة |
|
الموقع |
بشكله النقي: بالقرب من الكلى والغدة الدرقية. الأنسجة الدهنية المختلطة: بين لوحي الكتف، على الصدر والكتفين. |
|
إمدادات الدم |
جيد جدًا |
|
هيكل الخلايا الشحمية |
هناك العديد من قطرات الدهون الصغيرة في السيتوبلازم، وتقع النواة والعضيات في وسط الخلية، وهناك العديد من الميتوكوندريا والسيتوكرومات. |
|
توليد الحرارة |
|
تحدث الأكسدة في مصفوفة الميتوكوندريا. أولا يتم تنشيط الأحماض الدهنية: 1 .في السيتوبلازم يتم تنشيط كل حمض باستخدام طاقة CoA-8H وATP. 2. يتم نقل الحمض الدهني النشط، acyl-CoA، من العصارة الخلوية إلى مصفوفة الميتوكوندريا (MC). يبقى CoA-8H في العصارة الخلوية، ويتم دمج بقايا الأحماض الدهنية - الأسيل - مع الكارنيتين (من اللاتينية - كارنيتين - لحم - يتم عزل الكارنيتين من الأنسجة العضلية) لتكوين أسيل كارنيتين، الذي يدخل الفضاء بين الغشائي للميتوكوندريا. من الفضاء بين الغشائي للميتوكوندريا، يتم نقل مركب الأسيل كارنيتين إلى مصفوفة الميتوكوندريا. في هذه الحالة، يبقى الكارنيتين في الفضاء بين الغشاء. في المصفوفة، يتحد الأسيل مع CoA-8H. 3. أكسدة. يتم تكوين حمض دهني نشط في مصفوفة MC، والتي تخضع لاحقًا لتفاعلات الأكسدة للمنتجات النهائية. في أكسدة بيتا، تتم أكسدة مجموعة CH2- الموجودة في موضع بيتا للحمض الدهني إلى المجموعة C. في هذه الحالة، يحدث نزع الهيدروجين على مرحلتين: بمشاركة أسيل ديهيدروجينيز (إنزيم الفلافين، يتم نقل الهيدروجين إلى يوبيكوينون) وبيتا هيدروكسي أسيل ديهيدروجينيز (مستقبل الهيدروجين NAD+). بعد ذلك، يتحلل بيتا-كيتواسيل-CoA، تحت تأثير إنزيم ثيوليز، إلى أسيتيل CoA وأسيل-CoA، ويتم اختصارهما بذرتي كربون مقارنة بالأصل. يخضع أسيل CoA مرة أخرى لأكسدة بيتا. يؤدي التكرار المتكرر لهذه العملية إلى انهيار كامل للحمض الدهني إلى أسيل مرافق الإنزيم أ. أكسدة الأحماض الدهنية. يتضمن مرحلتين: 1. الانقسام المتسلسل لجزء ثنائي الكربون على شكل أسيتيل CoA من الطرف C للحمض؛ 2. أكسدة الأسيتيل CoA في دورة كريبس إلى CO2 و H2O. قيمة الطاقة لأكسدة الأحماض الدهنية. يخضع حمض الستريك (C 18) لـ 8 دورات أكسدة لتكوين 9 أسيتيل CoA، وفي كل دورة أكسدة يتكون 8 * 5 ATP = 40 ATP، وينتج أسيتيل CoA 9 * 12 ATP = 108 ATP. الإجمالي: 148 ATP، ولكن يتم إنفاق 1 ATP على تنشيط الأحماض الدهنية في العصارة الخلوية، وبالتالي يكون المجموع 147 ATP
β - أكسدة الأحماض الدهنية العالية (HFAs). كفاءة الطاقة في العملية (للأحماض الدهنية المشبعة وغير المشبعة). تأثير أكسدة الأنسجة IVFA على استخدام الجلوكوز بواسطة الأنسجة.
الأكسدة - مسار محدد لتقويض الأحماض الدهنية بسلاسل هيدروكربونية متوسطة وقصيرة غير متفرعة. تحدث أكسدة β في مصفوفة الميتوكوندريا، حيث يتم فصل ذرتين C بشكل تسلسلي عن الطرف C للـ FA في شكل أسيتيل CoA. تحدث أكسدة β للـ FA فقط في الظروف الهوائية وهي مصدر لكميات كبيرة من الطاقة، وتحدث أكسدة β للـ FA بشكل نشط في العضلات الهيكلية الحمراء وعضلة القلب والكلى والكبد. لا تعمل الـ FAs كمصدر للطاقة للأنسجة العصبية، لأن الـ FAs لا تمر عبر حاجز الدم في الدماغ، مثل المواد الأخرى الكارهة للماء، ويزداد أكسدة الـ β في فترة ما بعد الامتصاص، أثناء الصيام والعمل البدني. في الوقت نفسه، يزداد تركيز FAs في الدم نتيجة لتعبئة FAs من الأنسجة الدهنية.
تفعيل شاشات الكريستال السائل
يحدث تنشيط FA نتيجة لتكوين رابطة عالية الطاقة بين FA وHSCoA مع تكوين Acyl-CoA. يتم تحفيز التفاعل بواسطة إنزيم إنزيم Acyl-CoA Synthetase:
RCOOH + HSKoA + ATP → RCO~SCoA + AMP+ PPn
يتم تحلل البيروفوسفات بواسطة إنزيم بيروفوسفاتيز: H 4 P 2 O 7 + H 2 O → 2 H 3 PO 4
تم العثور على إنزيمات Acyl-CoA في العصارة الخلوية (على الغشاء الخارجي للميتوكوندريا) وفي مصفوفة الميتوكوندريا. تختلف هذه الإنزيمات في خصوصيتها بالنسبة للـ FAs ذات أطوال سلسلة هيدروكربونية مختلفة.
شاشات الكريستال السائل النقل. يعتمد نقل FAs إلى مصفوفة الميتوكوندريا على طول سلسلة الكربون.
يمكن للـ FAs ذات أطوال السلسلة القصيرة والمتوسطة (من 4 إلى 12 ذرة C) أن تخترق مصفوفة الميتوكوندريا عن طريق الانتشار. يحدث تنشيط هذه الـ FAs عن طريق صناعات أسيل CoA في مصفوفة الميتوكوندريا، ويتم تنشيط FAs طويلة السلسلة أولاً في العصارة الخلوية (بواسطة صناعات أسيل CoA على الغشاء الخارجي للميتوكوندريا)، ثم يتم نقلها إلى مصفوفة الميتوكوندريا بواسطة نظام نقل خاص. باستخدام الكارنيتين. كارنيتين يأتي من الطعام أو يتم تصنيعه من الليسين والميثيونين بمشاركة فيتامين سي.
في الغشاء الخارجي للميتوكوندريا، يحفز إنزيم كارنيتين أسيل ترانسفيراز I (كارنيتين بالميتويل ترانسفيراز I) نقل الأسيل من CoA إلى كارنيتين لتكوين أسيل كارنيتين؛
يمر أسيل كارنيتين عبر الفضاء بين الغشاء إلى الجانب الخارجي للغشاء الداخلي ويتم نقله بواسطة كارنيتين أسيل كارنيتين ترانزلوكاز إلى السطح الداخلي للغشاء الداخلي للميتوكوندريا؛
يحفز إنزيم كارنيتين أسيل ترانسفيراز II نقل الأسيل من الكارنيتين إلى HSCoA داخل الميتوكوندريا لتكوين Acyl-CoA؛
يتم إرجاع الكارنيتين الحر إلى الجانب العصاري الخلوي للغشاء الداخلي للميتوكوندريا بواسطة نفس المترجم.
تفاعلات β-أكسدة FA
1. تبدأ أكسدة β بإزالة هيدروجين أسيل CoA بواسطة نازعة هيدروجين الأسيل CoA المعتمدة على FAD، مما يشكل رابطة مزدوجة (ترانس) بين ذرات α- وβ-C في Enoyl-CoA. يضمن تقليل FADN 2، المؤكسد في CPE، تخليق جزيئين من ATP؛
2. يضيف هيدراتاز Enoyl-CoA الماء إلى الرابطة المزدوجة لـ Enoyl-CoA لتكوين β-hydroxyacyl-CoA؛
3. يتأكسد β-hydroxyacyl-CoA بواسطة نازعة الهيدروجين المعتمدة على NAD إلى β-ketoacyl-CoA. يضمن تقليل NADH 2، المؤكسد إلى CPE، تخليق 3 جزيئات ATP؛
4. ثيوليز بمشاركة HCoA يشق أسيتيل CoA من β-ketoacyl-CoA. ونتيجة لأربعة تفاعلات يتكون أسيل CoA، وهو أقصر من أسيل CoA السابق بمقدار ذرتين كربون. يضمن الأسيتيل-CoA، المؤكسد في دورة TCA، تخليق 12 جزيء ATP في CPE.
ثم يدخل Acyl-CoA مرة أخرى في تفاعلات الأكسدة. تستمر الدورات حتى يتحول Acyl-CoA إلى Acetyl-CoA مع ذرتين C (إذا كان FA يحتوي على عدد زوجي من ذرات C) أو Butyryl-CoA مع 3 ذرات C (إذا كان FA يحتوي على عدد فردي من ذرات C).
توازن الطاقة لأكسدة الأحماض الدهنية المشبعة مع عدد زوجي من ذرات الكربون
عند تنشيط FA، يتم استهلاك 2 روابط كبيرة من ATP.
أثناء أكسدة FA المشبع بعدد زوجي من ذرات C، يتم تشكيل FADH 2 وNADH 2 وAcetyl-CoA فقط.
خلال دورة واحدة من أكسدة بيتا، يتم تكوين 1 FADH 2 و1 NADH 2 و1 أسيتيل CoA، والتي تنتج عند الأكسدة 2 + 3 + 12 = 17 ATP.
عدد الدورات أثناء أكسدة β لـ FA = عدد ذرات C في (FA/2)-1. أثناء الأكسدة بيتا، يخضع حمض البالمتيك لـ (16/2)-1 = 7 دورات. في 7 دورات، يتم تكوين 17*7=119 ATP.
الدورة الأخيرة من أكسدة بيتا تكون مصحوبة بتكوين أسيتيل CoA إضافي، والذي عند الأكسدة ينتج 12 ATP.
وبالتالي فإن أكسدة حمض البالمتيك تنتج: -2+119+12=129ATP.
معادلة ملخصة لأكسدة β، بالميتويل-CoA:
C 15 H 31 CO-CoA + 7 FAD + 7 NAD + + 7 HSKoA → 8 CH 3 -CO-KoA + 7 FADH 2 + 7 NADH 2
توازن الطاقة لأكسدة الأحماض الدهنية المشبعة بعدد فردي من ذرات الكربون
تتم عملية أكسدة β لـ FA المشبع بعدد فردي من ذرات C في البداية بنفس الطريقة كما هو الحال مع الرقم الزوجي. يتم إنفاق 2 روابط كبيرة من ATP على التنشيط.
يخضع FA الذي يحتوي على 17 ذرة C لأكسدة β 17/2-1 = 7 دورات. في دورة واحدة، 2+3+12=17 ATP يتكون من 1 FADN 2، 1 NADH 2 و1 أسيتيل CoA. في 7 دورات، يتم تكوين 17*7=119 ATP.
الدورة الأخيرة من أكسدة β تكون مصحوبة بتكوين ليس أسيتيل CoA، ولكن بروبيونيل CoA مع 3 ذرات C.
يتم كربوكسيل بروبيونيل-CoA بتكلفة 1 ATP بواسطة كربوكسيلاز بروبيونيل-CoA لتكوين D-methylmalonyl-CoA، والذي، بعد الأيزومرة، يتحول أولاً إلى L-methylmalonyl-CoA ثم إلى Succinyl-CoA. يتم تضمين Succinyl-CoA في دورة TCA، وعند الأكسدة، ينتج PCA و6 ATP. يمكن أن يدخل PIKE في تكوين السكر في الدم لتخليق الجلوكوز. يؤدي نقص فيتامين ب12 إلى تراكم ميثيلمالونيل في الدم وإفرازه في البول. أثناء أكسدة FA، يتكون ما يلي: -2+119-1+6=122 ATP.
المعادلة الشاملة لأكسدة β للـ FAs مع 17 ذرة C:
C 16 H 33 CO-CoA + 7 FAD + 7 NAD + + 7 HSKoA → 7 CH 3 -CO-KoA + 1 C 2 H 5 -CO-KoA + 7 FADH 2 + 7 NADH 2
توازن الطاقة لأكسدة الأحماض الدهنية غير المشبعة مع عدد زوجي من ذرات الكربون
حوالي نصف الأحماض الدهنية الموجودة في جسم الإنسان غير مشبعة. تتم عملية أكسدة هذه الأحماض بالطريقة المعتادة حتى تصبح الرابطة المزدوجة بين ذرات C 3 و4. يقوم إنزيم إيزوميراز إنويل-CoA بعد ذلك بنقل الرابطة المزدوجة من الموضع 3-4 إلى الموضع 2-3 ويغير شكل رابطة الدول المستقلة لـ الرابطة المزدوجة للتحويل، وهو أمر ضروري للأكسدة β. في دورة الأكسدة β هذه، نظرًا لوجود الرابطة المزدوجة بالفعل في FA، لا يحدث أول تفاعل لإزالة الهيدروجين ولا يتم تشكيل FADH 2. علاوة على ذلك، تستمر دورات الأكسدة، ولا تختلف عن المسار المعتاد.
يتم حساب توازن الطاقة بنفس الطريقة كما هو الحال مع FAs المشبعة مع عدد زوجي من ذرات C، فقط لكل رابطة مزدوجة 1 FADN 2، وبالتالي، 2 ATP مفقودة.
المعادلة الشاملة لأكسدة β لـ palmitoleyl-CoA هي:
C 15 H 29 CO-CoA + 6 FAD + 7 NAD + + 7 HSKoA → 8 CH 3 -CO-KoA + 6 FADH 2 + 7 NADH 2
توازن الطاقة لأكسدة β لحمض البالميتوليك: -2+8*12+6*2+7*3=127 ATP.
الجوع والنشاط البدني → الجلوكاجون والأدرينالين → تحلل الدهون TG في الخلايا الشحمية → FA في الدم → أكسدة β في ظل الظروف الهوائية في العضلات والكبد → 1) ATP؛ 2) ATP، NADH 2، Acetyl-CoA، (FA) → ↓ تحلل السكر → توفير الجلوكوز الضروري للأنسجة العصبية وخلايا الدم الحمراء، إلخ.
الغذاء ← الأنسولين ← تحلل السكر ← أسيتيل CoA ← تخليق malonyl-CoA وFA
تخليق malonyl-CoA → malonyl-CoA → ↓ carnitine acyltransferase I في الكبد → ↓ نقل FAs إلى مصفوفة الميتوكوندريا → ↓ FAs في المصفوفة → ↓ β-أكسدة FAs
التخليق الحيوي لـ IVFA. هيكل مجمع سينسيز بالميتات. الكيمياء وتنظيم العملية.
تخليق حمض البالمتيك
تكوين المالونيل-CoA
التفاعل الأول في تخليق FA هو تحويل أسيتيل مرافق الإنزيم أ إلى مالونيل مرافق الإنزيم أ. يتم تحفيز هذا التفاعل التنظيمي في تخليق FA بواسطة كربوكسيلاز أسيتيل CoA.
يتكون كربوكسيلاز Acetyl-CoA من عدة وحدات فرعية تحتوي على البيوتين.
يحدث التفاعل على مرحلتين:
1) CO 2 + بيوتين + ATP → بيوتين-COOH + ADP + Fn
2) أسيتيل مرافق الإنزيم أ + بيوتين- كوه → مالونيل مرافق الإنزيم أ + بيوتين
يتم تنظيم كربوكسيلاز Acetyl-CoA بعدة طرق:
3) رابطة/تفكك مجمعات الوحدات الفرعية الإنزيمية. في شكله غير النشط، أسيتيل CoA كربوكسيلاز عبارة عن مركب يتكون من 4 وحدات فرعية. يحفز السيترات اتحاد المجمعات، مما يؤدي إلى زيادة نشاط الإنزيم. يتسبب Palmitoyl-CoA في تفكك المجمعات وانخفاض نشاط الإنزيم؛
2) الفسفرة/نزع الفسفرة من كربوكسيلاز أسيتيل CoA. يقوم الجلوكاجون أو الأدرينالين، من خلال نظام محلقة الأدينيلات، بتحفيز الفسفرة في الوحدات الفرعية من كربوكسيلاز أسيتيل CoA، مما يؤدي إلى تعطيله. ينشط الأنسولين فوسفاتاز البروتين الفوسفاتي، ويتم نزع كربوكسيلاز أسيتيل CoA. ثم، تحت تأثير السيترات، تحدث بلمرة بروتومرات الإنزيم، وتصبح نشطة؛
3) يؤدي الاستهلاك طويل الأمد للأطعمة الغنية بالكربوهيدرات وفقيرة الدهون إلى زيادة إفراز الأنسولين، مما يحفز تخليق كربوكسيلاز أسيتيل CoA، وسينسيز بالميتات، وسيترات لياز، وإيزوسيترات ديهيدروجينيز، ويسرع تخليق FA و تي جي. يؤدي الصيام أو تناول نظام غذائي غني بالدهون إلى انخفاض في تخليق الإنزيمات، وبالتالي FA وTG.
تكوين حمض البالمتيك
بعد تكوين malonyl-CoA، يستمر تصنيع حمض البالمتيك في مركب متعدد الإنزيمات - سينسيز الأحماض الدهنية (سينثيتاس بالميتويل) .
بالميتويل سينسيز هو ثنائي يتكون من سلسلتين متماثلتين من البولي ببتيد. تحتوي كل سلسلة على 7 مواقع نشطة وبروتين نقل الأسيل (ACP). تحتوي كل سلسلة على مجموعتين من SH: مجموعة SH واحدة تنتمي إلى السيستين، والأخرى تنتمي إلى بقايا حمض الفوسفوبانثيتيك. توجد مجموعة السيستين SH لأحد المونومر بجوار مجموعة SH 4-phosphopantetheinate للبروتومر الآخر. وهكذا يتم ترتيب بروتومرات الإنزيم "من الرأس إلى الذيل". على الرغم من أن كل مونومر يحتوي على جميع المواقع الحفزية، إلا أن مجمعًا مكونًا من بروتومرين نشط وظيفيًا. لذلك، يتم بالفعل تصنيع 2 LCs في وقت واحد.
يقوم هذا المركب بتمديد جذر FA بشكل تسلسلي بمقدار ذرتين C، الجهة المانحة لها هي malonyl-CoA.
تفاعلات تخليق حمض البالمتيك
1) نقل الأسيتيل من CoA إلى مجموعة SH من السيستين بواسطة مركز أسيتيل ترانسسيلاز.
2) نقل المالونيل من CoA إلى مجموعة SH من ACP بواسطة مركز malonyl transacylase؛
3) في مركز سينسيز كيتواسيل، تتكثف مجموعة الأسيتيل مع مجموعة المالونيل لتكوين كيتواسيل وإطلاق ثاني أكسيد الكربون.
4) يتم اختزال الكيتواسيل بواسطة إنزيم كيتواسيل المختزل إلى هيدروكسي أسيل؛
5) يتم تجفيف الأوكسيسيل بواسطة الهيدراتاز وتحويله إلى الإينويل؛
6) يتم اختزال الإينويل بواسطة إنزيم اختزال الإينويل إلى أسيل.
نتيجة للدورة الأولى من التفاعلات، يتم تشكيل أسيل يحتوي على 4 ذرات C (بوتيريل). بعد ذلك، يتم نقل البوتيريل من الموضع 2 إلى الموضع 1 (حيث كان الأسيتيل موجودًا في بداية الدورة الأولى من التفاعلات). يخضع البيوتيريل بعد ذلك لنفس التحولات ويتم تمديده بواسطة ذرتين C (من malonyl-CoA).
تتكرر دورات مماثلة من التفاعلات حتى يتم تشكيل جذر حمض البالمتيك، والذي، تحت تأثير مركز الثيوستيراز، يتم فصله مائيًا عن مجمع الإنزيم، ويتحول إلى حمض البالمتيك الحر.
المعادلة الشاملة لتخليق حمض البالمتيك من الأسيتيل-CoA والمالونيل-CoA هي كما يلي:
CH 3 -CO-SKoA + 7 HOOC-CH 2 -CO-SKoA + 14 NADPH 2 → C 15 H 31 COOH + 7 CO 2 + 6
H 2 O + 8 HS KoA + 14 NADP +
توليف FAs من Palmitic و FAs الأخرى
استطالة FAs في تفاعلات الاستطالة
إطالة الأحماض الدهنية تسمى استطالة. يمكن تصنيع FAs نتيجة لاستطالة حمض البالمتيك وغيره من FAs الأطول في ER. هناك استطالات لكل طول LC. تسلسل التفاعلات يشبه تخليق حمض البالمتيك، ولكن في هذه الحالة لا يحدث التوليف مع ACP، ولكن مع CoA. منتج الاستطالة الرئيسي في الكبد هو حمض دهني. في الأنسجة العصبية، يتم تشكيل FAs طويلة السلسلة (C = 20-24)، وهي ضرورية لتخليق الشحميات السفينجولية.
توليف FAs غير المشبعة في تفاعلات التشبع
يُطلق على إدراج الروابط المزدوجة في جذور FA اسم التشبع. يحدث عدم تشبع FAs في ER في تفاعلات أحادي الأكسجين المحفزة بواسطة desaturases.
إزالة التشبع Stearoyl-CoA– إنزيم متكامل يحتوي على حديد غير الهيم. يحفز تكوين رابطة مزدوجة واحدة بين 9 و10 ذرات كربون في FA. ينقل إنزيم Stearoyl-CoA desaturase الإلكترونات من السيتوكروم ب 5 إلى ذرة أكسجين واحدة، بمشاركة البروتونات، ويشكل هذا الأكسجين الماء. يتم دمج ذرة الأكسجين الثانية في حمض دهني لتكوين الهيدروكسيل، الذي ينزع الهيدروجين إلى حمض الأوليك.
لا يمكن لـ FA desaturases الموجودة في جسم الإنسان أن تشكل روابط مزدوجة في FAs البعيدة عن ذرة الكربون التاسعة، وبالتالي لا يتم تصنيع FAs من عائلات ω-3 وω-6 في الجسم، وهي ضرورية ويجب تزويدها بالطعام، لأنها أداء وظائف تنظيمية مهمة. إن العناصر الأساسية التي تتشكل في جسم الإنسان نتيجة عدم التشبع هي البالميتوليك والأوليك.
توليف α-هيدروكسي FAs
يحدث أيضًا تخليق FAs الأخرى، أحماض ألفا هيدروكسي، في الأنسجة العصبية. أكاسيداز مختلط الوظائف أحماض هيدروكسيلات C22 و C24 لتكوين حمض المخيخ، الموجود فقط في دهون الدماغ.
تشكل الكربوهيدرات الجزء الأكبر من النظام الغذائي للإنسان وتوفر جزءًا كبيرًا من احتياجات الجسم من الطاقة. مع اتباع نظام غذائي متوازن، تكون الكمية اليومية من الكربوهيدرات في المتوسط 4 مرات أعلى من كمية البروتينات والدهون.
دور الكربوهيدرات في التغذية:
1. الكربوهيدرات تفعل ذلك وظيفة الطاقة.عند أكسدة 1 جرام من الكربوهيدرات، يتم إطلاق 4.1 كيلو كالوري من الطاقة. الجلوكوز، الذي يتم فيه تكسير الجزء الأكبر من الكربوهيدرات، هو ركيزة الطاقة الرئيسية في الجسم.
2. نشاط العضلاتيرافقه استهلاك كبير للجلوكوز. أثناء العمل البدني، يتم استهلاك الكربوهيدرات أولاً، وفقط عندما يتم استنفاد احتياطياتها (الجليكوجين) يتم تضمين الدهون في عملية التبادل.
3. الكربوهيدرات ضرورية للوظيفة الطبيعية الجهاز العصبي المركزي،الذين تكون خلاياهم حساسة جدًا لنقص الجلوكوز في الدم.
4. الكربوهيدرات تفعل ذلك الوظيفة الهيكلية.تعمل الكربوهيدرات البسيطة كمصدر لتكوين البروتينات السكرية، التي تشكل أساس النسيج الضام.
5. الكربوهيدرات تشارك في استقلاب البروتينات والدهون.يمكن أن تتكون الدهون من الكربوهيدرات.
6. الكربوهيدرات من أصل نباتي (مواد السليلوز والبكتين) تحفز حركية الأمعاء وتساهم في التخلص من المنتجات السامة التي تتراكم فيها.
مصادرتخدم الكربوهيدرات في الغالب المنتجات النباتية,وخاصة منتجات الدقيق والحبوب والحلويات. يتم تقديم الكربوهيدرات في معظم الأطعمة على شكل نشا وبدرجة أقل على شكل سكريات ثنائية (الحليب وبنجر السكر والفواكه والتوت). لتحسين امتصاص الكربوهيدرات، من الضروري أن يدخل معظمها الجسم في شكل نشا.
ويتحلل النشا تدريجياً في القناة الهضمية إلى جلوكوز، الذي يدخل الدم بأجزاء صغيرة، مما يحسن الاستفادة منه ويحافظ على مستوى ثابت للسكر في الدم. عندما يتم تناول كميات كبيرة من السكر دفعة واحدة، فإن تركيز الجلوكوز في الدم يزداد بشكل حاد، ويبدأ في التخلص منه في البول. تعتبر الظروف الأكثر ملاءمة عندما يتم استهلاك 64٪ من الكربوهيدرات على شكل نشا و 36٪ على شكل سكريات.
معدل الاستهلاكالكربوهيدرات تعتمد على شدة العمل. أثناء العمل البدني، هناك حاجة إلى الكربوهيدرات بكميات أكبر. في المتوسط، مطلوب لكل 1 كجم من وزن الجسم 4-6-8 غرام من الكربوهيدرات يوميا، أي. حوالي 4 مرات أكثر من البروتينات والدهون.
الإفراط في تناول الكربوهيدراتيمكن أن يؤدي إلى السمنة والحمل الزائد المفرط للجهاز الهضمي، لأن عادة ما تكون الأطعمة النباتية الغنية بالكربوهيدرات أكبر حجمًا وتسبب الشعور بالثقل وتضعف هضم الطعام بشكل عام.
نقص الكربوهيدراتفي الغذاء أيضًا غير مرغوب فيه بسبب خطر الإصابة بحالات نقص السكر في الدم. عادة ما يكون نقص الكربوهيدرات مصحوبًا بالضعف العام والنعاس وانخفاض الذاكرة والأداء العقلي والبدني والصداع وانخفاض هضم البروتينات والفيتامينات والحماض وما إلى ذلك. وفي هذا الصدد، لا ينبغي أن تكون كمية الكربوهيدرات في النظام الغذائي اليومي أن يكون أقل من 300 جرام
ترتبط ارتباطًا وثيقًا بمجموعة الكربوهيدرات بالمواد الموجودة في معظم الأطعمة النباتية التي يصعب هضمها بواسطة جسم الإنسان - مواد البكتين (الكربوهيدرات غير القابلة للهضم) والألياف.
المواد البكتيرية هيمواد تبلور نباتية ذات قدرة عالية على الامتصاص. لها تأثير مفيد في علاج أمراض الجهاز الهضمي والحروق والتقرحات، كما أن لها القدرة على تحييد بعض المواد السامة (تنشط بشكل خاص في إزالة أملاح المعادن الثقيلة، مثل مركبات الرصاص، من الجسم).
يوجد الكثير من مواد البكتين في البرتقال والتفاح والكشمش الأسود والفواكه والتوت الأخرى.
السليلوز(أسماء أخرى - الخضار الخشنة، أو غير القابلة للهضم، أو الطعام، أو الألياف الغذائية) هو السكاريد الذي يشكل جزءًا من جدران الخلايا الضخمة للأغذية النباتية. لها هيكل ليفي خشن إلى حد ما.
المصادر الشائعة للألياف الغذائية هي النخالة والخبز والحبوب (خاصة الحنطة السوداء ودقيق الشوفان). وتوجد بكميات كبيرة في العديد من الخضروات والفواكه وأوراق وسيقان النباتات؛ يوجد الكثير منه بشكل خاص في قشور الحبوب وفي قشور الفواكه. عند تعليب الخضار والفواكه، يتم الحفاظ على الألياف الغذائية بشكل كامل (ما عدا العصائر بدون لب).
مع عدم وجود نسبة عالية من السعرات الحرارية، فإن معظم الخضروات والفواكه، بسبب المحتوى العالي من الكربوهيدرات غير القابلة للهضم، تساهم في شعور سريع ومستمر إلى حد ما بالشبع: نظرًا لأن الألياف الغذائية لديها القدرة على امتصاص الكثير من السوائل، فإنها تنتفخ المعدة تملأ جزءًا من حجمها - ونتيجة لذلك يحدث التشبع بشكل أسرع. الألياف نفسها لا تحمل سعرًا حراريًا واحدًا إلى الجسم.
تكمن قيمة الألياف في حقيقة أنها مكون ضخم إلى حد ما من التغذية اليومية، ولا يتم هضمها من قبل جسم الإنسان. إن وجود كمية كبيرة من الألياف يقلل إلى حد ما من هضم الطعام بشكل عام. ومع ذلك، فإن غيابه الكامل له تأثير ضار على عمل الجهاز الهضمي.
تسبب الألياف التمعج المناسب (حركة الجدران) للأمعاء وبالتالي تعزز حركة الطعام عبر القناة الهضمية وإزالة العناصر الغذائية غير المهضومة من الجسم.
يتم ضمان الكمية المطلوبة من الألياف في الطعام من خلال المزيج الصحيح من المنتجات الحيوانية والنباتية في النظام الغذائي اليومي.
بعد تحللها، تتحول الألياف، مثل السكريات الأخرى، إلى سكريات. ومع ذلك، لا توجد إنزيمات في الجهاز الهضمي البشري يمكنها القيام بمثل هذا الانهيار. ويمكن هضم جزء صغير منه فقط تحت تأثير الكائنات الحية الدقيقة الموجودة في الأمعاء، أما الجزء الأكبر فيتم إخراجه من الجسم دون تغيرات. بفضل هذا عدم الفائدة الخارجية، تسمى الألياف والبكتين بمواد الصابورة.
تؤدي مواد الصابورة أيضًا وظيفة مهمة في عملية الهضم: حيث يتم تخمير الألياف بواسطة البكتيريا المعوية وتساعد حرفيًا على طحن الطعام؛ عن طريق تهيج النهايات العصبية لجدران الأمعاء، فإنها تزيد من التمعج. إذا كان الطعام فقيرًا بالمواد الصابورة، تتعطل حركية الأمعاء، لذلك لتجنب هذه الاضطرابات يوصى باستخدام الأطعمة الخشنة الغنية بالألياف.
بالإضافة إلى ذلك، تتمتع الألياف الغذائية بالقدرة على تحفيز عملية التمثيل الغذائي، حيث تمنع الألياف امتصاص السموم التي تأتي مع الطعام أو التي تتشكل أثناء معالجته، وتعمل كنوع من الخفق: تتحرك على طول الجهاز الهضمي، وتأخذ معها كل ما قد تمسك بالجدران وإزالتها من الجسم.
ميزة أخرى للألياف الغذائية هي أن لها القدرة على خفض مستوى الكولسترول الداخلي (وهذا هو الكولسترول الذي لا يدخل إلينا مع الطعام، ولكن ينتجه الجسم نفسه في الكبد من الأحماض الصفراوية التي تدخل الكبد من الأمعاء) ).
الهيميسيلولوز:مثل الألياف، أو السليلوز، فهو جزء من جدران خلايا منتجات الحبوب، وتوجد بكميات قليلة في لب الفواكه والخضروات. وهي قادرة على الاحتفاظ بالمياه وربط المعادن.
أكسدة الأحماض الدهنية (أكسدة بيتا). دور ه.س. – كو في هذه العملية. طاقة الأكسدة الكاملة لحمض الستيوريك شركة 2 ج ح 2 يا . احسب عدد جزيئات ATP المتكونة أثناء الأكسدة.
يحدث تنشيط FA في السيتوبلازم، وتحدث أكسدة بيتا في الميتوكوندريا.
لا يمكن لـ Acyl-CoA المرور عبر غشاء الميتوكوندريا. ولذلك، هناك آلية خاصة لنقل FAs من السيتوبلازم إلى الميتوكوندريا بمشاركة مادة “الكارنيتين”. يوجد في الغشاء الداخلي للميتوكوندريا بروتين نقل خاص يضمن النقل. بفضل هذا، يخترق Acylcarnitine بسهولة غشاء الميتوكوندريا.
تختلف إنزيمات أسيل ترانسفيراز الكارنيتين السيتوبلازمية والميتوكوندريا في البنية، كما أنها تختلف عن بعضها البعض في الخصائص الحركية. يكون Vmax لأنزيم ترانسفيراز الأسيل كارنيتين السيتوبلازمي أقل من Vmax لإنزيم الميتوكوندريا، وأيضًا أقل من Vmax لإنزيمات الأكسدة بيتا. ولذلك، فإن ترانسفيراز أسيل كارنيتين السيتوبلازمي هو إنزيم رئيسي في تحلل الأحماض الدهنية.
إذا دخل حمض دهني إلى الميتوكوندريا، فسوف يخضع بالضرورة لعملية تقويض إلى أسيتيل CoA.
إن "الوقود" الأكثر إحكاما الذي يلبي احتياجات الجسم من الطاقة هو الأحماض الدهنية، والتي يتم تحديدها من خلال خصائص تركيبها الكيميائي. لكل مول واحد، تطلق الأكسدة الكاملة للأحماض الدهنية طاقة كيميائية قابلة للاستخدام عدة مرات أكثر من أكسدة الكربوهيدرات؛ على سبيل المثال، أكسدة 1 مول من حمض البالمتيك تنتج 130 مول من ATP، في حين أن أكسدة 1 مول من الجلوكوز تنتج 38 مول من ATP. لكل وحدة وزن، يختلف إنتاج الطاقة أيضًا بأكثر من مرتين (9 سعرة حرارية لكل 1 جرام من الدهون مقابل 4 سعرة حرارية لكل 1 جرام من الكربوهيدرات أو البروتينات). يعتمد إنتاج الطاقة المرتفع هذا على نفس السبب الذي يجعل البنزين والبترول والمنتجات البترولية الأخرى وقودًا فعالًا لتوليد الطاقة الحرارية والميكانيكية، وهو الدرجة العالية لاختزال الكربون في سلاسل الألكيل الطويلة. يتكون الجزء الرئيسي من جزيء الأحماض الدهنية من وحدات متكررة (CH2)n، أي بنية مخصبة إلى الحد الأقصى بالهيدروجين. كما رأينا من العرض السابق، فإن الطاقة المخزنة أثناء عمليات الأكسدة البيولوجية تتشكل بشكل رئيسي فيما يتعلق بالانتقال المتحكم فيه للإلكترونات من ذرات الهيدروجين في السلسلة التنفسية، إلى جانب فسفرة ADP إلى ATP. نظرًا لأن الأحماض الدهنية تتكون أساسًا من الكربون والهيدروجين وبالتالي تحتوي على ذرات أكسجين أقل بكثير من الكربوهيدرات، فإن أكسدة الأحماض الدهنية يصاحبها امتصاص كمية أكبر نسبيًا من الأكسجين، وبالتالي تكوين المزيد من ATP أثناء الفسفرة التأكسدية.
لقد ثبت أن أكسدة الأحماض الدهنية تحدث بشكل مكثف في الكبد والكلى والعضلات الهيكلية والقلبية وفي الأنسجة الدهنية. في أنسجة المخ، يكون معدل أكسدة الأحماض الدهنية منخفضًا جدًا، وذلك لأن المصدر الرئيسي للطاقة في أنسجة المخ هو الجلوكوز.
الأكسدة بيتا هي مسار محدد لتقويض الأحماض الدهنية، حيث يتم فصل ذرتين كربون بشكل تسلسلي عن نهاية الكربوكسيل للحمض الدهني في شكل أسيتيل مرافق الإنزيم أ. سمي المسار الأيضي -أكسدة بيتا - بهذا الاسم لأن تفاعلات أكسدة الأحماض الدهنية تحدث عند ذرة الكربون بيتا. تعمل تفاعلات الأكسدة β والأكسدة اللاحقة لأسيتيل CoA في دورة TCA كأحد مصادر الطاقة الرئيسية لتخليق ATP عبر آلية الفسفرة التأكسدية. β-أكسدة الأحماض الدهنية تحدث فقط في الظروف الهوائية.
تفعيل الأحماض الدهنية
قبل الدخول في التفاعلات المختلفة يجب تفعيل الأحماض الدهنية، أي: ترتبط برابطة كبيرة مع الإنزيم المساعد A:
RCOOH + HSKoA + ATP → RCO ~ CoA + AMP + PPi.
يتم تحفيز التفاعل بواسطة إنزيم أسيل-CoA سينثيتيز. يتم تحلل البيروفوسفات المنطلق أثناء التفاعل بواسطة إنزيم بيروفوسفاتيز: H 4 P 2 O 7 + H 2 O → 2 H 3 PO 4.
يؤدي إطلاق الطاقة أثناء التحلل المائي لرابطة البيروفوسفات عالية الطاقة إلى تحويل توازن التفاعل إلى اليمين ويضمن اكتمال تفاعل التنشيط.
إنزيم أسيل-CoAتم العثور عليها في العصارة الخلوية وفي مصفوفة الميتوكوندريا. تختلف هذه الإنزيمات في خصوصيتها بالنسبة للأحماض الدهنية ذات أطوال السلسلة الهيدروكربونية المختلفة. يمكن للأحماض الدهنية ذات السلسلة القصيرة والمتوسطة الطول (من 4 إلى 12 ذرة كربون) أن تخترق مصفوفة الميتوكوندريا عن طريق الانتشار. يحدث تنشيط هذه الأحماض الدهنية في مصفوفة الميتوكوندريا. يتم تنشيط الأحماض الدهنية طويلة السلسلة، والتي تسود في جسم الإنسان (12 إلى 20 ذرة كربون)، بواسطة إنزيمات أسيل-CoA الموجودة على الغشاء الخارجي للميتوكوندريا.
يحدث انهيار الأحماض الدهنية المنشطة وفقًا للفرضية ب - الأكسدة F. Knoop، اقترح عام 1904 ب - تحدث الأكسدة داخل الميتوكوندريا
β- أكسدة الأحماض الدهنية- مسار محدد لتقويض الأحماض الدهنية، يحدث في مصفوفة الميتوكوندريا فقط في ظل الظروف الهوائية وينتهي بتكوين أسيتيل مرافق الإنزيم أ. يدخل الهيدروجين الناتج عن تفاعلات الأكسدة β إلى CPE، ويتأكسد الأسيتيل CoA في دورة السيترات، والتي تزود أيضًا الهيدروجين إلى CPE. ولذلك، فإن أكسدة الأحماض الدهنية هي أهم مسار استقلابي يوفر تخليق ATP في السلسلة التنفسية.
تبدأ الأكسدة β بإزالة هيدروجين أسيل CoA بواسطة نازع هيدروجين الأسيل CoA المعتمد على FAD، مما يشكل رابطة مزدوجة بين ذرات الكربون α و β في منتج التفاعل، enoyl-CoA. يقوم الإنزيم المساعد FADH 2، الذي تم استعادته في هذا التفاعل، بنقل ذرات الهيدروجين الموجودة في CPE إلى الإنزيم المساعد Q. ونتيجة لذلك، يتم تصنيع جزيئين ATP (الشكل 8-27). في تفاعل الأكسدة p التالي، تتم إضافة جزيء ماء في موقع الرابطة المزدوجة بحيث تقع مجموعة OH عند ذرة الكربون β في الأسيل، مكونة β-hydroxyacyl-CoA. يتم بعد ذلك أكسدة β-hydroxyacyl-CoA بواسطة نازعة الهيدروجين المعتمدة على NAD+. يوفر NADH المخفض، المؤكسد في CPE، الطاقة اللازمة لتخليق 3 جزيئات ATP. يخضع β-ketoacyl-CoA الناتج إلى انقسام ثيولاز بواسطة إنزيم ثيوليز، لأنه في موقع انقسام رابطة CC، تتم إضافة جزيء من الإنزيم المساعد A من خلال ذرة الكبريت. ونتيجة لهذا التسلسل من 4 تفاعلات، يتم فصل بقايا ثنائي الكربون، أسيتيل CoA، عن أسيل CoA. يخضع الحمض الدهني المختصر بذرتي كربون مرة أخرى لتفاعلات نزع الهيدروجين، والترطيب، ونزع الهيدروجين، وإزالة أسيتيل مرافق الإنزيم أ. عادةً ما يُطلق على تسلسل التفاعلات هذا اسم "دورة الأكسدة بيتا"، مما يعني أن نفس التفاعلات تتكرر مع جذري الأحماض الدهنية حتى يتم تحويل كل الحمض إلى بقايا الأسيتيل.
β - أكسدة الأحماض الدهنية.
عملية الأكسدة ب هي عملية دورية.في كل دورة من الدورة، يتم فصل ذرتي كربون من الحمض الدهني على شكل بقايا الأسيتيل.
بعد ذلك، يخضع أسيل CoA، الذي تم اختصاره بذرتي كربون، للأكسدة مرة أخرى (يدخل في دورة جديدة من تفاعلات الأكسدة ب). يمكن أن يدخل الأسيتيل CoA الناتج إلى دورة حمض ثلاثي الكربوكسيل، ويجب أن تكون قادرًا على حساب إنتاج الطاقة من تحلل الأحماض الدهنية. الصيغة المقدمة صحيحة بالنسبة لأي حمض دهني مشبع يحتوي على ذرات كربون n، وينتج عن انهيار الأحماض الدهنية غير المشبعة كمية أقل من ATP. كل رابطة مزدوجة في حمض دهني تعني فقدان جزيئين من ATP. تحدث الأكسدة بشكل مكثف في الأنسجة العضلية والكلى والكبد.نتيجة لأكسدة FA، يتم تشكيل أسيتيل CoA. يتم تحديد معدل الأكسدة بمعدل عمليات تحلل الدهون. إن تسريع تحلل الدهون هو سمة من سمات حالة تجويع الكربوهيدرات والعمل العضلي المكثف. ويلاحظ تسارع الأكسدة ب في العديد من الأنسجة، بما في ذلك الكبد. ينتج الكبد كمية من الأسيتيل CoA أكثر مما يحتاجه. الكبد هو "عضو إيثاري" ولذلك يرسل الكبد الجلوكوز إلى الأنسجة الأخرى.
يسعى الكبد لإرسال أسيتيل مرافق الإنزيم أ الخاص به إلى الأنسجة الأخرى، لكنه لا يستطيع ذلك، لأن أغشية الخلايا غير منفذة لأسيتيل مرافق الإنزيم أ. ولذلك، يتم تصنيع مواد خاصة تسمى "أجسام الكيتون" في الكبد من أسيتيل مرافق الإنزيم أ. أجسام الكيتون هي شكل خاص من أشكال نقل الأسيتيل CoA.
يتم تقسيم جزيء الأحماض الدهنية إلى الميتوكوندريا عن طريق الإزالة التدريجية لشظايا الكربون الثنائية في شكل أنزيم الأسيتيل A (أسيتيل CoA).
C17H35COOH + 26 O2 = 18 CO2 + 18 H2O.
عندما يتأكسد حمض دهني، سوف تتلقى الخلية 146 جزيء ATP.
لتحويل الطاقة الموجودة في الأحماض الدهنية إلى طاقة روابط ATP، هناك مسار استقلابي لأكسدة الأحماض الدهنية إلى ثاني أكسيد الكربون والماء، والذي يرتبط ارتباطًا وثيقًا بدورة حمض ثلاثي الكربوكسيل والسلسلة التنفسية. هذا المسار يسمى الأكسدة، لأن تحدث أكسدة ذرة الكربون الثالثة من الحمض الدهني (موضع β) إلى مجموعة كربوكسيل، وفي نفس الوقت تنفصل مجموعة الأسيتيل، بما في ذلك C 1 وC 2 من الحمض الدهني الأصلي، عن الحمض.
رسم تخطيطي أولي للأكسدة β
تحدث تفاعلات الأكسدة β الميتوكوندريامعظم خلايا الجسم (ما عدا الخلايا العصبية). يتم استخدام الأحماض الدهنية التي تدخل العصارة الخلوية من الدم أو تظهر أثناء تحلل الدهون للعلامات الموجودة داخل الخلايا الخاصة بها للأكسدة. المعادلة الشاملة لأكسدة حمض البالمتيك هي كما يلي:
بالميتويل-SCoA + 7FAD + 7NAD + + 7H2O + 7HS-KoA → 8Acetyl-SCoA + 7FADH 2 + 7NADH
مراحل أكسدة الأحماض الدهنية
1. قبل اختراق مصفوفة الميتوكوندريا والأكسدة، يجب على الأحماض الدهنية تفعيلفي العصارة الخلوية. يتم تحقيق ذلك عن طريق إضافة الإنزيم المساعد A إليه لتكوين أسيل-SCoA. Acyl-SCoA هو مركب عالي الطاقة. يتم تحقيق عدم انعكاس التفاعل عن طريق التحلل المائي لثنائي الفوسفات إلى جزيئين من حمض الفوسفوريك.
تم العثور على مُصنّعات Acyl-SCoA في الشبكة الإندوبلازمية، وعلى الغشاء الخارجي للميتوكوندريا وداخلها. هناك مجموعة واسعة من التركيبات الخاصة بالأحماض الدهنية المختلفة.
تفاعل تنشيط الأحماض الدهنية
2. Acyl-SCoA غير قادر على المرور عبر غشاء الميتوكوندريا، لذلك هناك طريقة لنقله مع مادة الكارنيتين الشبيهة بالفيتامين. يوجد إنزيم على الغشاء الخارجي للميتوكوندريا كارنيتين أسيل ترانسفيراز I.

نقل الأحماض الدهنية المعتمدة على الكارنيتين إلى الميتوكوندريا
يتم تصنيع الكارنيتين في الكبد والكليتين ثم يتم نقله إلى الأعضاء الأخرى. في داخل الرحمالفترة وفي السنوات المبكرةفي الحياة، أهمية الكارنيتين للجسم كبيرة للغاية. إمداد الطاقة للجهاز العصبي الأطفاليتم تنفيذ الجسم، وعلى وجه الخصوص، الدماغ من خلال عمليتين متوازيتين: أكسدة الأحماض الدهنية المعتمدة على الكارنيتين والأكسدة الهوائية للجلوكوز. الكارنيتين ضروري لنمو الدماغ والحبل الشوكي، ولتفاعل جميع أجزاء الجهاز العصبي المسؤولة عن الحركة والتفاعل العضلي. هناك دراسات تربط بين نقص الكارنيتين الشلل الدماغيوالظاهرة" الموت في المهد".
الأطفال الصغار والأطفال المبتسرون والأطفال منخفضو الوزن عند الولادة حساسون بشكل خاص لنقص الكارنيتين. يتم استنفاد احتياطياتها الداخلية بسرعة في ظل المواقف العصيبة المختلفة (الأمراض المعدية، واضطرابات الجهاز الهضمي، واضطرابات التغذية). يكون التخليق الحيوي للكارنيتين محدودًا بشكل حاد بسبب انخفاض كتلة العضلات، كما أن تناول الأطعمة العادية غير قادر على الحفاظ على مستويات كافية في الدم والأنسجة.
3. بعد الارتباط بالكارنيتين، يتم نقل الحمض الدهني عبر الغشاء بواسطة المترجم. هنا، على الجانب الداخلي للغشاء، يشكل إنزيم كارنيتين أسيل ترانسفيراز II مرة أخرى أسيل-SCoA، الذي يدخل مسار الأكسدة بيتا.
4. العملية نفسها الأكسدةيتكون من 4 تفاعلات تتكرر دوريا. أنها تحدث بالتتابع أكسدة(أسيل-SCoA ديهيدروجينيز)، الترطيب(إنويل-SCoA هيدراتاز) ومرة أخرى أكسدةذرة الكربون الثالثة (hydroxyacyl-SCoA dehydrogenase). في تفاعل الترانسفيراز الأخير، يتم فصل الأسيتيل-SCoA من الحمض الدهني. تتم إضافة HS-CoA إلى الحمض الدهني المتبقي (المختصر بواسطة ذرتي كربون)، ويعود إلى التفاعل الأول. يتكرر هذا حتى تنتج الدورة الأخيرة اثنين من أسيتيل SCoAs.

تسلسل تفاعلات أكسدة الأحماض الدهنية
حساب توازن الطاقة للأكسدة β
في السابق، عند حساب كفاءة الأكسدة، كان معامل P/O لـ NADH يساوي 3.0، لـ FADH 2 – 2.0.
وفقًا للبيانات الحديثة، فإن قيمة معامل P/O لـ NADH تقابل 2.5، لـ FADH 2 – 1.5.
عند حساب كمية ATP المتكونة أثناء أكسدة الأحماض الدهنية، من الضروري مراعاة ما يلي:
- يتم تحديد كمية الأسيتيل SCoA المتكونة من خلال التقسيم المعتاد لعدد ذرات الكربون في الحمض الدهني على 2.
- رقم دورات الأكسدة β. من السهل تحديد عدد دورات الأكسدة، بناءً على مفهوم الأحماض الدهنية كسلسلة من وحدات ثنائية الكربون. عدد الفواصل بين الوحدات يتوافق مع عدد دورات الأكسدة. ويمكن حساب نفس القيمة باستخدام الصيغة (n/2 -1)، حيث n هو عدد ذرات الكربون في الحمض.
- عدد الروابط المزدوجة في الأحماض الدهنية. في تفاعل الأكسدة بيتا الأول، يتم تكوين رابطة مزدوجة بمشاركة FAD. إذا كانت الرابطة المزدوجة موجودة بالفعل في الحمض الدهني، فلا داعي لهذا التفاعل ولا يتكون FADN 2. يتوافق عدد FADN 2 المفقود مع عدد الروابط المزدوجة. التفاعلات المتبقية من الدورة تستمر دون تغييرات.
- كمية طاقة ATP المستهلكة في التنشيط (تتوافق دائمًا مع رابطتين عاليتي الطاقة).
مثال. أكسدة حمض البالمتيك
- نظرًا لوجود 16 ذرة كربون، تنتج أكسدة β 8 جزيئات أسيتيل-SCoA. يدخل الأخير إلى دورة TCA؛ عندما يتأكسد في دورة واحدة من الدورة، يتم تشكيل 3 جزيئات من NADH (7.5 ATP)، وجزيء واحد من FADH 2 (1.5 ATP) وجزيء واحد من GTP، وهو ما يعادل 10 جزيئات. من اعبي التنس المحترفين. لذا، فإن 8 جزيئات من الأسيتيل-SCoA ستوفر تكوين 8 × 10 = 80 جزيئات ATP.
- لحمض البالمتيك عدد دورات الأكسدة β هو 7. في كل دورة، يتم إنتاج جزيء واحد من FADH 2 (1.5 ATP) وجزيء واحد من NADH (2.5 ATP). عند دخولهم السلسلة التنفسية، في المجموع "يعطون" 4 جزيئات ATP. وهكذا، في 7 دورات يتم تشكيل 7 × 4 = 28 جزيء ATP.
- روابط مزدوجة في حمض البالمتيك لا.
- يتم استخدام جزيء واحد من ATP لتنشيط الحمض الدهني، والذي يتحلل إلى AMP، أي أنه يتم استهلاكه 2 اتصالات ماكرورجيكأو اثنان من اعبي التنس المحترفين.
وهكذا، تلخيص، نحصل على 80+28-2 =106 تتشكل جزيئات ATP أثناء أكسدة حمض البالمتيك.
- الدوران المنتظم للسفينة حول المحور العمودي
- Tsyplenkov، Denis Ivanovich أسرار ضخ الأسلحة من D Tsyplenkov
- ما هي الدولة التي نشأت فيها صناعة الجبن المطبوخ؟
- كم يبلغ وزن قطعة سنيكرز؟
- كم درجة يجب أن تكون الفودكا؟
- أنواع وأوقات وطرق طبخ المعكرونة
- المأكولات البحرية لصحتك
- كم من الوقت لطهي شرائح الديك الرومي؟
- طريقة عمل جولاش لحم البقر مع المرق
- خبز كب كيك في المنزل في الفرن - وصفة بسيطة
- خمس قواعد لتحضير تتبيلة كبد الدجاج المثالية لكباب كبد الدجاج
- كل شيء عن مندوب واحد كحد أقصى (1RM) تحديد مندوب واحد كحد أقصى
- توازن الطاقة لأكسدة الأحماض الدهنية المشبعة مع عدد زوجي من ذرات الكربون
- قائمة الأدبيات المستخدمة الكيمياء الحيوية للنشاط العضلي
- الكيمياء الحيوية لنشاط العضلات
- غوجي التوت: الفوائد والأضرار وكيفية تناولها
- من الأحياء الفقيرة إلى الرياضة! سيرجي ميرونوف. الرياضي سيرجي ميرونوف (كمال الأجسام): السيرة الذاتية، المعلمات، السيرة الذاتية لنموذج اللياقة البدنية سيرجي ميرونوف
- مراجعة الفيديو! ميخائيل بريجونوف. مقابلة مع ميخائيل بريجونوف ما هو الانضباط الذي قمت به في ألعاب القوى؟
- تحديد الحد الأقصى لاستهلاك الأوكسجين
- رمي الكرة من مسافة بعيدة