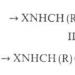டான்டலம் என்றால் என்ன, அது எங்கே பயன்படுத்தப்படுகிறது? டான்டலம் என்றால் என்ன? அம்சங்கள், தயாரிப்புகள், பண்புகள் மற்றும் பயன்பாடுகள். டான்டலம் விலை
டான்டலம் (Ta) என்பது அணு எண் 73 மற்றும் அணு எடை 180.948 கொண்ட ஒரு தனிமம் ஆகும். இது ஐந்தாவது குழுவின் இரண்டாம் துணைக்குழுவின் ஒரு உறுப்பு ஆகும், இது டிமிட்ரி இவனோவிச் மெண்டலீவின் கால அட்டவணையின் ஆறாவது காலகட்டமாகும். சாதாரண நிலைமைகளின் கீழ் இலவச நிலையில் உள்ள டான்டலம் ஒரு பிளாட்டினம்-சாம்பல் உலோகம், இது ஒரு ஆக்சைடு படம் (Ta 2 O 5) உருவாவதன் விளைவு ஆகும். டான்டலம் ஒரு கனமான, பயனற்ற, மிகவும் கடினமான, ஆனால் உடையக்கூடிய உலோகம் அல்ல, அதே நேரத்தில் இது மிகவும் இணக்கமானது, எளிதில் இயந்திரமயமாக்கப்படுகிறது, குறிப்பாக அதன் தூய வடிவத்தில்.
இயற்கையில், டான்டலம் இரண்டு ஐசோடோப்புகளின் வடிவத்தில் காணப்படுகிறது: நிலையான 181 Ta (99.99%) மற்றும் கதிரியக்க 180 Ta (0.012%) 10 12 ஆண்டுகள் அரை ஆயுளுடன். செயற்கையாக பெறப்பட்ட கதிரியக்கத்தில் 182 Ta (அரை ஆயுள் 115.1 நாட்கள்) ஐசோடோப்பு காட்டியாகப் பயன்படுத்தப்படுகிறது.
1802 ஆம் ஆண்டில் ஸ்வீடிஷ் வேதியியலாளர் A. G. Ekeberg என்பவரால் பின்லாந்து மற்றும் ஸ்வீடனில் காணப்படும் இரண்டு கனிமங்களில் இந்த தனிமம் கண்டுபிடிக்கப்பட்டது. பண்டைய கிரேக்க தொன்மங்களின் ஹீரோவை தனிமைப்படுத்துவதில் சிரமம் இருப்பதால் டான்டலஸ் என்று பெயரிடப்பட்டது. கொலம்பியம் (நியோபியம்) அடங்கிய கொலம்பைட், டான்டலம் அடங்கிய டான்டலைட் ஆகிய கனிமங்கள் நீண்ட காலமாக ஒன்றாகவே கருதப்பட்டன. எல்லாவற்றிற்கும் மேலாக, இந்த இரண்டு கூறுகளும் ஒருவருக்கொருவர் அடிக்கடி தோழர்கள் மற்றும் பல வழிகளில் ஒத்தவை. இந்த கருத்து அனைத்து நாடுகளின் வேதியியலாளர்களிடையே நீண்ட காலமாக சரியானதாகக் கருதப்பட்டது, 1844 ஆம் ஆண்டில் ஜெர்மன் வேதியியலாளர் ஹென்ரிச் ரோஸ் மீண்டும் பல்வேறு இடங்களிலிருந்து கொலம்பைட்டுகள் மற்றும் டான்டலைட்டுகளை ஆய்வு செய்தார், மேலும் அவற்றில் டான்டலத்தின் பண்புகளைப் போலவே ஒரு புதிய உலோகத்தைக் கண்டறிந்தார். அது நியோபியம். பிளாஸ்டிக் தூய உலோக டான்டலம் முதன்முதலில் ஜெர்மன் விஞ்ஞானி டபிள்யூ. வான் போல்டன் 1903 இல் பெறப்பட்டது.
டான்டலம் தாதுக்களின் முக்கிய வைப்புக்கள் பின்லாந்து, ஸ்காண்டிநேவிய நாடுகள், வட அமெரிக்கா, பிரேசில், ஆஸ்திரேலியா, பிரான்ஸ், சீனா மற்றும் பல நாடுகளில் அமைந்துள்ளன.
டான்டலம் பல மதிப்புமிக்க பண்புகளைக் கொண்டிருப்பதால் - நல்ல நீர்த்துப்போகும் தன்மை, அதிக வலிமை, பற்றவைப்பு, மிதமான வெப்பநிலையில் அரிப்பு எதிர்ப்பு, பயனற்ற தன்மை மற்றும் பல முக்கிய குணங்கள் - எழுபத்து மூன்றாவது தனிமத்தின் பயன்பாடு மிகவும் விரிவானது. டான்டலம் பயன்பாட்டின் மிக முக்கியமான பகுதிகள் மின்னணுவியல் மற்றும் இயந்திர பொறியியல் ஆகும். உலகின் டான்டலம் உற்பத்தியில் ஏறத்தாழ கால் பகுதி மின்சாரம் மற்றும் வெற்றிடத் தொழில்களுக்கு செல்கிறது. எலக்ட்ரானிக்ஸில், இது மின்னாற்பகுப்பு மின்தேக்கிகள், உயர் சக்தி விளக்குகளின் அனோட்கள் மற்றும் கட்டங்கள் ஆகியவற்றின் உற்பத்திக்கு பயன்படுத்தப்படுகிறது. இரசாயனத் தொழிலில், அமிலங்களின் உற்பத்தியில் பயன்படுத்தப்படும் இயந்திர பாகங்களை உருவாக்க டான்டலம் பயன்படுத்தப்படுகிறது, ஏனெனில் இந்த உறுப்பு விதிவிலக்கான இரசாயன எதிர்ப்பைக் கொண்டுள்ளது. அக்வா ரெஜியா போன்ற இரசாயன ஆக்கிரமிப்பு சூழலில் கூட டான்டலம் கரைவதில்லை! அரிய மண் போன்ற உலோகங்கள் டான்டலம் சிலுவைகளில் உருகுகின்றன. உயர் வெப்பநிலை உலைகளுக்கான ஹீட்டர்கள் அதிலிருந்து தயாரிக்கப்படுகின்றன. டான்டலம் மனித உடலின் உயிருள்ள திசுக்களுடன் தொடர்பு கொள்ளாது மற்றும் அவர்களுக்கு தீங்கு விளைவிப்பதில்லை என்ற உண்மையின் காரணமாக, எலும்பு முறிவுகளின் போது எலும்புகளை ஒன்றாக இணைக்க அறுவை சிகிச்சையில் பயன்படுத்தப்படுகிறது. இருப்பினும், அத்தகைய மதிப்புமிக்க உலோகத்தின் முக்கிய நுகர்வோர் உலோகம் (45% க்கு மேல்). சமீபத்திய ஆண்டுகளில், டான்டலம் அதிகளவில் சிறப்பு இரும்புகளில் ஒரு கலவை உறுப்பு பயன்படுத்தப்படுகிறது - தீவிர வலுவான, அரிப்பை எதிர்ப்பு, வெப்ப-எதிர்ப்பு. கூடுதலாக, பல கட்டமைப்பு பொருட்கள் விரைவாக வெப்ப கடத்துத்திறனை இழக்கின்றன: வெப்பத்தை மோசமாக நடத்தும் ஒரு ஆக்சைடு அல்லது உப்பு படம் அவற்றின் மேற்பரப்பில் உருவாகிறது. டான்டலம் மற்றும் அதன் உலோகக்கலவைகளால் செய்யப்பட்ட கட்டமைப்புகள் இத்தகைய சிக்கல்களை எதிர்கொள்வதில்லை. அவற்றில் உருவாகும் ஆக்சைடு படம் மெல்லியதாகவும், வெப்பத்தை நன்றாக நடத்துகிறது, மேலும் பாதுகாப்பு அரிப்பு எதிர்ப்பு பண்புகளையும் கொண்டுள்ளது.
தூய டான்டலம் மட்டும் மதிப்புமிக்கது, ஆனால் அதன் கலவைகள். இவ்வாறு, டான்டலம் கார்பைட்டின் அதிக கடினத்தன்மை உலோகத்தை அதிவேகமாக வெட்டுவதற்கான கார்பைடு கருவிகளை தயாரிப்பதில் பயன்படுத்தப்படுகிறது. டான்டலம்-டங்ஸ்டன் உலோகக்கலவைகள் அவற்றிலிருந்து தயாரிக்கப்பட்ட பகுதிகளுக்கு வெப்ப எதிர்ப்பை அளிக்கின்றன.
உயிரியல் பண்புகள்
அதன் உயர் உயிரியல் பொருந்தக்கூடிய தன்மை காரணமாக - உடலில் எரிச்சல் அல்லது நிராகரிப்பை ஏற்படுத்தாமல் உயிருள்ள திசுக்களுடன் பழகும் திறன் - டான்டலம் மருத்துவத்தில், முக்கியமாக புனரமைப்பு அறுவை சிகிச்சையில் - மனித உடலை மீட்டெடுக்க பரந்த பயன்பாட்டைக் கண்டறிந்துள்ளது. மண்டை ஓட்டின் சேதத்திற்கு டான்டலத்தின் மெல்லிய தட்டுகள் பயன்படுத்தப்படுகின்றன - அவை மண்டை ஓட்டில் உள்ள இடைவெளிகளை மூடுகின்றன. டான்டலம் தட்டில் இருந்து செயற்கைக் காது தயாரிக்கப்பட்டு, தொடையிலிருந்து இடமாற்றம் செய்யப்பட்ட தோல் மிகவும் நன்றாகவும் விரைவாகவும் வேரூன்றியது, விரைவில் செயற்கை உறுப்பை உண்மையான உறுப்புகளிலிருந்து வேறுபடுத்த முடியவில்லை என்பது மருத்துவத்திற்குத் தெரியும். சேதமடைந்த தசை திசுக்களை மீட்டெடுக்க டான்டலம் நூல்கள் பயன்படுத்தப்படுகின்றன. அறுவைசிகிச்சைக்குப் பிறகு வயிற்றுத் துவாரத்தின் சுவர்களைக் கட்டுவதற்கு அறுவை சிகிச்சை நிபுணர்கள் டான்டலம் தட்டுகளைப் பயன்படுத்துகின்றனர். டான்டலம் கிளிப்களைப் பயன்படுத்தி இரத்த நாளங்களை கூட இணைக்க முடியும். இந்த தனித்துவமான பொருளால் செய்யப்பட்ட நெட்வொர்க்குகள் கண் புரோஸ்டீஸ் தயாரிப்பில் பயன்படுத்தப்படுகின்றன. இந்த உலோகத்தால் செய்யப்பட்ட நூல்கள் தசைநாண்களை மாற்றவும் மற்றும் நரம்பு இழைகளை ஒன்றாக தைக்கவும் பயன்படுத்தப்படுகின்றன.
டான்டலம் பென்டாக்சைடு Ta 2 O 5 இன் பயன்பாடு குறைவான பரவலானது அல்ல - ஒரு சிறிய அளவு இரும்பு ட்ரை ஆக்சைடுடன் அதன் கலவையானது இரத்த உறைதலை துரிதப்படுத்த பயன்படுத்த பரிந்துரைக்கப்படுகிறது.
கடந்த தசாப்தத்தில், மனித உடலில் நேர்மறையான உயிரியல் செயல்முறைகளைத் தூண்டுவதற்கு குறுகிய தூர நிலையான மின்சார புலங்களைப் பயன்படுத்துவதன் அடிப்படையில் மருத்துவத்தின் ஒரு புதிய கிளை உருவாகி வருகிறது. மேலும், மின்சார புலங்கள், நெட்வொர்க் அல்லது பேட்டரி பவர் சப்ளை கொண்ட பாரம்பரிய மின் ஆற்றல் மூலங்களால் உருவாகவில்லை, மாறாக தன்னாட்சி முறையில் செயல்படும் எலக்ட்ரெட் பூச்சுகள் (நீண்ட காலத்திற்கு ஈடுசெய்யப்படாத மின் கட்டணத்தைத் தக்கவைக்கும் மின்கடத்தா), பல்வேறு நோக்கங்களுக்காக உள்வைப்புகளுக்குப் பயன்படுத்தப்படுகின்றன. மருத்துவத்தில் பயன்படுத்தப்படுகிறது.
தற்போது, டான்டலம் பென்டாக்சைட்டின் எலக்ட்ரெட் படங்களின் பயன்பாட்டின் நேர்மறையான முடிவுகள் மருத்துவத்தின் பின்வரும் பகுதிகளில் பெறப்பட்டுள்ளன: மாக்ஸில்லோஃபேஷியல் அறுவை சிகிச்சை (Ta 2 O 5 உடன் பூசப்பட்ட உள்வைப்புகளின் பயன்பாடு அழற்சி செயல்முறைகள் ஏற்படுவதை நீக்குகிறது மற்றும் உள்வைப்பு குணப்படுத்தும் நேரத்தை குறைக்கிறது) ; எலும்பியல் பல் மருத்துவம் (டாண்டலம் பென்டாக்சைடு படத்துடன் அக்ரிலிக் பிளாஸ்டிக்கால் செய்யப்பட்ட பூச்சுப் பற்கள் அக்ரிலேட்டுகளுக்கு சகிப்புத்தன்மையின்மையால் ஏற்படக்கூடிய அனைத்து நோயியல் வெளிப்பாடுகளையும் நீக்குகிறது); அறுவைசிகிச்சை (நீண்ட கால குணமடையாத காயம் செயல்முறைகள், பெட்ஸோர்ஸ், நியூரோட்ரோபிக் புண்கள், வெப்ப காயங்கள் ஆகியவற்றில் தோல் மற்றும் இணைப்பு திசுக்களின் குறைபாடுகளுக்கு சிகிச்சையளிப்பதில் எலக்ட்ரெட் அப்ளிகேட்டரின் பயன்பாடு); அதிர்ச்சி மற்றும் எலும்பியல் (எலக்ட்ரெட் பூச்சு படத்தால் உருவாக்கப்பட்ட நிலையான புலத்தின் செல்வாக்கின் கீழ் மனித தசைக்கூட்டு அமைப்பின் எலும்பு முறிவுகள் மற்றும் நோய்களுக்கான சிகிச்சையில் எலும்பு திசு வளர்ச்சியின் முடுக்கம்).
இந்த தனித்துவமான அறிவியல் முன்னேற்றங்கள் அனைத்தும் செயின்ட் பீட்டர்ஸ்பர்க் ஸ்டேட் எலக்ட்ரோடெக்னிகல் யுனிவர்சிட்டி (LETI) நிபுணர்களின் விஞ்ஞானப் பணிகளால் சாத்தியமானது.
மேலே பட்டியலிடப்பட்டுள்ள பகுதிகளுக்கு கூடுதலாக, தனித்துவமான டான்டாலம் பென்டாக்சைடு பூச்சுகள் ஏற்கனவே பயன்படுத்தப்பட்டு வருகின்றன அல்லது அறிமுகப்படுத்தப்படுகின்றன, அவை ஆரம்ப கட்டங்களில் உள்ளன. மருத்துவத்தின் பின்வரும் பகுதிகளுக்கான முன்னேற்றங்கள் இதில் அடங்கும்: அழகுசாதனவியல் (டான்டலம் பென்டாக்சைடு பூச்சுகளின் அடிப்படையில் ஒரு பொருளின் உற்பத்தி, இது "தங்க நூல்களை" மாற்றும்); இதய அறுவை சிகிச்சை (செயற்கை இரத்த நாளங்களின் உள் மேற்பரப்பில் எலக்ட்ரெட் படங்களைப் பயன்படுத்துதல், இரத்த உறைவு உருவாவதைத் தடுக்கிறது); எண்டோபிரோஸ்டெடிக்ஸ் (எலும்பு திசுக்களுடன் நிலையான தொடர்பு கொண்ட புரோஸ்டீஸ்களை நிராகரிக்கும் அபாயத்தைக் குறைக்கிறது). கூடுதலாக, டான்டில் பென்டாக்சைடு படம் பூசப்பட்ட ஒரு அறுவை சிகிச்சை கருவி உருவாக்கப்படுகிறது.
டான்டலம் ஆக்கிரமிப்பு சூழல்களுக்கு மிகவும் எதிர்ப்புத் தெரிவிக்கிறது, இது பல உண்மைகளால் நிரூபிக்கப்பட்டுள்ளது. எனவே 200 டிகிரி செல்சியஸ் வெப்பநிலையில் இந்த உலோகம் எழுபது சதவீத நைட்ரிக் அமிலத்தால் பாதிக்கப்படாது! 150 டிகிரி செல்சியஸ் வெப்பநிலையில் கந்தக அமிலத்தில், டான்டலம் அரிப்பைக் காண முடியாது, மேலும் 200 டிகிரி செல்சியஸ் வெப்பநிலையில் உலோகம் அரிக்கிறது, ஆனால் ஆண்டுக்கு 0.006 மிமீ மட்டுமே!
ஹைட்ரஜன் குளோரைடு வாயுவைப் பயன்படுத்திய ஒரு நிறுவனத்தில், துருப்பிடிக்காத எஃகு பாகங்கள் சில மாதங்களுக்குப் பிறகு தோல்வியடைந்ததாக அறியப்பட்ட வழக்கு உள்ளது. இருப்பினும், எஃகு டான்டலத்தால் மாற்றப்பட்டவுடன், மெல்லிய பாகங்கள் (0.3 ... 0.5 மிமீ தடிமன்) கூட நடைமுறையில் காலவரையற்றதாக மாறியது - அவற்றின் சேவை வாழ்க்கை 20 ஆண்டுகளாக அதிகரித்தது!
டான்டலம், நிக்கல் மற்றும் குரோமியத்துடன் சேர்ந்து, அரிப்பு எதிர்ப்பு பூச்சாக பரவலாகப் பயன்படுத்தப்படுகிறது. இது பலவிதமான வடிவங்கள் மற்றும் அளவுகளின் பகுதிகளை உள்ளடக்கியது: சிலுவைகள், குழாய்கள், தாள்கள், ராக்கெட் முனைகள் மற்றும் பல. மேலும், டான்டலம் பூச்சு பயன்படுத்தப்படும் பொருள் மிகவும் மாறுபட்டதாக இருக்கும்: இரும்பு, தாமிரம், கிராஃபைட், குவார்ட்ஸ், கண்ணாடி மற்றும் பிற. மிகவும் சுவாரஸ்யமான விஷயம் என்னவென்றால், டான்டலம் பூச்சுகளின் கடினத்தன்மை, தொழில்நுட்ப டான்டலத்தின் கடினத்தன்மையை விட மூன்று முதல் நான்கு மடங்கு அதிகமாக உள்ளது!
டான்டலம் மிகவும் மதிப்புமிக்க உலோகம் என்ற உண்மையின் காரணமாக, அதன் மூலப்பொருட்களுக்கான தேடல் இன்றும் தொடர்கிறது. கனிமவியலாளர்கள் சாதாரண கிரானைட்டுகள், மற்ற மதிப்புமிக்க கூறுகளுடன் கூடுதலாக, டான்டலத்தையும் கொண்டிருப்பதாகக் கண்டறிந்துள்ளனர். கிரானைட் பாறைகளிலிருந்து டான்டலத்தை பிரித்தெடுக்கும் முயற்சி பிரேசிலில் செய்யப்பட்டது, உலோகம் பெறப்பட்டது, ஆனால் அத்தகைய பிரித்தெடுத்தல் ஒரு தொழில்துறை அளவை எட்டவில்லை - செயல்முறை மிகவும் விலை உயர்ந்ததாகவும் சிக்கலானதாகவும் மாறியது.
நவீன எலக்ட்ரோலைடிக் டான்டலம் மின்தேக்கிகள் நிலையானவை, நம்பகமானவை மற்றும் நீடித்தவை. இந்த பொருளிலிருந்து தயாரிக்கப்பட்ட மினியேச்சர் மின்தேக்கிகள், பல்வேறு மின்னணு அமைப்புகளில் பயன்படுத்தப்படுகின்றன, மேலே உள்ள நன்மைகளுக்கு கூடுதலாக, ஒரு தனித்துவமான தரம் உள்ளது: அவர்கள் தங்கள் சொந்த பழுதுபார்ப்புகளை மேற்கொள்ளலாம்! இது எப்படி நடக்கிறது? மின்னழுத்த வீழ்ச்சியால் அல்லது வேறு காரணத்தால் இன்சுலேஷனின் ஒருமைப்பாடு சேதமடைந்ததாக வைத்துக்கொள்வோம் - முறிவு ஏற்பட்ட இடத்தில் உடனடியாக ஒரு இன்சுலேடிங் ஆக்சைடு படம் உருவாகிறது, மேலும் மின்தேக்கி எதுவும் நடக்காதது போல் தொடர்ந்து செயல்படுகிறது!
சந்தேகத்திற்கு இடமின்றி, 20 ஆம் நூற்றாண்டின் நடுப்பகுதியில் தோன்றிய "ஸ்மார்ட் மெட்டல்", அதாவது ஸ்மார்ட் இயந்திரங்கள் செயல்பட உதவும் ஒரு உலோகம், டான்டலத்திற்கு சரியாக ஒதுக்கப்படலாம்.
சில பகுதிகளில், டான்டலம் மாற்றுகிறது மற்றும் சில நேரங்களில் பிளாட்டினத்துடன் போட்டியிடுகிறது! இவ்வாறு, நகை வேலைகளில், வளையல்கள், வாட்ச் கேஸ்கள் மற்றும் பிற நகைகளை தயாரிப்பதில் டான்டலம் பெரும்பாலும் விலை உயர்ந்த உன்னத உலோகத்தை மாற்றுகிறது. மற்றொரு பகுதியில், டான்டலம் வெற்றிகரமாக பிளாட்டினத்துடன் போட்டியிடுகிறது - இந்த உலோகத்தால் செய்யப்பட்ட நிலையான பகுப்பாய்வு நிலுவைகள் பிளாட்டினத்தை விட தரத்தில் தாழ்ந்தவை அல்ல.
கூடுதலாக, தானியங்கு பேனாக்களுக்கான நிப்ஸ் தயாரிப்பில் அதிக விலை கொண்ட இரிடியத்தை டான்டலம் மாற்றுகிறது.
அதன் தனித்துவமான வேதியியல் பண்புகள் காரணமாக, டான்டலம் கேத்தோட்களுக்கான ஒரு பொருளாக பயன்பாட்டைக் கண்டறிந்துள்ளது. இவ்வாறு, தங்கம் மற்றும் வெள்ளியை மின்னாற்பகுப்பு முறையில் பிரிப்பதில் டான்டலம் கத்தோட்கள் பயன்படுத்தப்படுகின்றன. உன்னத உலோகங்களின் வண்டலை அக்வா ரெஜியா மூலம் கழுவ முடியும் என்பதில் அவற்றின் மதிப்பு உள்ளது, இது டான்டலத்திற்கு தீங்கு விளைவிக்காது.
ஸ்வீடிஷ் வேதியியலாளர் எக்பெர்க், ஒரு புதிய பொருளை அமிலங்களுடன் நிறைவு செய்ய முயற்சிக்கும்போது, அதன் "தாகத்தால்" தாக்கப்பட்டு, புதிய உறுப்புக்கு ஒரு பெயரைக் கொடுத்தார் என்பதில், ஏதோ ஒரு குறியீட்டு, மர்மம் இல்லை என்ற உண்மையைப் பற்றி ஒருவர் நிச்சயமாகப் பேசலாம். தனது சொந்த மகனைக் கொன்று கடவுளைக் காட்டிக் கொடுத்த புராண வில்லனின் மரியாதை. இருநூறு ஆண்டுகளுக்குப் பிறகு, இந்த உறுப்பு ஒரு நபரை உண்மையில் "தையல்" செய்யக்கூடியது மற்றும் அவரது தசைநாண்கள் மற்றும் நரம்புகளை "மாற்றும்" திறன் கொண்டது என்று மாறியது! தியாகி, பாதாள உலகில் தவித்து, மனிதனுக்கு உதவுவதன் மூலம் தனது குற்றத்திற்கு பரிகாரம் செய்து, கடவுளிடம் மன்னிப்பு கேட்க முயற்சிக்கிறார்.
கதை
டான்டலஸ் பண்டைய கிரேக்க புராணங்களின் ஹீரோ, லிடியன் அல்லது ஃபிரிஜியன் மன்னர், ஜீயஸின் மகன். அவர் ஒலிம்பியன் கடவுள்களின் ரகசியங்களை வெளிப்படுத்தினார், அவர்களின் விருந்தில் இருந்து அம்ப்ரோசியாவைத் திருடி, ஒலிம்பியன்களுக்கு அவர் கொன்ற தனது சொந்த மகன் பெலோப்ஸின் உடலில் இருந்து தயாரிக்கப்பட்ட உணவை வழங்கினார். அவரது அட்டூழியங்களுக்காக, டான்டலஸ் பாதாள உலகில் பசி, தாகம் மற்றும் பயத்தின் நித்திய வேதனைக்கு கடவுள்களால் தண்டனை விதிக்கப்பட்டார். அப்போதிருந்து, அவர் தனது கழுத்து வரை வெளிப்படையான படிக தெளிவான நீரில் நிற்கிறார், பழுத்த பழங்களின் எடையின் கீழ் கிளைகள் அவரது தலையை நோக்கி வளைந்தன. அவனால் மட்டுமே தாகம் அல்லது பசியைத் தணிக்க முடியாது - அவர் குடிக்க முயற்சித்தவுடன் தண்ணீர் கீழே செல்கிறது, மற்றும் கிளைகள் ஒரு பசி கொலையாளியின் கைகளிலிருந்து காற்றால் தூக்கி எறியப்படுகின்றன. டான்டலஸின் தலைக்கு மேல் ஒரு பாறை தொங்குகிறது, அது எந்த நேரத்திலும் இடிந்து விழும், துரதிர்ஷ்டவசமான பாவியை என்றென்றும் பயத்தில் தள்ளுகிறது. இந்த கட்டுக்கதைக்கு நன்றி, "டாண்டலமின் வேதனை" என்ற வெளிப்பாடு எழுந்தது, தாங்க முடியாத துன்பங்களைக் குறிக்கிறது, வேதனையிலிருந்து தன்னை விடுவித்துக் கொள்ள முயற்சிக்கிறது. வெளிப்படையாக, 1802 ஆம் ஆண்டில் அவர் கண்டுபிடித்த "பூமியை" அமிலங்களில் கரைத்து அதிலிருந்து ஒரு புதிய உறுப்பை தனிமைப்படுத்த ஸ்வீடிஷ் வேதியியலாளர் எகெபெர்க்கின் தோல்வியுற்ற முயற்சிகளின் போது, இந்த வெளிப்பாடுதான் அவரது நினைவுக்கு வந்தது. ஒன்றுக்கு மேற்பட்ட முறை விஞ்ஞானி தனது இலக்கை நெருங்கிவிட்டதாக நினைத்தார், ஆனால் புதிய உலோகத்தை அதன் தூய வடிவில் தனிமைப்படுத்த முடியவில்லை. புதிய தனிமத்தின் "தியாகி" பெயர் தோன்றியது இப்படித்தான்.
டான்டலத்தின் கண்டுபிடிப்பு மற்றொரு தனிமத்தின் கண்டுபிடிப்புடன் நெருங்கிய தொடர்புடையது - நியோபியம், இது ஒரு வருடம் முன்பு பிறந்தது மற்றும் முதலில் கொலம்பியா என்று பெயரிடப்பட்டது, இது அதன் கண்டுபிடிப்பாளர் ஹாட்செட்டால் வழங்கப்பட்டது. இந்த உறுப்பு டான்டலத்தின் இரட்டை மற்றும் பல பண்புகளில் அதனுடன் நெருக்கமாக உள்ளது. இந்த அருகாமையே வேதியியலாளர்களை தவறாக வழிநடத்தியது, அவர்கள் பல விவாதங்களுக்குப் பிறகு, டான்டலமும் கொலம்பியமும் ஒரே உறுப்பு என்ற தவறான முடிவுக்கு வந்தனர். இந்த தவறான கருத்து நாற்பது ஆண்டுகளுக்கும் மேலாக நீடித்தது, 1844 ஆம் ஆண்டில் புகழ்பெற்ற ஜெர்மன் வேதியியலாளர் ஹென்ரிச் ரோஸ், பல்வேறு வைப்புகளிலிருந்து கொலம்பைட்டுகள் மற்றும் டான்டலைட்டுகள் பற்றிய தொடர்ச்சியான ஆய்வின் போது, கொலம்பியம் ஒரு சுயாதீனமான உறுப்பு என்பதை நிரூபித்தார். கேட்செட் ஆய்வு செய்த கொலம்பியாவில் அதிக டான்டலம் உள்ளடக்கம் கொண்ட நியோபியம் இருந்தது, இது விஞ்ஞான உலகத்தை தவறாக வழிநடத்தியது. இரண்டு கூறுகளுக்கும் இடையிலான அத்தகைய நெருங்கிய உறவின் நினைவாக, ரோஸ் கொலம்பியாவுக்கு நியோபியம் என்ற புதிய பெயரைக் கொடுத்தார் - ஃபிரிஜியன் மன்னர் டான்டலஸ் நியோபியாவின் மகளின் நினைவாக. ரோஸ் மற்றொரு புதிய தனிமத்தைக் கண்டுபிடித்ததாகக் கூறப்படும் தவறைச் செய்திருந்தாலும், அதற்கு அவர் பெலோபியஸ் (டான்டலஸின் மகன் பெலோப்ஸின் பெயர்) என்று பெயரிட்டார், அவருடைய பணி நியோபியம் (கொலம்பியம்) மற்றும் டான்டலம் இடையே கடுமையான வேறுபாட்டிற்கு அடிப்படையாக அமைந்தது. ரோஸின் சான்றுகளுக்குப் பிறகும், டான்டலம் மற்றும் நியோபியம் ஆகியவை நீண்ட காலமாக குழப்பமடைந்தன. எனவே டான்டலம் கொலம்பியம் என்று அழைக்கப்பட்டது, ரஷ்யாவில் கொலம்பஸ். ஹெஸ், அதன் ஆறாவது பதிப்பு (1845) வரை அவரது "தூய வேதியியலின் கோட்பாடுகள்" இல் கொலம்பியாவைக் குறிப்பிடாமல், டான்டலம் பற்றி மட்டுமே பேசுகிறார்; Dvigubsky (1824) டான்டாலியம் என்ற பெயரைக் குறிப்பிடுகிறார். இத்தகைய பிழைகள் மற்றும் முன்பதிவுகள் புரிந்துகொள்ளத்தக்கவை - டான்டலம் மற்றும் நியோபியத்தை பிரிப்பதற்கான முறை 1866 ஆம் ஆண்டில் சுவிஸ் வேதியியலாளர் மரிக்னாக் என்பவரால் உருவாக்கப்பட்டது, மேலும் அத்தகைய தூய தனிம டான்டலம் இன்னும் இல்லை: எல்லாவற்றிற்கும் மேலாக, விஞ்ஞானிகள் இந்த உலோகத்தை அதன் தூய கச்சிதமாகப் பெற முடிந்தது. 20 ஆம் நூற்றாண்டில் மட்டுமே வடிவம். டான்டலம் உலோகத்தை முதன்முதலில் பெற முடிந்தது ஜெர்மன் வேதியியலாளர் வான் போல்டன், இது 1903 இல் மட்டுமே நடந்தது. முன்னதாக, நிச்சயமாக, தூய டான்டலம் உலோகத்தைப் பெறுவதற்கான முயற்சிகள் மேற்கொள்ளப்பட்டன, ஆனால் வேதியியலாளர்களின் அனைத்து முயற்சிகளும் தோல்வியடைந்தன. எடுத்துக்காட்டாக, பிரெஞ்சு வேதியியலாளர் மொய்சான் ஒரு உலோக தூளைப் பெற்றார், இது தூய டான்டலம் என்று அவர் கூறினார். இருப்பினும், மின்சார உலைகளில் கார்பனுடன் டான்டலம் பென்டாக்சைடு Ta 2 O 5 ஐக் குறைப்பதன் மூலம் பெறப்பட்ட இந்த தூள் தூய டான்டலம் அல்ல; தூளில் 0.5% கார்பன் இருந்தது.
இதன் விளைவாக, எழுபத்து மூன்றாம் தனிமத்தின் இயற்பியல் வேதியியல் பண்புகள் பற்றிய விரிவான ஆய்வு இருபதாம் நூற்றாண்டின் தொடக்கத்தில் மட்டுமே சாத்தியமானது. இன்னும் பல ஆண்டுகளாக, டான்டலம் நடைமுறைப் பயன்பாட்டைக் காணவில்லை. 1922 இல் மட்டுமே ஏசி ரெக்டிஃபையர்களில் இதைப் பயன்படுத்த முடிந்தது.
இயற்கையில் இருப்பது
பூமியின் மேலோட்டத்தில் (கிளார்க்) எழுபத்து மூன்றாவது தனிமத்தின் சராசரி உள்ளடக்கம் 2.5∙10 -4% நிறை. டான்டலம் என்பது அமிலப் பாறைகளின் ஒரு சிறப்பியல்பு உறுப்பு - கிரானைட் மற்றும் வண்டல் ஓடுகள், இதில் அதன் சராசரி உள்ளடக்கம் 3.5∙10 -4% அடையும், அல்ட்ராபேசிக் மற்றும் அடிப்படை பாறைகள் - மேலோட்டத்தின் மேல் பகுதிகள் மற்றும் பூமியின் மேலோட்டத்தின் ஆழமான பகுதிகள், டான்டலத்தின் செறிவு மிகவும் குறைவாக உள்ளது: 1 .8∙10 -6%. டான்டலம் பற்றவைக்கப்பட்ட பாறைகளிலும், உயிர்க்கோளத்திலும் சிதறிக்கிடக்கிறது, ஏனெனில் இது பல வேதியியல் கூறுகளுடன் ஐசோமார்பிக் ஆகும்.
பூமியின் மேலோட்டத்தில் டான்டலத்தின் குறைந்த உள்ளடக்கம் இருந்தபோதிலும், அதன் தாதுக்கள் மிகவும் பரவலாக உள்ளன - அவற்றில் நூற்றுக்கும் மேற்பட்டவை உள்ளன, டான்டலம் தாதுக்கள் மற்றும் டான்டலம் கொண்ட தாதுக்கள், அவை அனைத்தும் மாக்மடிக் செயல்பாடு தொடர்பாக உருவாகின்றன (டான்டலைட், கொலம்பைட், லோபரைட், பைரோகுளோர் மற்றும் பிற). அனைத்து தாதுக்களிலும், டான்டலத்தின் துணை நியோபியம் ஆகும், இது தனிமங்களின் தீவிர இரசாயன ஒற்றுமை மற்றும் அவற்றின் அயனிகளின் கிட்டத்தட்ட ஒரே மாதிரியான அளவுகளால் விளக்கப்படுகிறது.
டான்டலம் தாதுக்கள் Ta 2 O 5: Nb 2 O 5 ≥1 என்ற விகிதத்தைக் கொண்டுள்ளன. டான்டலம் தாதுக்களின் முக்கிய தாதுக்கள் கொலம்பைட்-டான்டலைட் (Ta 2 O 5 உள்ளடக்கம் 30-45%), டான்டலைட் மற்றும் மாங்கனோடான்டலிட் (Ta 2 O 5 45-80%), வோட்ஜினைட் (Ta, Mn, Sn) 3 O 6 (Ta 2 O 5 60-85%), மைக்ரோலைட் Ca 2 (Ta, Nb) 2 O 6 (F, OH) (Ta 2 O 5 50-80%) மற்றும் பிற. டான்டலைட் (Fe, Mn)(Ta, Nb) 2 O 6 பல வகைகளைக் கொண்டுள்ளது: ஃபெரோடான்டலைட் (FeO>MnO), மாங்கனோடான்டலிட் (MnO>FeO). டான்டலைட் கருப்பு முதல் சிவப்பு-பழுப்பு வரை வெவ்வேறு நிழல்களில் வருகிறது. டான்டலம்-நியோபியம் தாதுக்களின் முக்கிய தாதுக்கள், அதிலிருந்து, நியோபியத்துடன், அதிக விலை கொண்ட டான்டலம் பிரித்தெடுக்கப்படுகிறது, கொலம்பைட் (Ta 2 O 5 5-30%), டான்டலம் கொண்ட பைரோகுளோர் (Ta 2 O 5 1-4%) , லோபரைட் (Ta 2 O 5 0.4-0.8%), கேட்செட்டோலைட் (Ca, Tr, U) 2 (Nb, Ta) 2 O 6 (F, OH)∙nH 2 O (Ta 2 O 5 8-28%), ixiolite (Nb , Ta, Sn, W, Sc) 3 O 6 மற்றும் சில. U, Th, TR ஆகியவற்றைக் கொண்ட டான்டலம்-நியோபேட்டுகள் மெட்டாமிக்ட், அதிக கதிரியக்க மற்றும் மாறி அளவு தண்ணீரைக் கொண்டிருக்கின்றன; பாலிமார்பிக் மாற்றங்கள் பொதுவானவை. டான்டலம்-நியோபேட்டுகள் சிறிய பரவல்களை உருவாக்குகின்றன, பெரிய ஒதுக்கீடுகள் அரிதானவை (படிகங்கள் முக்கியமாக லோபரைட், பைரோகுளோர் மற்றும் கொலம்பைட்-டான்டலைட்டுக்கு பொதுவானவை). நிறம் கருப்பு, அடர் பழுப்பு, பழுப்பு-மஞ்சள். பொதுவாக ஒளிஊடுருவக்கூடியது அல்லது சற்று ஒளிஊடுருவக்கூடியது.
டான்டலம் தாது வைப்புகளில் பல முக்கிய தொழில்துறை மற்றும் மரபணு வகைகள் உள்ளன. நாட்ரோ-லித்தியம் வகையின் அரிய-உலோக பெக்மாடைட்டுகள் அல்பைட், மைக்ரோக்லைன், குவார்ட்ஸ் மற்றும் குறைந்த அளவிற்கு, ஸ்போடுமீன் அல்லது பெடலைட் ஆகியவற்றைக் கொண்ட மண்டல நரம்பு உடல்களால் குறிப்பிடப்படுகின்றன. அரிய-உலோக டான்டலம்-தாங்கி கிரானைட்டுகள் (அபோகிரானைட்டுகள்) சிறிய பங்குகள் மற்றும் மைக்ரோக்லைன்-குவார்ட்ஸ்-ஆல்பைட் கிரானைட்களின் குவிமாடங்களால் குறிப்பிடப்படுகின்றன, அவை பெரும்பாலும் புஷ்பராகம் மற்றும் லித்தியம் மைக்காக்களால் செறிவூட்டப்பட்ட கொலம்பைட்-டான்டலைட் மற்றும் மைக்ரோலைட் ஆகியவற்றின் மெல்லிய பரவலைக் கொண்டுள்ளன. பெக்மாடைட்டுகளின் அழிவு தொடர்பாக எழும் வானிலை மேலோடுகள், டெலுவியல்-வண்டல் மற்றும் வண்டல் பிளேசர்கள் கொலம்பைட்-டான்டலைட் குழுவின் காசிடரைட் மற்றும் தாதுக்களைக் கொண்டிருக்கின்றன. லுஜாவ்ரைட் மற்றும் ஃபோயலைட் கலவையின் லோபரைட்-தாங்கி நெஃபெலின் சைனைட்டுகள்.
கூடுதலாக, சிக்கலான டான்டலம்-நியோபியம் தாதுக்களின் வைப்புக்கள், கார்பனாடைட்டுகள் மற்றும் அதனுடன் தொடர்புடைய ஃபார்ஸ்டரைட்-அபாடைட்-மேக்னடைட் பாறைகளால் குறிப்பிடப்படுகின்றன, அவை தொழில்துறை பயன்பாட்டில் ஈடுபட்டுள்ளன; மைக்ரோக்லைன்-ஆல்பைட் ரைபெக்கைட் அல்கலைன் கிரானைட்டுகள் மற்றும் கிரானோசைனைட்டுகள் மற்றும் பிற. சில டான்டலம் கிரீசன் வைப்புகளில் இருந்து வால்ஃப்ரேமைட்டுகளில் இருந்து பிரித்தெடுக்கப்படுகிறது.
டைட்டானியம் தாதுக்களின் மிகப்பெரிய வைப்பு கனடா (மனிடோபா, பெர்னிக் ஏரி), ஆஸ்திரேலியா (கிரீன்புஷ்ஸ், பில்பரா), மலேசியா மற்றும் தாய்லாந்து (டான்டலம்-தாங்கும் டின் பிளேசர்கள்), பிரேசில் (பரைபா, ரியோ கிராண்டே டோ நோர்டே) மற்றும் பல ஆப்பிரிக்க நாடுகளில் உள்ளன. மாநிலங்கள் (ஜைர், நைஜீரியா, தெற்கு ரோடீசியா).
விண்ணப்பம்
டான்டலம் அதன் தொழில்நுட்ப பயன்பாட்டை மிகவும் தாமதமாகக் கண்டறிந்தது - 20 ஆம் நூற்றாண்டின் தொடக்கத்தில் இது மின் விளக்குகளின் ஒளிரும் இழைகளுக்கு ஒரு பொருளாகப் பயன்படுத்தப்பட்டது, இது இந்த உலோகத்தின் தரம், அதாவது பயனற்ற தன்மை போன்றது. இருப்பினும், இது விரைவில் இந்த பகுதியில் அதன் முக்கியத்துவத்தை இழந்தது, குறைந்த விலை மற்றும் அதிக பயனற்ற டங்ஸ்டனால் மாற்றப்பட்டது. 20 ஆம் நூற்றாண்டின் இருபதுகள் வரை டான்டலம் மீண்டும் "தொழில்நுட்ப ரீதியாக பொருத்தமற்றது" ஆனது, இது மாற்று மின்னோட்ட திருத்திகளில் (டான்டலம், ஆக்சைடு படத்துடன் பூசப்பட்ட, ஒரே ஒரு திசையில் மின்னோட்டத்தை கடக்கிறது) மற்றும் ஒரு வருடம் கழித்து - ரேடியோ குழாய்களில் பயன்படுத்தத் தொடங்கியது. . அதன் பிறகு உலோகம் அங்கீகாரம் பெற்றது மற்றும் விரைவில் தொழில்துறையின் மேலும் மேலும் புதிய பகுதிகளை கைப்பற்றத் தொடங்கியது.
இப்போதெல்லாம், அதன் தனித்துவமான பண்புகள் காரணமாக, டான்டலம் மின்னணுவியலில் பயன்படுத்தப்படுகிறது (அதிக குறிப்பிட்ட கொள்ளளவு கொண்ட மின்தேக்கிகளின் உற்பத்தி). உலகின் டான்டலம் உற்பத்தியில் நான்கில் ஒரு பங்கு மின்சாரம் மற்றும் வெற்றிடத் தொழில்களுக்கு செல்கிறது. டான்டலம் மற்றும் அதன் ஆக்சைடு பிலிம் இரண்டின் அதிக இரசாயன செயலற்ற தன்மை காரணமாக, எலக்ட்ரோலைடிக் டான்டலம் மின்தேக்கிகள் செயல்பாட்டில் மிகவும் நிலையானவை, நம்பகமானவை மற்றும் நீடித்தவை: அவற்றின் சேவை வாழ்க்கை பன்னிரண்டு ஆண்டுகளுக்கு மேல் அடையும். ரேடியோ பொறியியலில், ரேடார் கருவிகளில் டான்டலம் பயன்படுத்தப்படுகிறது. டான்டலம் மினி மின்தேக்கிகள் ரேடியோ டிரான்ஸ்மிட்டர்கள், ரேடார் நிறுவல்கள் மற்றும் பிற மின்னணு அமைப்புகளில் பயன்படுத்தப்படுகின்றன.
டான்டலத்தின் முக்கிய நுகர்வோர் உலோகம் ஆகும், இது உற்பத்தி செய்யப்படும் உலோகத்தில் 45% க்கும் அதிகமானவற்றைப் பயன்படுத்துகிறது. டான்டலம் சிறப்பு இரும்புகளில் ஒரு கலவை உறுப்பு என தீவிரமாக பயன்படுத்தப்படுகிறது - தீவிர வலுவான, அரிப்பை எதிர்க்கும், வெப்ப-எதிர்ப்பு. வழக்கமான குரோமியம் இரும்புகளுடன் இந்த உறுப்பு சேர்ப்பது அவற்றின் வலிமையை அதிகரிக்கிறது மற்றும் கடினப்படுத்துதல் மற்றும் அனீலிங் செய்த பிறகு உடையக்கூடிய தன்மையைக் குறைக்கிறது. வெப்ப-எதிர்ப்பு உலோகக்கலவைகளின் உற்பத்தி ராக்கெட் மற்றும் விண்வெளி தொழில்நுட்பத்திற்கு பெரும் தேவை. அரிப்பை (லித்தியம் அல்லது சோடியம்) ஏற்படுத்தும் திரவ உலோகத்தால் ராக்கெட் முனைகள் குளிர்விக்கப்படும் சந்தர்ப்பங்களில், டான்டலம்-டங்ஸ்டன் அலாய் இல்லாமல் செய்ய இயலாது. கூடுதலாக, உயர் வெப்பநிலை வெற்றிட உலைகள், ஹீட்டர்கள் மற்றும் கலவைகளுக்கான ஹீட்டர்கள் வெப்ப-எதிர்ப்பு இரும்புகளிலிருந்து தயாரிக்கப்படுகின்றன. டான்டலம் கார்பைடு (உருகுநிலை 3,880 °C) கடினமான உலோகக்கலவைகள் (டங்ஸ்டன் மற்றும் டான்டலம் கார்பைடுகளின் கலவைகள் - TT குறியீட்டுடன் கூடிய தரங்கள், உலோக வேலைப்பாடு மற்றும் சுழலும் தாக்கம் ஆகியவற்றின் மிகவும் கடினமான நிலைமைகளுக்கு வலுவான பொருட்கள் (கல், கலவைகள்) உற்பத்தியில் பயன்படுத்தப்படுகிறது. )
டான்டலத்துடன் கலந்த இரும்புகள் பரவலாகப் பயன்படுத்தப்படுகின்றன, உதாரணமாக இரசாயனப் பொறியியலில். எல்லாவற்றிற்கும் மேலாக, அத்தகைய உலோகக்கலவைகள் விதிவிலக்கான இரசாயன எதிர்ப்பைக் கொண்டுள்ளன, அவை நீர்த்துப்போகும், வெப்ப-எதிர்ப்பு மற்றும் வெப்பத்தை எதிர்க்கும்; இந்த பண்புகளுக்கு நன்றி, டான்டலம் இரசாயனத் தொழிலுக்கு ஒரு தவிர்க்க முடியாத கட்டமைப்பு பொருளாக மாறியுள்ளது. ஹைட்ரோகுளோரிக், சல்பூரிக், நைட்ரிக், பாஸ்போரிக், அசிட்டிக், அத்துடன் புரோமின், குளோரின் மற்றும் ஹைட்ரஜன் பெராக்சைடு: பல அமிலங்களின் உற்பத்தியில் டான்டலம் உபகரணங்கள் பயன்படுத்தப்படுகின்றன. சுருள்கள், டிஸ்டில்லர்கள், வால்வுகள், மிக்சர்கள், ஏரேட்டர்கள் மற்றும் இரசாயன எந்திரத்தின் பல பாகங்கள் அதிலிருந்து தயாரிக்கப்படுகின்றன. சில நேரங்களில் - முழு சாதனங்கள். தங்கம் மற்றும் வெள்ளியை மின்னாற்பகுப்பு முறையில் பிரிப்பதில் டான்டலம் கத்தோட்கள் பயன்படுத்தப்படுகின்றன. இந்த கேத்தோட்களின் நன்மை என்னவென்றால், தங்கம் மற்றும் வெள்ளி வைப்புகளை அக்வா ரெஜியா மூலம் கழுவலாம், இது டான்டலத்திற்கு தீங்கு விளைவிக்காது.
கூடுதலாக, டான்டலம் கருவி தயாரிப்பில் பயன்படுத்தப்படுகிறது (எக்ஸ்-ரே உபகரணங்கள், கட்டுப்பாட்டு கருவிகள், உதரவிதானங்கள்); மருத்துவத்தில் (புனரமைப்பு அறுவை சிகிச்சைக்கான பொருள்); அணுசக்தியில் - அணுசக்தி அமைப்புகளுக்கான வெப்பப் பரிமாற்றியாக (டான்டலம் அனைத்து உலோகங்களிலும் சூப்பர் ஹீட் உருகும் மற்றும் சீசியம்-133 நீராவிகளில் மிகவும் நிலையானது). அதிக வெற்றிடத்தை (மின்சார வெற்றிட சாதனங்கள்) பராமரிக்க, வாயுக்களை உறிஞ்சும் டான்டலத்தின் உயர் திறன் பயன்படுத்தப்படுகிறது.
சமீபத்திய ஆண்டுகளில், டான்டலம் ஒரு நகைப் பொருளாகப் பயன்படுத்தப்படுகிறது, ஏனெனில் மேற்பரப்பில் எந்த நிறத்திலும் நீடித்த ஆக்சைடு படங்களை உருவாக்கும் திறன் உள்ளது.
டான்டலம் கலவைகளும் பரவலாகப் பயன்படுத்தப்படுகின்றன. காமா கதிர்வீச்சை உறிஞ்சும் கண்ணாடியை உருகுவதற்கு அணு தொழில்நுட்பத்தில் டான்டலம் பென்டாக்சைடு பயன்படுத்தப்படுகிறது. பொட்டாசியம் புளோரோடான்டலேட் செயற்கை ரப்பர் உற்பத்தியில் வினையூக்கியாகப் பயன்படுத்தப்படுகிறது. எத்தில் ஆல்கஹாலில் இருந்து பியூடாடீனை உற்பத்தி செய்யும் போது டான்டலம் பென்டாக்சைடும் அதே பாத்திரத்தை வகிக்கிறது.
உற்பத்தி
டான்டலம் கொண்ட தாதுக்கள் இந்த தனிமத்தில் அரிதானவை மற்றும் மோசமானவை என்று அறியப்படுகிறது. டான்டலம் மற்றும் அதன் உலோகக்கலவைகளின் உற்பத்திக்கான முக்கிய மூலப்பொருட்கள் டான்டலைட் மற்றும் லோபரைட் செறிவுகள் 8% Ta 2 O 5 மற்றும் 60% Nb 2 O 5 க்கும் அதிகமானவை. கூடுதலாக, நூறில் ஒரு சதவிகிதம் (Ta, Nb) 2 O 5 உள்ள தாதுக்கள் கூட செயலாக்கப்படுகின்றன!
டான்டலம் உற்பத்தி தொழில்நுட்பம் மிகவும் சிக்கலானது மற்றும் மூன்று நிலைகளில் மேற்கொள்ளப்படுகிறது: திறப்பு அல்லது சிதைவு; நியோபியத்திலிருந்து டான்டலத்தை பிரித்து அவற்றின் தூய இரசாயன சேர்மங்களைப் பெறுதல்; டான்டலத்தின் மீட்பு மற்றும் சுத்திகரிப்பு.
டான்டலம் செறிவைத் திறப்பது, வேறுவிதமாகக் கூறினால், தாதுக்களிலிருந்து டான்டலத்தை பிரித்தெடுப்பது அல்கலிஸ் (இணைவு) அல்லது ஹைட்ரோஃப்ளூரிக் அமிலம் (சிதைவு) அல்லது ஹைட்ரோஃப்ளூரிக் மற்றும் சல்பூரிக் அமிலங்களின் கலவையைப் பயன்படுத்தி மேற்கொள்ளப்படுகிறது. அதன் பிறகு அவை உற்பத்தியின் இரண்டாம் கட்டத்திற்கு செல்கின்றன - பிரித்தெடுத்தல் மற்றும் டான்டலம் மற்றும் நியோபியம் பிரித்தல். இந்த உலோகங்களின் வேதியியல் பண்புகளின் ஒற்றுமை மற்றும் அவற்றின் அயனிகளின் கிட்டத்தட்ட ஒரே அளவு காரணமாக கடைசி பணி மிகவும் கடினம். சமீப காலம் வரை, 1866 ஆம் ஆண்டில் சுவிஸ் வேதியியலாளர் மாரிக்னாக் முன்மொழியப்பட்ட முறையால் மட்டுமே உலோகங்கள் பிரிக்கப்பட்டன, அவர் நீர்த்த ஹைட்ரோஃப்ளூரிக் அமிலத்தில் பொட்டாசியம் ஃப்ளோரோடான்டலேட் மற்றும் பொட்டாசியம் ஃப்ளோரோனியோபேட் ஆகியவற்றின் வெவ்வேறு கரைதிறனைப் பயன்படுத்திக் கொண்டார். டான்டலம் மற்றும் நியோபியத்தை பிரிப்பதற்கு நவீன தொழில்துறை பல முறைகளைப் பயன்படுத்துகிறது: கரிம கரைப்பான்கள் மூலம் பிரித்தெடுத்தல், நியோபியம் பென்டாக்ளோரைடு தேர்ந்தெடுக்கப்பட்ட குறைப்பு, சிக்கலான ஃவுளூரைடு உப்புகளின் பகுதியளவு படிகமாக்கல், அயன் பரிமாற்ற பிசின்களைப் பயன்படுத்தி பிரித்தல், குளோரைடுகளை சரிசெய்தல். தற்போது, மிகவும் பொதுவாகப் பயன்படுத்தப்படும் பிரிப்பு முறை (இது மிகவும் மேம்பட்டது) ஹைட்ரோஃப்ளூரிக் மற்றும் சல்பூரிக் அமிலங்களைக் கொண்ட டான்டலம் மற்றும் நியோபியம் ஃவுளூரைடு கலவைகளின் தீர்வுகளிலிருந்து பிரித்தெடுத்தல் ஆகும். அதே நேரத்தில், டான்டலம் மற்றும் நியோபியம் மற்ற உறுப்புகளின் அசுத்தங்களிலிருந்தும் சுத்திகரிக்கப்படுகின்றன: சிலிக்கான், டைட்டானியம், இரும்பு, மாங்கனீசு மற்றும் பிற தொடர்புடைய கூறுகள். லோபரைட் தாதுக்களைப் பொறுத்தவரை, அவற்றின் செறிவுகள் குளோரின் முறையைப் பயன்படுத்தி டான்டலம் மற்றும் நியோபியம் குளோரைடுகளின் மின்தேக்கியை உருவாக்குகின்றன, அவை மேலும் திருத்தம் மூலம் பிரிக்கப்படுகின்றன. குளோரைடுகளின் கலவையைப் பிரிப்பது பின்வரும் நிலைகளைக் கொண்டுள்ளது: பூர்வாங்க சரிசெய்தல் (டன்டலம் மற்றும் நியோபியம் குளோரைடுகளை அசுத்தங்களிலிருந்து பிரித்தல்), முக்கிய திருத்தம் (தூய்மையான NbCl 5 மற்றும் TaCl 5 செறிவுகளைப் பெற) மற்றும் டான்டலம் பின்னத்தின் இறுதி திருத்தம் (இதற்கு தூய TaCl 5) பெறவும். தொடர்புடைய உலோகங்களைப் பிரித்ததைத் தொடர்ந்து, டான்டலம் கட்டம் துரிதப்படுத்தப்பட்டு சுத்திகரிக்கப்பட்டு, பொட்டாசியம் புளோரோடான்டலேட் அதிகரித்த தூய்மையின் (KCl ஐப் பயன்படுத்தி) உற்பத்தி செய்யப்படுகிறது.
டான்டலம் உலோகம் அதன் உயர் தூய்மை சேர்மங்களைக் குறைப்பதன் மூலம் பெறப்படுகிறது, இதற்காக பல முறைகளைப் பயன்படுத்தலாம். இது 1800-2000 டிகிரி செல்சியஸ் வெப்பநிலையில் பென்டாக்சைடிலிருந்து டான்டாலத்தைக் குறைப்பது (கார்போதெர்மிக் முறை), அல்லது சூடாக்கும்போது சோடியத்துடன் பொட்டாசியம் ஃப்ளோரோடான்டலேட்டைக் குறைப்பது (சோடியம் வெப்ப முறை), அல்லது பொட்டாசியம் ஃப்ளோரோட்டாமேட் கொண்ட உருகலில் இருந்து மின் வேதியியல் குறைப்பு. மற்றும் டான்டலம் ஆக்சைடு (எலக்ட்ரோலைடிக் முறை). ஒரு வழி அல்லது வேறு, உலோகம் 98-99% தூய்மையுடன் தூள் வடிவில் பெறப்படுகிறது. இங்காட்களில் உலோகத்தைப் பெறுவதற்காக, அது தூளில் இருந்து முன் சுருக்கப்பட்ட பில்லெட்டுகளின் வடிவத்தில் சின்டர் செய்யப்படுகிறது. 2,500-2,700 டிகிரி செல்சியஸ் வெப்பநிலையில் மின்னோட்டத்தைக் கடப்பதன் மூலமோ அல்லது வெற்றிடத்தில் 2,200-2,500 டிகிரி செல்சியஸ் வெப்பமடைவதன் மூலமோ சின்டரிங் ஏற்படுகிறது. அதன் பிறகு உலோகத்தின் தூய்மை கணிசமாக அதிகரிக்கிறது, 99.9-99.95% க்கு சமமாகிறது.
டான்டலம் இங்காட்களை மேலும் சுத்திகரிப்பதற்கும் உற்பத்தி செய்வதற்கும், நுகர்வு மின்முனையுடன் கூடிய வில் உலைகளில் மின்சார வெற்றிட உருகுதல் பயன்படுத்தப்படுகிறது, மேலும் ஆழமான சுத்திகரிப்புக்கு எலக்ட்ரான் கற்றை உருகுதல் பயன்படுத்தப்படுகிறது, இது டான்டலத்தில் உள்ள அசுத்தங்களின் உள்ளடக்கத்தை கணிசமாகக் குறைக்கிறது, அதன் நீர்த்துப்போகும் தன்மையை அதிகரிக்கிறது மற்றும் வெப்பநிலையைக் குறைக்கிறது. உடையக்கூடிய நிலைக்கு மாறுதல். அத்தகைய தூய்மையின் டான்டலம் முழுமையான பூஜ்ஜியத்திற்கு நெருக்கமான வெப்பநிலையில் அதிக நீர்த்துப்போகும் தன்மையைத் தக்க வைத்துக் கொள்கிறது! ஒரு டான்டலம் இங்காட்டின் மேற்பரப்பு உருகப்படுகிறது (இங்காட்டின் மேற்பரப்பிற்கு தேவையான பண்புகளை வழங்க) அல்லது ஒரு லேத்தில் செயலாக்கப்படுகிறது.
இயற்பியல் பண்புகள்
20 ஆம் நூற்றாண்டின் தொடக்கத்தில் மட்டுமே விஞ்ஞானிகள் தூய டான்டலம் உலோகத்தின் மீது தங்கள் கைகளைப் பெற்றனர் மற்றும் சற்று நீல நிற ஈய நிறத்துடன் இந்த வெளிர் சாம்பல் உலோகத்தின் பண்புகளை விரிவாக ஆய்வு செய்ய முடிந்தது. இந்த உறுப்பு என்ன குணங்களைக் கொண்டுள்ளது? நிச்சயமாக, டான்டலம் ஒரு கன உலோகம்: அதன் அடர்த்தி 20 ° C இல் 16.6 g/cm 3 ஆகும் (ஒப்பிடுகையில், இரும்பின் அடர்த்தி 7.87 g/cm 3, ஈயத்தின் அடர்த்தி 11.34 g/cm 3) கன மீட்டர் இந்த உறுப்புக்கு ஆறு மூன்று டன் டிரக்குகள் தேவைப்படும். அதிக வலிமை மற்றும் கடினத்தன்மை சிறந்த பிளாஸ்டிக் பண்புகளுடன் இணைக்கப்பட்டுள்ளது. தூய டான்டலம் இயந்திர செயலாக்கத்திற்கு நன்கு உதவுகிறது, எளிதில் முத்திரையிடப்பட்டு, மெல்லிய தாள்கள் (சுமார் 0.04 மிமீ தடிமன்) மற்றும் கம்பி (டாண்டலம் 190 Hn/m2 அல்லது 190·102 kgf/mm2 இன் மீள் மாடுலஸ் 25 °C) ஆகியவற்றில் செயலாக்கப்படுகிறது. குளிரில், குறிப்பிடத்தக்க வேலை கடினப்படுத்துதல் இல்லாமல் உலோகத்தை செயலாக்க முடியும் மற்றும் இடைநிலை துப்பாக்கிச் சூடு இல்லாமல் 99% சுருக்க விகிதத்துடன் உருமாற்றத்திற்கு உட்பட்டது. -196 டிகிரி செல்சியஸ் வரை குளிரூட்டப்பட்டாலும் டான்டலம் ஒரு பிளாஸ்டிக்கில் இருந்து உடையக்கூடிய நிலைக்கு மாறுவது கவனிக்கப்படுவதில்லை. அனீல்டு உயர் தூய்மையான டான்டலத்தின் இழுவிசை வலிமை 27 °C இல் 206 MN/m2 (20.6 kgf/mm2) மற்றும் 490 °C இல் 190 MN/m2 (19 kgf/mm2) ஆகும்; ஒப்பீட்டு நீட்சி 36% (27 °C இல்) மற்றும் 20% (490 °C இல்). டான்டலம் ஒரு உடலை மையமாகக் கொண்ட கனசதுர லட்டு (a = 3.296 A); அணு ஆரம் 1.46 A, அயனி ஆரம் Ta 2+ 0.88 A, Ta 5+ 0.66 A.
முன்பு குறிப்பிட்டபடி, டான்டலம் மிகவும் கடினமான உலோகம் (அனீல் செய்யப்பட்ட நிலையில் டான்டலம் தாள்களின் பிரைனெல் கடினத்தன்மை 450-1250 MPa, சிதைந்த நிலையில் 1250-3500 MPa). மேலும், பல அசுத்தங்களைச் சேர்ப்பதன் மூலம் உலோகத்தின் கடினத்தன்மையை அதிகரிக்க முடியும், எடுத்துக்காட்டாக கார்பன் அல்லது நைட்ரஜன் (வெப்பத்தின் போது வாயுக்களை உறிஞ்சிய பிறகு டான்டலம் தாளின் பிரினெல் கடினத்தன்மை 6000 MPa ஆக அதிகரிக்கிறது). இதன் விளைவாக, இடைநிலை அசுத்தங்கள் ப்ரினெல் கடினத்தன்மை, இழுவிசை வலிமை மற்றும் மகசூல் வலிமை ஆகியவற்றின் அதிகரிப்புக்கு பங்களிக்கின்றன, ஆனால் அவை பிளாஸ்டிசிட்டி பண்புகளைக் குறைத்து குளிர் மிருதுவான தன்மையை அதிகரிக்கின்றன; வேறுவிதமாகக் கூறினால், அவை உலோகத்தை உடையக்கூடியதாக ஆக்குகின்றன. எழுபத்து-மூன்றாவது தனிமத்தின் மற்ற சிறப்பியல்பு அம்சங்கள் அதன் உயர் வெப்ப கடத்துத்திறன் ஆகும், 20-100 °C இல் இந்த மதிப்பு 54.47 W/(m∙K) அல்லது 0.13 cal/(cm·sec·°С) மற்றும் பயனற்ற தன்மை (ஒருவேளை அதிகமாக இருக்கலாம் டான்டலத்தின் ஒரு முக்கியமான இயற்பியல் சொத்து) - இது கிட்டத்தட்ட 3,000 °C இல் உருகும் (இன்னும் துல்லியமாக, 2,996 °C), டங்ஸ்டன் மற்றும் ரீனியம் இரண்டாவதாக. டான்டலத்தின் கொதிநிலையும் மிக அதிகமாக உள்ளது: 5,300 °C.
டான்டலத்தின் மற்ற இயற்பியல் பண்புகளைப் பொறுத்தவரை, 0 முதல் 100 °C வெப்பநிலையில் அதன் குறிப்பிட்ட வெப்பம் 0.142 kJ/(kg K) அல்லது 0.034 cal/(g °C); டான்டலத்தின் நேரியல் விரிவாக்கத்தின் வெப்பநிலை குணகம் 8.0·10 -6 (20-1,500 °C வெப்பநிலையில்). 0 °C இல் எழுபத்து-மூன்றாவது தனிமத்தின் மின் எதிர்ப்புத் திறன் 13.2 10 -8 ohm m, 2000 °C 87 10 -8 ohm m. 4.38 K இல் உலோகம் ஒரு சூப்பர் கண்டக்டராக மாறுகிறது. டான்டலம் என்பது பாரா காந்தம், குறிப்பிட்ட காந்த உணர்திறன் 0.849·10 -6 (18 °C இல்).
எனவே, டான்டலம் ஒரு தனித்துவமான இயற்பியல் பண்புகளைக் கொண்டுள்ளது: அதிக வெப்ப பரிமாற்ற குணகம், வாயுக்களை உறிஞ்சும் அதிக திறன், வெப்ப எதிர்ப்பு, பயனற்ற தன்மை, கடினத்தன்மை மற்றும் பிளாஸ்டிசிட்டி. கூடுதலாக, இது அதிக வலிமையால் வேறுபடுகிறது - இது ஏற்கனவே உள்ள அனைத்து முறைகளையும் பயன்படுத்தி அழுத்த சிகிச்சைக்கு நன்கு உதவுகிறது: மோசடி, ஸ்டாம்பிங், உருட்டல், வரைதல், முறுக்குதல். டான்டலம் நல்ல வெல்டிபிலிட்டியால் வகைப்படுத்தப்படுகிறது (ஆர்கான், ஹீலியம் அல்லது வெற்றிடத்தில் வெல்டிங் மற்றும் சாலிடரிங்). கூடுதலாக, டான்டலம் விதிவிலக்கான இரசாயன மற்றும் அரிப்பு எதிர்ப்பைக் கொண்டுள்ளது (ஒரு அனோடிக் படத்தின் உருவாக்கத்துடன்), குறைந்த நீராவி அழுத்தம் மற்றும் குறைந்த எலக்ட்ரான் வேலை செயல்பாடு, மேலும், இது உடலின் வாழும் திசுக்களுடன் நன்றாகப் பெறுகிறது.
இரசாயன பண்புகள்
நிச்சயமாக, டான்டலத்தின் மிகவும் மதிப்புமிக்க பண்புகளில் ஒன்று அதன் விதிவிலக்கான இரசாயன எதிர்ப்பாகும்: இந்த வகையில் இது உன்னத உலோகங்களுக்கு அடுத்தபடியாக உள்ளது, பின்னர் எப்போதும் இல்லை. இது அனைத்து செறிவுகளின் (150 ° C வெப்பநிலை வரை) ஹைட்ரோகுளோரிக், சல்பூரிக், நைட்ரிக், பாஸ்போரிக் மற்றும் கரிம அமிலங்களுக்கு எதிர்ப்புத் தெரிவிக்கிறது. அதன் வேதியியல் நிலைத்தன்மையைப் பொறுத்தவரை, டான்டலம் கண்ணாடியைப் போன்றது - இது அமிலங்கள் மற்றும் அவற்றின் கலவைகளில் கரையாதது, அக்வா ரெஜியா கூட அதைக் கரைக்காது, இதற்கு எதிராக தங்கம் மற்றும் பிளாட்டினம் மற்றும் பல மதிப்புமிக்க உலோகங்கள் சக்தியற்றவை. எழுபத்து மூன்றாவது தனிமம் ஹைட்ரோபுளோரிக் மற்றும் நைட்ரிக் அமிலங்களின் கலவையில் மட்டுமே கரையக்கூடியது. மேலும், ஹைட்ரோஃப்ளூரிக் அமிலத்துடன் எதிர்வினை உலோக தூசியுடன் மட்டுமே நிகழ்கிறது மற்றும் ஒரு வெடிப்புடன் சேர்ந்துள்ளது. சூடான ஹைட்ரோகுளோரிக் மற்றும் சல்பூரிக் அமிலங்களில் கூட, டான்டலம் அதன் இரட்டை சகோதரர் நியோபியத்தை விட அதிக எதிர்ப்புத் திறன் கொண்டது. இருப்பினும், டான்டலம் காரங்களுக்கு எதிர்ப்புத் திறன் குறைவாக உள்ளது - காஸ்டிக் காரங்களின் சூடான தீர்வுகள் உலோகத்தை அரிக்கிறது. டான்டாலிக் அமிலங்களின் உப்புகள் (டான்டலேட்டுகள்) பொதுவான சூத்திரத்தால் வெளிப்படுத்தப்படுகின்றன: xMe 2 O yTa 2 O 5 H 2 O, இதில் metatantalates MeTaO 3, orthotantalates Me 3 TaO 4, Me 5 TaO 5 போன்ற உப்புகள், இங்கு நான் ஒரு கார உலோகம் ; ஹைட்ரஜன் பெராக்சைடு முன்னிலையில், பெர்டான்டலேட்டுகளும் உருவாகின்றன. மிக முக்கியமான ஆல்காலி மெட்டல் டான்டலேட்டுகள் KTaO 3 மற்றும் NaTaO 3; இந்த உப்புகள் ஃபெரோ எலக்ட்ரிக்ஸ் ஆகும்.
டான்டலத்தின் உயர் அரிப்பு எதிர்ப்பானது வளிமண்டல ஆக்சிஜனுடனான அதன் தொடர்பு அல்லது இந்த செல்வாக்கிற்கு அதன் உயர் எதிர்ப்பின் மூலம் குறிக்கப்படுகிறது. உலோகம் 280 °C இல் மட்டுமே ஆக்சிஜனேற்றம் செய்யத் தொடங்குகிறது, இது Ta 2 O 5 (டான்டலம் பென்டாக்சைடு மட்டுமே நிலையான உலோக ஆக்சைடு) பாதுகாப்பு படத்தால் மூடப்பட்டிருக்கும், இது உலோகத்தை இரசாயன எதிர்வினைகளின் செயல்பாட்டிலிருந்து பாதுகாக்கிறது மற்றும் மின்சார ஓட்டத்தைத் தடுக்கிறது. உலோகத்திலிருந்து எலக்ட்ரோலைட் வரை. இருப்பினும், வெப்பநிலை 500 ° C ஆக அதிகரிப்பதன் மூலம், ஆக்சைடு படம் படிப்படியாக நுண்ணியதாகி, சிதைந்து, உலோகத்திலிருந்து பிரிந்து, அரிப்புக்கு எதிரான பாதுகாப்பு அடுக்கின் மேற்பரப்பை இழக்கிறது. எனவே, ஒரு வெற்றிடத்தில் சூடான அழுத்த சிகிச்சையை மேற்கொள்வது நல்லது, ஏனெனில் காற்றில் உலோகம் குறிப்பிடத்தக்க ஆழத்திற்கு ஆக்ஸிஜனேற்றப்படுகிறது. நைட்ரஜன் மற்றும் ஆக்ஸிஜனின் இருப்பு டான்டலத்தின் கடினத்தன்மையையும் வலிமையையும் அதிகரிக்கிறது, அதே நேரத்தில் அதன் நீர்த்துப்போகும் தன்மையைக் குறைக்கிறது மற்றும் உலோகத்தை உடையக்கூடியதாக ஆக்குகிறது, மேலும், முன்பு குறிப்பிட்டபடி, டான்டலம் ஒரு திடமான கரைசலை உருவாக்குகிறது மற்றும் ஆக்ஸிஜனுடன் Ta 2 O 5 ஆக்சைடை உருவாக்குகிறது (அதிகரிப்புடன். டான்டலத்தில் உள்ள O 2 உள்ளடக்கம், வலிமை பண்புகளில் கூர்மையான அதிகரிப்பு ஏற்படுகிறது மற்றும் டக்டிலிட்டி மற்றும் அரிப்பு எதிர்ப்பில் வலுவான குறைவு). டான்டலம் நைட்ரஜனுடன் வினைபுரிந்து மூன்று கட்டங்களை உருவாக்குகிறது - டான்டலத்தில் நைட்ரஜனின் திடமான தீர்வு, டான்டலம் நைட்ரைடுகள்: Ta 2 N மற்றும் TaN - வெப்பநிலை வரம்பில் 300 முதல் 1,100 ° C வரை. அதிக வெற்றிட நிலையில் (2,000 °C க்கும் அதிகமான வெப்பநிலையில்) டான்டலத்தில் உள்ள நைட்ரஜன் மற்றும் ஆக்ஸிஜனை அகற்றுவது சாத்தியமாகும்.
டான்டலம் ஹைட்ரஜனுடன் 350 °C வரை வெப்பமடையும் வரை பலவீனமாக வினைபுரிகிறது; எதிர்வினை வீதம் 450 °C இலிருந்து மட்டுமே கணிசமாக அதிகரிக்கிறது (டான்டலம் ஹைட்ரைடு உருவாகிறது மற்றும் டான்டலம் உடையக்கூடியது). வெற்றிடத்தில் (800 °C க்கு மேல்) அதே வெப்பமாக்கல் ஹைட்ரஜனை அகற்ற உதவுகிறது, இதன் போது டான்டலத்தின் இயந்திர பண்புகள் மீட்டமைக்கப்பட்டு ஹைட்ரஜன் முற்றிலும் அகற்றப்படும்.
ஃவுளூரின் ஏற்கனவே அறை வெப்பநிலையில் டான்டலத்தில் செயல்படுகிறது, மேலும் ஹைட்ரஜன் ஃவுளூரைடும் உலோகத்துடன் வினைபுரிகிறது. உலர் குளோரின், புரோமின் மற்றும் அயோடின் ஆகியவை 150 டிகிரி செல்சியஸ் மற்றும் அதற்கு மேற்பட்ட வெப்பநிலையில் டான்டலத்தில் ஒரு இரசாயன விளைவைக் கொண்டுள்ளன. குளோரின் 250 டிகிரி செல்சியஸ் வெப்பநிலையிலும், புரோமின் மற்றும் அயோடின் 300 டிகிரி செல்சியஸ் வெப்பநிலையிலும் உலோகத்துடன் தீவிரமாக தொடர்பு கொள்ளத் தொடங்குகிறது. டான்டலம் மிக அதிக வெப்பநிலையில் கார்பனுடன் தொடர்பு கொள்ளத் தொடங்குகிறது: 1,200-1,400 டிகிரி செல்சியஸ், மற்றும் அமிலங்களுக்கு மிகவும் எதிர்ப்புத் திறன் கொண்ட ரிஃப்ராக்டரி டான்டலம் கார்பைடுகளின் உருவாக்கம் ஏற்படுகிறது. டான்டலம் போரோனுடன் இணைந்து போரைடுகளை உருவாக்குகிறது - அக்வா ரெஜியாவின் விளைவுகளை எதிர்க்கும் திடமான, பயனற்ற கலவைகள். டான்டலம் பல உலோகங்களுடன் (மாலிப்டினம், நியோபியம், டைட்டானியம், டங்ஸ்டன், வெனடியம் மற்றும் பிற) தொடர்ச்சியான திடமான தீர்வுகளை உருவாக்குகிறது. டான்டலம் தங்கம், அலுமினியம், நிக்கல், பெரிலியம் மற்றும் சிலிக்கான் ஆகியவற்றுடன் வரையறுக்கப்பட்ட திடமான தீர்வுகளை உருவாக்குகிறது. டான்டலம் மெக்னீசியம், லித்தியம், பொட்டாசியம், சோடியம் மற்றும் வேறு சில தனிமங்களுடன் எந்த சேர்மத்தையும் உருவாக்குவதில்லை. தூய டான்டலம் பல திரவ உலோகங்களை (Na, K, Li, Pb, U-Mg மற்றும் Pu-Mg கலவைகள்) எதிர்க்கும்.
அறியப்பட்ட வேதியியல் கூறுகளின் குழுவில் டான்டலம் ஒரு சிறப்பு இடத்தைப் பிடித்துள்ளது. இந்த உலோகம் உன்னதமானது அல்ல, ஆனால் அதன் செயல்திறன் குணங்கள் பல்வேறு துறைகளில் தேவையை உருவாக்குகின்றன. மேலும், இது கட்டுமானம் மற்றும் உற்பத்தித் தொழில்களுக்கு மட்டுமல்ல, நகைகளுக்கும் பொருந்தும். இன்று, டான்டலத்தின் பயன்பாடு அதன் அரிதான தன்மையால் மிகவும் குறைவாகவே உள்ளது. இன்னும் சந்தையில் இந்த பொருளிலிருந்து தயாரிக்கப்படும் பரந்த அளவிலான தயாரிப்புகள் உள்ளன.
உலோகம் பற்றிய பொதுவான தகவல்கள்
டான்டலம் அதன் தூய வடிவத்தில் இயற்கையில் இல்லை. இது பொதுவாக ஒத்த குணாதிசயங்களைக் கொண்ட மற்ற கனிமங்களுடன் சேர்ந்து வெட்டி எடுக்கப்படுகிறது. தனிமத்தின் இந்த அம்சம் அதன் தாமதமான கண்டுபிடிப்புக்கு வழிவகுத்தது. ஆனால் இந்த நாட்களில் டான்டலத்தை தனிமைப்படுத்த பயனுள்ள வழிகள் உள்ளன, அவற்றில் ஒன்று பிரித்தெடுக்கும் முறை. மின்னாற்பகுப்பு குறிப்பாக உலோகப் பொருட்களை உற்பத்தி செய்யப் பயன்படுகிறது. ஒரு கிராஃபைட் க்ரூசிபிளைப் பயன்படுத்தி, உறுப்பு கொண்டிருக்கும் அடித்தளம் உருகுகிறது, அதன் பிறகு கொள்கலனின் சுவர்களில் தூள் உள்ளது. தீவனத்தை செயலாக்குவதற்கான கூடுதல் தொழில்நுட்பம் டான்டலம் எவ்வாறு பயன்படுத்தப்படும் என்பதைப் பொறுத்தது: இது ஒரு இங்காட், கம்பி, தாள், ஒரு குறிப்பிட்ட வடிவத்தின் ஒரு பகுதி அல்லது தெளிப்பதற்கான கலவையின் வடிவத்தில் கொடுக்கப்படலாம். டான்டலம் பவுடரில் இருந்து உலோகக் கலவைகளை உருவாக்கும் தொழில்நுட்பங்களும் பிரபலமாக உள்ளன. கலப்பு பொருட்களுடன் கலவையானது பொருளின் தனிப்பட்ட பண்புகளை மேம்படுத்துவதை சாத்தியமாக்குகிறது.

இயற்பியல் பண்புகள்
உலோகம் சுமார் 3017 °C உயர் உருகும் புள்ளியைக் கொண்டுள்ளது, இது உற்பத்தியில் தீவிர வெப்ப நிலைகளில் பயன்படுத்த அனுமதிக்கிறது. அதே நேரத்தில், இது டக்டிலிட்டி மற்றும் கடினத்தன்மையின் பண்புகளின் அரிய கலவையைக் கொண்டுள்ளது. முதல்வரைப் பொறுத்தவரை, அது தங்கத்தைப் போல மென்மையானது. இந்த வழக்கில், டான்டலத்தின் கடினத்தன்மை 16.65 g/cm 3 ஆகும். இயற்பியல் குணங்களின் இந்த கலவையானது பொருளை எளிதாக செயலாக்க உதவுகிறது, அதற்கு வெவ்வேறு வடிவங்கள் மற்றும் அளவுகளை அளிக்கிறது, மேலும் அதை முக்கியமான வழிமுறைகள் மற்றும் கட்டமைப்புகளிலும் பயன்படுத்துகிறது. சிறிய கூறுகள் கியர்கள் மற்றும் மின் சாதனங்களின் பாகங்களாக சிறப்பாக செயல்படுகின்றன. Tantalum அணிய எதிர்ப்பு மற்றும் நீடித்தது, எனவே நுகர்வு கூறுகள் நீண்ட கால செயல்பாட்டின் எதிர்பார்ப்புடன் அதிலிருந்து தயாரிக்கப்படுகின்றன. கூடுதலாக, இந்த உலோகம் ஒரு பயனுள்ள வாயு உறிஞ்சியாக செயல்பட முடியும். அதிக வெப்பநிலையில், டான்டலம் பாகங்களும் அதிக கடத்தும் பண்புகளை வெளிப்படுத்துகின்றன.
இரசாயன பண்புகள்

அதன் தூய வடிவத்தில், உலோகம் காரங்கள், கரிம மற்றும் கனிம அமில பொருட்கள் மற்றும் பிற செயலில் உள்ள ஊடகங்களின் செல்வாக்கின் விளைவுகளை திறம்பட எதிர்க்கிறது. உருகிய வடிவத்தில் காரங்கள் டான்டலத்தில் குறிப்பிடத்தக்க விளைவைக் கொண்டிருக்கும் வரை. ஆக்சிஜனேற்ற செயல்முறைகள் 280 °C க்கும் குறைவான வெப்பநிலையில் நிகழ்கின்றன, மேலும் இது 250 °C இல் ஆலசன் கூறுகளுடன் வினைபுரிகிறது. எதிர்வினைகளுடன் தொடர்பு கொண்ட டான்டலத்தின் வேதியியல் பண்புகளை கண்ணாடியுடன் ஒப்பிடலாம். நைட்ரிக் மற்றும் ஹைட்ரோபுளோரிக் அமிலங்கள் தவிர அமில சூழல்களில் இது கரையாது. இந்த பொருள் அதன் செறிவு பொருட்படுத்தாமல், சல்பூரிக் அமிலத்தை எதிர்க்கும். இருப்பினும், பெரும்பாலான சந்தர்ப்பங்களில் செயல்பாட்டு செயல்முறைகள் உலோகத்தின் கட்டமைப்பில் ஒரு சிறிய விளைவைக் கொண்டிருக்கின்றன. பொதுவாக மாற்றங்கள் திரைப்பட பூச்சு அல்லது அரிப்பு வடிவத்தில் தோன்றும்.
டான்டலம் எங்கே பயன்படுத்தப்படுகிறது?

இந்த உலோகம் பரவலாக இல்லை, ஆனால் அதன் பயன்பாட்டின் பல பகுதிகள் உள்ளன. முதலில், இது தொழில். உலோகம், உணவுத் துறை, உற்பத்தித் தொழில்கள், ரேடியோ இன்ஜினியரிங், மெக்கானிக்கல் இன்ஜினியரிங் போன்றவற்றில் இந்த உறுப்பு பயன்படுத்தப்படுகிறது. கட்டுமானத் துறையில், இந்த உலோகம் குறைவான உற்பத்தி அளவுகளால் துல்லியமாக தேவை இல்லை, ஆனால் தனிப்பட்ட கட்டமைப்பு கூறுகள் இன்னும் தயாரிக்கப்படுகின்றன. இந்த பொருள் - ஒரு விதியாக, கட்டமைப்புகளை வலுப்படுத்தும் முக்கியமான பணிகளுக்காக வடிவமைக்கப்பட்ட வன்பொருள். டான்டலம் எங்கு பயன்படுத்தப்படுகிறது என்பதைப் புரிந்து கொள்ள, அதன் செயல்திறன் பண்புகளுக்கு கவனம் செலுத்த வேண்டியது அவசியம். அவர் ஒரு நல்ல நடத்துனராக செயல்பட முடியும் என்பது ஏற்கனவே குறிப்பிடப்பட்டுள்ளது. எனவே, இது மின் பொறியியலில் சூப்பர் கண்டக்டராகப் பயன்படுத்தப்படுகிறது. மறுபுறம், அதன் வெப்ப எதிர்ப்பு மற்ற உலோகங்களின் வெப்ப சிகிச்சையில் அதன் பயன்பாட்டிற்கான சாத்தியங்களைத் திறக்கிறது. அதன் அதிகரித்த அடர்த்திக்கு நன்றி, டான்டலம் பாதுகாப்புத் துறையில் ஒரு சிறந்த தீர்வாக மாறியுள்ளது. அதிக ஊடுருவும் சக்தி கொண்ட எறிகணைகளை உருவாக்க இது பயன்படுகிறது.
டான்டலம் கம்பி
பொதுவாக உருட்டப்பட்ட உலோகம் என்பது சந்தையில் இந்த பொருளின் விளக்கக்காட்சியின் மிக விரிவான வடிவமாகும். வயர் பிரிவில் குறிப்பிடத்தக்க இடத்தைப் பிடித்துள்ளது. இது அசாதாரணமானது, அதன் மிதமான அளவு காரணமாக, அதை ஒரு நூலாகப் பயன்படுத்தலாம். இது மருத்துவத் துறைக்கான டான்டலத்தின் மதிப்பை விளக்குகிறது - இந்த வகையான தயாரிப்புகள் தையல் மற்றும் கட்டுகளுக்குப் பயன்படுத்தப்படுகின்றன. ஆனால் இது அத்தகைய கம்பியின் தனித்துவமான குணங்களில் ஒன்றை நிரூபிக்கும் ஒரு எடுத்துக்காட்டு. இயந்திர பொறியியல், விமானப் போக்குவரத்து, இயந்திரக் கருவிகள் மற்றும் மூலதன கட்டுமானம் ஆகியவற்றில் பெரிய வடிவங்கள் பயன்படுத்தப்படுகின்றன. மேலும், நோக்கத்தைப் பொறுத்து, மென்மையான மற்றும் கடினமான உலோகத்தைப் பயன்படுத்தலாம். டான்டலம், செயலாக்கத்தில் அதன் நெகிழ்வுத்தன்மையின் காரணமாக, 0.15 மிமீ அல்லது அதற்கு மேற்பட்ட தடிமன் கொண்ட 1500 செ.மீ முதல் நீண்ட கம்பிகளை உற்பத்தி செய்ய அனுமதிக்கிறது. முடிக்கப்பட்ட தயாரிப்புகளில், பயனர்கள் குறிப்பிடுவது போல், பர்ர்கள், விரிசல்கள் மற்றும் பிற குறைபாடுகள் அரிதாகவே காணப்படுகின்றன. இருப்பினும், மெல்லிய அமைப்பு இன்னும் சேமிப்பு மற்றும் போக்குவரத்து நிலைமைகளில் தேவைகளை விதிக்கிறது - குறிப்பாக, ஈரப்பதம் மற்றும் ஆக்கிரமிப்பு சூழல்களுடன் தொடர்பு கொள்ள கம்பியை வெளிப்படுத்த பரிந்துரைக்கப்படவில்லை.

டான்டலம் டேப்
உருட்டப்பட்ட உலோக தயாரிப்புகளின் உற்பத்திக்கான இந்த வடிவம் பரவலாக உள்ளது. நாடாக்கள் மருத்துவம், எண்ணெய் தொழில், இயந்திர பொறியியல் மற்றும் ஆற்றல் துறையில் கூட பயன்படுத்தப்படுகின்றன. நுகர்வோர் இந்த தயாரிப்பை அதன் உயிர் இணக்கத்தன்மை, சிறந்த அமைப்புடன் கூடிய அதிக வலிமை, நல்ல வேலைத்திறன் மற்றும் அரிப்பு செயல்முறைகளுக்கு எதிர்ப்பை மதிக்கிறார்கள். டான்டலத்தால் செய்யப்பட்ட ஒத்த தயாரிப்புகளை எஃகு அல்லது அலுமினியத்தால் செய்யப்பட்ட அனலாக்ஸுடன் ஒப்பிட்டுப் பார்த்தால், உடைகள் எதிர்ப்பு மற்றும் ஆயுள் முன்னுக்கு வரும். டேப் அதிக இழுவிசை சுமைகள் மற்றும் இரசாயன தாக்கங்களை தாங்கும். மறுபுறம், உயர் பிளாஸ்டிசிட்டி அத்தகைய தயாரிப்புகளை ஒரு குறிப்பிட்ட வடிவத்தை நிலையானதாக பராமரிக்க அனுமதிக்காது. சிறிய அழுத்தம் கூட சிதைவுக்கு வழிவகுக்கிறது.
டான்டலம் அடிப்படையிலான உலோகக்கலவைகள்

கலப்பு கூறுகளுடன் மாற்றியமைக்கப்பட்ட உலோகக்கலவைகள் முக்கியமாக உடல் வலிமை மற்றும் வெப்ப எதிர்ப்பின் உயர் குணங்களைப் பெறுகின்றன. சராசரி குணாதிசயங்களைக் கொண்ட ஒரு தயாரிப்பு அதன் செயல்திறன் குணங்களை இழக்காமல் 1650 ° C வெப்பநிலையைத் தாங்கும் என்று சொன்னால் போதுமானது. உண்மையில், இது இரசாயனத் தொழில், ஆற்றல், உலோகம் மற்றும் கருவி தயாரிப்பில் டான்டலம் உலோகக் கலவைகளைப் பயன்படுத்த அனுமதிக்கிறது. மேலும், சில நிறுவனங்கள் ராக்கெட் மற்றும் விண்வெளிக் கோளத்திற்கான கூறுகளை தயாரிப்பதில் இந்த பொருளைப் பயன்படுத்துகின்றன. பயன்பாட்டின் திசையைப் பொறுத்து, தொழில்நுட்ப வல்லுநர்கள் டான்டலத்தை அலாய் செய்வதற்கு வெவ்வேறு கலவைகளை உருவாக்குகிறார்கள். சில சந்தர்ப்பங்களில், மாற்றம் அதிக நீர்த்துப்போகும் தன்மையை அடைவதை சாத்தியமாக்குகிறது, மற்றவற்றில், எடுத்துக்காட்டாக, எலக்ட்ரான் கற்றை முறையைப் பயன்படுத்தி வெல்டிங் செயல்பாடுகளுக்கு பொருத்தமான பொருளை உருவாக்குகிறது. டான்டலம் ஒரு கலவை கூறுகளாகவும் செயல்பட முடியும். பொதுவாக, செயல்திறன் பண்புகளை மேம்படுத்தும் இந்த முறை அடிப்படை உலோகங்களுக்கு எதிர்ப்பு அரிப்பை மற்றும் வெப்ப எதிர்ப்பை வழங்க பயன்படுகிறது.
ரேடியோ பொறியியலில் டான்டலம்
மின் சாதனங்கள் மற்றும் பாகங்களின் உற்பத்தியில், உகந்த மின்னோட்ட கடத்துத்திறனை பராமரிக்கும் திறன் மற்றும் அதிர்வெண் சமிக்ஞைகளை பராமரிக்கும் திறன், உறுப்பு தளத்தின் அளவைக் குறைக்கும் போது முன்னுக்கு வருகிறது. இந்த காரணத்திற்காக, டான்டலம் பெரும்பாலும் மின்தேக்கிகள், தைரிஸ்டர்கள், டிரான்சிஸ்டர்கள் மற்றும் செமிஸ்டர்கள் தயாரிப்பில் பயன்படுத்தப்படுகிறது. முன்னதாக, அதே மின்தேக்கிகளுக்கு தாள் அலுமினியத்தின் ரோல்கள் பயன்படுத்தப்பட்டன. இந்த தீர்வு பகுதியின் அளவை அதிகரித்தால் மட்டுமே செயல்பாட்டு அளவுருக்களை அதிகரிக்கும் சாத்தியத்தை கருதுகிறது. மின்தேக்கியின் அளவை அதிகரிப்பதோடு தொடர்புடைய பிற குணாதிசயங்களின் தலைகீழ் குறைவை இது குறிப்பிடவில்லை. ரேடியோ-எலக்ட்ரானிக் கூறுகள் பங்கேற்கும் எதிர்மறை செயல்முறைகளுக்கு எதிர்ப்புத் தெரிவிக்கும் டான்டலத்தின் பயன்பாடு, பகுதியின் பரிமாணங்களைப் பராமரிக்கும் போது மின் அளவை அதிகரிக்கச் செய்தது. மற்றொரு விஷயம் என்னவென்றால், அலுமினியம் இந்த பகுதியில் தோல்வியடையாது, ஏனெனில் இது மிகவும் மலிவு.
முடிவுரை

இந்த உலோகம் தனித்துவமான அல்லது தரமற்ற பண்புகளைக் கொண்டிருக்கவில்லை. இது அரிப்பு எதிர்ப்பு, கடினத்தன்மை அல்லது வெப்ப எதிர்ப்பு உட்பட பல கவர்ச்சிகரமான குணங்களைக் கொண்டுள்ளது. ஆனால் இந்த பண்புகள் தனித்தனியாக மற்ற உலோகங்களில் உள்ளன. மேலும், சிலவற்றில் அவை மிகவும் உச்சரிக்கப்படுகின்றன. இருப்பினும், ஒரு தனிமத்தில் வெளித்தோற்றத்தில் எதிரெதிர் பண்புகளின் கலவையானது உண்மையிலேயே தனித்துவமானது. தொழில்நுட்ப வல்லுநர்கள் செயற்கையான வழிமுறைகளால் பொருட்களின் வேலை குணங்களில் சிறப்பு சேர்க்கைகளை அடைய முயற்சி செய்கிறார்கள், இந்த விஷயத்தில் அவை தோற்றத்தின் தன்மையால் தீர்மானிக்கப்படுகின்றன. எடுத்துக்காட்டாக, மருத்துவம் மற்றும் உலோகவியலில் டான்டலத்தின் பயன்பாடு முற்றிலும் வேறுபட்ட நோக்கங்களைக் கொண்டுள்ளது. ஒரு வழக்கில், சிறிய தயாரிப்பு அளவுகளுடன் அதிக வலிமை மதிப்பிடப்படுகிறது, இரண்டாவதாக, செயலாக்கத்தில் நெகிழ்வுத்தன்மை மதிப்பிடப்படுகிறது. ஆனால் டான்டலத்தின் எதிர்மறையான சொத்தும் உள்ளது, இது அதன் பயன்பாட்டின் அனைத்து பகுதிகளுக்கும் பொருந்தும் - இது அதிக விலை, மற்றும் சில சந்தர்ப்பங்களில், உடல் அணுக முடியாதது.
டான்டலம் அதிக உருகுநிலையைக் கொண்டுள்ளது -- 3290 K (3017 °C); 5731 K (5458 °C) இல் கொதிக்கிறது.
டான்டலம் அடர்த்தி 16.65 கிராம்/செ.மீ. அதன் கடினத்தன்மை இருந்தபோதிலும், அது தங்கம் போல நெகிழ்வானது. தூய டான்டலம் எந்திரத்திற்கு நன்கு உதவுகிறது, எளிதில் முத்திரையிடப்படுகிறது, கம்பி மற்றும் மெல்லிய தாள்களில் ஒரு மில்லிமீட்டர் தடிமன் கொண்ட நூறில் ஒரு பங்கு தடிமன் கொண்டது. டான்டலம் ஒரு சிறந்த பெறுபவர் (எரிவாயு உறிஞ்சி) டான்டலம் ஒரு உடலை மையமாகக் கொண்ட கனசதுர லட்டியைக் கொண்டுள்ளது. பரம காந்த பண்புகளை கொண்டது. 4.38 K இல் அது ஒரு சூப்பர் கண்டக்டராக மாறுகிறது. தூய டான்டலம் என்பது ஒரு நீர்த்துப்போகக்கூடிய உலோகமாகும், இது குறிப்பிடத்தக்க கடினப்படுத்துதல் இல்லாமல் குளிரில் அழுத்தத்தால் செயலாக்கப்படும். இது இடைநிலை அனீலிங் இல்லாமல் 99% குறைப்பு விகிதத்துடன் சிதைக்கப்படலாம். -196 டிகிரி செல்சியஸ்க்கு குளிர்ச்சியடையும் போது டான்டலம் ஒரு டக்டைலில் இருந்து உடையக்கூடிய நிலைக்கு மாறுவது கண்டறியப்படவில்லை. டான்டலத்தின் பண்புகள் பெரும்பாலும் அதன் தூய்மையைப் பொறுத்தது; ஹைட்ரஜன், நைட்ரஜன், ஆக்ஸிஜன் மற்றும் கார்பன் ஆகியவற்றின் அசுத்தங்கள் உலோகத்தை உடையக்கூடியதாக ஆக்குகின்றன.
அணுவின் மின்னணு அமைப்பு.
1s 22s 22p 63s 23p64s 23d104p65s24d105p66s24f145d3
வரிசை எண்-73
குழுவைச் சேர்ந்தவர் - ஏ
d-உறுப்பு
டான்டலம் (V) ஆக்சைடு ஒரு வெள்ளை தூள், நீர் அல்லது அமிலங்களில் (H2F2 தவிர) கரையாதது. மிகவும் பயனற்றது (tmelt = 1875 ° C). ஆக்சைட்டின் அமிலத்தன்மை மிகவும் பலவீனமாக வெளிப்படுத்தப்படுகிறது மற்றும் முக்கியமாக காரம் உருகும்போது எதிர்வினையின் போது வெளிப்படுகிறது: டான்டலம் அணு ஆக்சிஜனேற்றம் நியோபியம்
Ta2O5 + 2NaOH = 2NaTaO3 + H2O
அல்லது கார்பனேட்டுகள்:
Ta2O5 + 3Na2CO3 = 2Na3TaO4 + 3CO2
-4, -5 ஆக்சிஜனேற்ற நிலையில் டான்டலம் கொண்ட உப்புகள் பல வகைகளாக இருக்கலாம்: மெட்டான்டலேட்டுகள் NaTaO3, orthotantalates Na3TaO4, ஆனால் பாலியன்கள் penta- மற்றும் hexa- உள்ளன, நீர் மூலக்கூறுகள், 7- மற்றும் 8- உடன் படிகமாக்குகின்றன. ஐந்து-சார்ந்த டான்டலம் TaO3+ கேஷனை உருவாக்குகிறது மற்றும் அமிலங்களுடனான எதிர்வினைகளில் TaO(NO3)3 அல்லது Nb2O5(SO4)3 உப்புகள், வெனடியம் அயன் VO2+ அறிமுகப்படுத்திய பக்க துணைக்குழுவின் "பாரம்பரியத்தை" தொடர்கிறது.
1000°C இல் Ta2O5 குளோரின் மற்றும் ஹைட்ரஜன் குளோரைடுடன் வினைபுரிகிறது:
Ta2O5+ 10HC1==2ТаС15+5Н2О
இதன் விளைவாக, டான்டலம் (V) ஆக்சைடு ஒரு தளத்தின் பண்புகளை விட உயர்ந்த அமில பண்புகளுடன் ஆம்போடெரிசிட்டியால் வகைப்படுத்தப்படுகிறது என்று வாதிடலாம்.
டான்டலம் டெட்ராக்ளோரைட்டின் அமிலக் கரைசல்களை நடுநிலையாக்குவதன் மூலம் டான்டலம் (V) ஆக்சைடுக்கு தொடர்புடைய ஹைட்ராக்சைடு பெறப்படுகிறது. இந்த எதிர்வினை +4 ஆக்சிஜனேற்ற நிலையின் உறுதியற்ற தன்மையையும் உறுதிப்படுத்துகிறது.
குறைந்த ஆக்சிஜனேற்ற நிலைகளில், மிகவும் நிலையான சேர்மங்கள் ஹைலைடுகள் (படம் 3 ஐப் பார்க்கவும்) அவற்றைப் பெறுவதற்கான எளிதான வழி பைரிடின் வளாகங்கள் ஆகும். Pentahalides TaX5 (இங்கு X என்பது C1, Br, I) Pyridine ஆல் எளிதாகக் குறைக்கப்பட்டு (Py ஆல் குறிக்கப்படுகிறது) MX4(Py)2 கலவையை உருவாக்குகிறது.
டான்டலம் உப்புகள். ஆறாவது துணைக்குழுவின் உப்புகள் முக்கியமாக நிறமற்ற படிகங்கள் அல்லது வெள்ளை பொடிகள். அவற்றில் பல மிகவும் ஹைக்ரோஸ்கோபிக் மற்றும் காற்றில் பரவுகின்றன. இந்த உலோகங்களின் ஆக்சைடுகள் ஆம்போடெரிக் பண்புகளைக் கொண்டுள்ளன, எனவே அவற்றின் உப்புகளில் பெரும்பாலானவை எளிதில் நீராற்பகுப்பு செய்யப்படுகின்றன, அவை தண்ணீரில் சிறிது அல்லது முற்றிலும் கரையாத அடிப்படை உப்புகளாக மாறும்.இந்த உலோகங்கள் அனான்களின் ஒரு பகுதியாக இருக்கும் (உதாரணமாக, நியோபேட்டுகள் மற்றும் டான்டலேட்டுகள்) உப்புகளும் அறியப்படுகின்றன. ) நீரேற்றம் மற்றும் நீரிழப்பு. இந்த வகுப்பின் அனைத்து வினையூக்கிகளும் தண்ணீருடன் வலுவான உறவைக் கொண்டுள்ளன. பி வகுப்பின் முக்கிய பிரதிநிதி அலுமினா. டான்டலம், சிர்கோனியம் அல்லது ஹாஃப்னியம் ஆக்சைடுகளுடன் கூடிய அலுமினோசிலிகேட் ஜெல் மற்றும் சிலிக்கா ஜெல் போன்ற கேரியர்களிலும் பாஸ்போரிக் அமிலம் அல்லது அதன் அமில உப்புகள் பயன்படுத்தப்படுகின்றன. டான்டலம் மற்றும் நியோபியத்தை பிரித்தெடுத்தல் மூலம் பிரிப்பதற்கான முதல் வேலைகளில், ஹைட்ரோகுளோரிக் அமிலம்-சைலீன்-மெத்தில்டியோக்டைலமைன் (1952), அத்துடன் ஹைட்ரோகுளோரிக் அமிலம்-ஹைட்ரோபுளோரிக் அமிலம்-டைசோபிரைல் கீட்டோன் (1953) ஆகிய அமைப்புகள் முன்மொழியப்பட்டன. இரண்டு உலோகங்களும் அக்வஸ் அமிலக் கரைசல்களில் உப்புகளாகக் கரைக்கப்படுகின்றன, பின்னர் டான்டலம் ஒரு கரிம கரைப்பான் மூலம் பிரித்தெடுக்கப்படுகிறது. அமைப்பில் 6/W சல்பூரிக் அமிலம்--9 ஐ ஹைட்ரோபுளோரிக் அமிலம்
7. செயற்கை இழைகள் தயாரிப்பில் நூல்கள் வரைவதற்கு டான்டலம் பயன்படுத்தப்படுகிறது. முன்னதாக, இத்தகைய சாவுகள் பிளாட்டினம் மற்றும் தங்கத்தால் செய்யப்பட்டன. கடினமான உலோகக் கலவைகள் டான்டலம் கார்பைடிலிருந்து நிக்கலுடன் சிமென்ட் சேர்க்கையாக தயாரிக்கப்படுகின்றன. அவை மிகவும் கடினமானவை, அவை வைரத்தில் கூட கீறல்களை விடுகின்றன, இது கடினத்தன்மையின் தரமாகக் கருதப்படுகிறது.
சூப்பர் கண்டக்டிங் நிலைக்கு மாறுவதற்கான முக்கியமான வெப்பநிலையின் அடிப்படையில் முதல் இடம் நியோபியம் ஜெர்மானைடு Nb3Ge க்கு வழங்கப்பட்டது. இதன் முக்கிய வெப்பநிலை 23.2K (சுமார் -250 °C) ஆகும். மற்றொரு சேர்மமான நியோபியம் ஸ்டானைடு -255 டிகிரி செல்சியஸ் குறைந்த வெப்பநிலையில் சூப்பர் கண்டக்டராக மாறுகிறது. இந்த உண்மையை இன்னும் முழுமையாகப் புரிந்துகொள்ள, பெரும்பாலான சூப்பர் கண்டக்டர்கள் திரவ ஹீலியத்தின் (2.172 K) வெப்பநிலைகளுக்கு மட்டுமே அறியப்படுகின்றன என்பதை நாங்கள் சுட்டிக்காட்டுகிறோம். நியோபியம் பொருட்களிலிருந்து தயாரிக்கப்படும் சூப்பர் கண்டக்டர்கள் மிகவும் சக்திவாய்ந்த காந்தப்புலங்களை உருவாக்கும் காந்த சுருள்களை உருவாக்குவதை சாத்தியமாக்குகின்றன. 16 செ.மீ விட்டம் மற்றும் 11 செ.மீ உயரம் கொண்ட ஒரு காந்தம், முறுக்கு என்பது அத்தகைய பொருட்களால் செய்யப்பட்ட நாடா ஆகும், இது மிகப்பெரிய தீவிரத்தன்மை கொண்ட ஒரு புலத்தை உருவாக்கும் திறன் கொண்டது. காந்தத்தை ஒரு சூப்பர் கண்டக்டிங் நிலைக்கு மாற்றுவது மட்டுமே அவசியம், அதாவது அதை குளிர்விப்பது மற்றும் குறைந்த வெப்பநிலைக்கு குளிர்விப்பது நிச்சயமாக எளிதானது.
வெல்டிங்கில் நியோபியத்தின் பங்கு முக்கியமானது. சாதாரண எஃகு வெல்டிங் செய்யும் போது, இந்த செயல்முறை எந்த குறிப்பிட்ட சிரமங்களையும் முன்வைக்கவில்லை மற்றும் எந்த சிரமத்தையும் உருவாக்கவில்லை. இருப்பினும், சிக்கலான இரசாயன கலவையின் சிறப்பு இரும்புகளால் செய்யப்பட்ட கட்டமைப்புகளை பற்றவைக்கத் தொடங்கியபோது, பற்றவைக்கப்பட்ட உலோகத்தின் பல மதிப்புமிக்க குணங்களை வெல்ட்கள் இழக்கத் தொடங்கின. மின்முனைகளின் கலவையில் மாற்றங்கள், அல்லது வெல்டிங் இயந்திரங்களின் வடிவமைப்புகளில் மேம்பாடுகள் அல்லது மந்த வாயுக்களின் வளிமண்டலத்தில் வெல்டிங் ஆகியவை எந்த விளைவையும் ஏற்படுத்தவில்லை. இங்குதான் நியோபியம் மீட்புக்கு வருகிறது. நியோபியம் ஒரு சிறிய சேர்க்கையாக அறிமுகப்படுத்தப்பட்ட எஃகு, வெல்டின் தரத்திற்கு பயப்படாமல் பற்றவைக்கப்படலாம் (படம் 4). வெல்டிங்கின் பலவீனம் வெல்டிங்கின் போது உருவாகும் கார்பைடுகளால் ஏற்படுகிறது, ஆனால் நியோபியத்தின் திறன் கார்பனுடன் ஒன்றிணைந்து, உலோகக் கலவைகளின் பண்புகளை மீறும் மற்ற உலோகங்களின் கார்பைடுகளை உருவாக்குவதைத் தடுக்கிறது. டான்டலம் போன்ற நியோபியத்தின் கார்பைடுகள் போதுமான பாகுத்தன்மையைக் கொண்டுள்ளன. அழுத்தம் மற்றும் ஆக்கிரமிப்பு சூழல்களில் செயல்படும் கொதிகலன்கள் மற்றும் எரிவாயு விசையாழிகளை வெல்டிங் செய்யும் போது இது குறிப்பாக மதிப்புமிக்கது.
நியோபியம் மற்றும் டான்டலம் ஆகியவை ஹைட்ரஜன், ஆக்ஸிஜன் மற்றும் நைட்ரஜன் போன்ற குறிப்பிடத்தக்க அளவு வாயுக்களை உறிஞ்சும் திறன் கொண்டவை. அறை வெப்பநிலையில், 1 கிராம் நியோபியம் 100 செமீ3 ஹைட்ரஜனை உறிஞ்சும் திறன் கொண்டது. ஆனால் வலுவான வெப்பத்துடன் கூட, இந்த சொத்து நடைமுறையில் பலவீனமடையாது. 500 டிகிரி செல்சியஸ் வெப்பநிலையில், நியோபியம் இன்னும் 75 செமீ3 ஹைட்ரஜனையும், டான்டலம் 10 மடங்கு அதிகமாகவும் உறிஞ்சும். இந்த சொத்து அதிக வெற்றிடங்களை உருவாக்க அல்லது அதிக வெப்பநிலையில் துல்லியமான பண்புகளை பராமரிக்க தேவையான மின்னணு சாதனங்களில் பயன்படுத்தப்படுகிறது. நியோபியம் மற்றும் டான்டலம், கடற்பாசி போன்ற பகுதிகளின் மேற்பரப்பில் வைக்கப்பட்டு, வாயுக்களை உறிஞ்சி, சாதனங்களின் நிலையான செயல்பாட்டை உறுதி செய்கிறது. இந்த உலோகங்களின் உதவியுடன் மறுசீரமைப்பு அறுவை சிகிச்சை பெரும் வெற்றியை அடைந்துள்ளது. மருத்துவ நடைமுறையில் டான்டலத்தின் தட்டுகள் மட்டுமல்ல, டான்டலம் மற்றும் நியோபியம் நூல்களும் அடங்கும். கிழிந்த தசைநாண்கள், இரத்த நாளங்கள் மற்றும் நரம்புகளை ஒன்றாக இணைக்க அறுவை சிகிச்சை நிபுணர்கள் வெற்றிகரமாக இத்தகைய நூல்களைப் பயன்படுத்துகின்றனர். டான்டலம் "நூல்" தசை வலிமையை ஈடுசெய்ய உதவுகிறது. அதன் உதவியுடன், அறுவைசிகிச்சைக்குப் பிறகு வயிற்று குழியின் சுவர்களை அறுவை சிகிச்சை நிபுணர்கள் வலுப்படுத்துகிறார்கள். டான்டலம் அணுக்களுக்கு இடையே மிகவும் வலுவான பிணைப்புகளைக் கொண்டுள்ளது. இது அதன் மிக உயர்ந்த உருகும் மற்றும் கொதிநிலைகளை ஏற்படுத்துகிறது. இயந்திர குணங்கள் மற்றும் இரசாயன எதிர்ப்பு ஆகியவை டான்டலத்தை பிளாட்டினத்திற்கு நெருக்கமாக கொண்டு வருகின்றன. இரசாயனத் தொழில் டான்டலம் குணங்களின் இந்த சாதகமான கலவையைப் பயன்படுத்துகிறது. ஆக்கிரமிப்பு சூழல்களுடன் தொடர்பு கொள்ளும் இரசாயன ஆலைகள், வெப்பமூட்டும் மற்றும் குளிரூட்டும் சாதனங்களின் அமில-எதிர்ப்பு உபகரணங்களுக்கான பாகங்களைத் தயாரிக்க இது பயன்படுகிறது.
வேகமாக வளரும் அணு ஆற்றல் துறையில் நியோபியத்தின் இரண்டு பண்புகள் பயன்படுத்தப்படுகின்றன. நியோபியம் வெப்ப நியூட்ரான்களுக்கு அற்புதமான "வெளிப்படைத்தன்மையை" கொண்டுள்ளது, அதாவது, நியூட்ரான்களுடன் நடைமுறையில் வினைபுரியாமல் உலோகத்தின் ஒரு அடுக்கு வழியாக அவற்றை அனுப்ப முடியும். நியோபியத்தின் செயற்கை கதிரியக்கம் (கதிரியக்கப் பொருட்களுடன் தொடர்பு கொண்டு உற்பத்தி செய்யப்படுகிறது) குறைவாக உள்ளது. எனவே, கதிரியக்க கழிவுகளை சேமிப்பதற்கான கொள்கலன்கள் மற்றும் அவற்றின் செயலாக்கத்திற்கான நிறுவல்களை உருவாக்க இதைப் பயன்படுத்தலாம். நியோபியத்தின் மற்றொரு சமமான மதிப்புமிக்க (அணு உலைக்கான) பண்பு 1000 வெப்பநிலையில் கூட யுரேனியம் மற்றும் பிற உலோகங்களுடன் குறிப்பிடத்தக்க தொடர்பு இல்லாதது ஆகும். °C.சில வகையான அணு உலைகளில் குளிரூட்டிகளாகப் பயன்படுத்தப்படும் உருகிய சோடியம் மற்றும் பொட்டாசியம், நியோபியம் குழாய்கள் வழியாக எந்தத் தீங்கும் விளைவிக்காமல் சுதந்திரமாகச் சுற்றும்.
உலோக டான்டலம்மிக சமீபத்தில், அதாவது 1802 இல் திறக்கப்பட்டது. ஸ்வீடிஷ் வேதியியலாளர் ஏ.ஜி இந்த உலோகத்தைக் கண்டுபிடிக்கும் அளவுக்கு அதிர்ஷ்டசாலி. எக்பெர்க். ஸ்காண்டிநேவிய நாடுகளில் கண்டுபிடிக்கப்பட்ட இரண்டு புதிய தாதுக்களைப் படிக்கும் போது, அறியப்பட்ட கூறுகளுக்கு கூடுதலாக, அவை முன்னர் படிக்கப்படாதவற்றையும் கொண்டிருக்கின்றன. விஞ்ஞானியால் உலோகத்தை கனிமத்திலிருந்து அதன் தூய வடிவத்தில் தனிமைப்படுத்த முடியவில்லை, ஏனெனில் இதில் பெரும் சிரமங்கள் எழுந்தன.
இது சம்பந்தமாக, ஆராயப்படாத உலோகம் பண்டைய கிரேக்கத்தின் புராணங்களிலிருந்து ஒரு ஹீரோவின் பெயரிடப்பட்டது, அதன் பிறகு அது எழுதப்பட்டது. டான்டலஸின் கட்டுக்கதை. இதற்குப் பிறகு, 40 ஆண்டுகளுக்கும் மேலாக, அது நம்பப்பட்டது டான்டலம் மற்றும் நியோபியம்- இவை ஒரே உலோகம். இருப்பினும், ஒரு ஜெர்மன் வேதியியலாளர் உலோகங்களுக்கு இடையிலான வேறுபாட்டை நிரூபித்தார், அதன் பிறகு மற்றொரு ஜெர்மன் டான்டலத்தை அதன் தூய வடிவத்தில் தனிமைப்படுத்தினார், இது 1903 இல் மட்டுமே நடந்தது.
உருட்டப்பட்ட பொருட்களின் தொடர் உற்பத்தி மற்றும் டான்டாலம் தயாரிப்புகள்இரண்டாம் உலகப் போரின் போதுதான் தொடங்கியது. இன்று இந்த உறுப்புக்கு "ஸ்மார்ட் மெட்டல்" என்ற பெயர் வழங்கப்படுகிறது, ஏனெனில் வேகமாக வளரும் மின்னணுவியல் அது இல்லாமல் செய்ய முடியாது.
டான்டலத்தின் விளக்கம் மற்றும் பண்புகள்
டான்டலம்அதிக கடினத்தன்மை மற்றும் அணு அடர்த்தி கொண்ட உலோகமாகும். கால வேதியியல் கூறுகளில், டான்டலம் 73 வது இடத்தில் அமைந்துள்ளது. உலக நடைமுறையில், இந்த உலோகத்தை Ta என்ற இரண்டு எழுத்துக்களின் கலவையால் குறிக்கும் வழக்கம் உள்ளது. வளிமண்டல அழுத்தம் மற்றும் அறை வெப்பநிலையில், டான்டலம் ஒரு சிறப்பியல்பு வெள்ளி-உலோக நிறத்தைக் கொண்டுள்ளது. உலோகத்தின் மேற்பரப்பில் உருவாகும் ஆக்சைடு படம் அதற்கு ஈய நிறத்தைக் கொடுக்கும்.
டான்டலம் உறுப்புஅறை வெப்பநிலையில் செயலற்றது. 280 டிகிரிக்கு மேல் வெப்பநிலையில் மட்டுமே இந்த உலோகத்தின் மேற்பரப்பில் காற்றின் ஆக்சிஜனேற்றம் சாத்தியமாகும். டான்டலம் காற்றை விட 30 டிகிரி குறைந்த வெப்பநிலையில் ஆலசன்களுடன் வினைபுரிகிறது. இந்த வழக்கில், மேற்பரப்பில் ஒரு பாதுகாப்பு படம் உருவாகிறது, இது உலோகத்தின் ஆழம் முழுவதும் ஆக்ஸிஜனேற்ற கூறுகளின் மேலும் ஊடுருவலைத் தடுக்கிறது.

டான்டலம் இரசாயன உறுப்புஅதிக உருகுநிலையுடன். எனவே, இது 3290 K, மற்றும் கொதிநிலை 5731 K ஐ அடைகிறது. அதிக அடர்த்தி (16.7 g/cm3) மற்றும் கடினத்தன்மை இருந்தபோதிலும், இது மிகவும் பிளாஸ்டிக் ஆகும். டக்டிலிட்டி அடிப்படையில், டான்டலத்தை ஒப்பிடலாம். தூய உலோகம் வேலை செய்ய மிகவும் எளிதானது மற்றும் வசதியானது.
இது இயந்திரம் எளிதானது, எடுத்துக்காட்டாக, அதை 1-10 மைக்ரான் தடிமன் வரை உருட்டலாம். டான்டலம் பரமகாந்தம் என்பதையும் கவனத்தில் கொள்ள வேண்டும். இந்த உலோகத்தின் ஒரு சுவாரஸ்யமான அம்சம் 800 டிகிரி வெப்பநிலையில் தோன்றத் தொடங்குகிறது: டான்டலம் அதன் வாயு அளவுகளில் 740 ஐ உறிஞ்சுகிறது.
உலக நடைமுறையில் ஏற்கனவே பல உண்மைகள் உள்ளன, அவை மிகவும் ஆக்கிரோஷமான சூழலில் இந்த உலோகத்தின் சிறந்த ஆயுளைக் குறிக்கின்றன. உதாரணமாக, டான்டலம் 70% நைட்ரிக் அமிலத்தால் கூட சேதமடையாது என்பது அறியப்படுகிறது. 150 டிகிரி வரை சல்பூரிக் அமிலம் அரிக்கும் அழிவுக்கு வழிவகுக்காது, ஆனால் ஏற்கனவே 200 டிகிரியில் உலோகம் 0.006 மிமீ / ஆண்டு என்ற விகிதத்தில் கரைக்கத் தொடங்கும்.
ஆஸ்டெனிடிக் துருப்பிடிக்காத இரும்புகளை விட டான்டலம் மிகவும் எதிர்ப்புத் திறன் கொண்டது என்பதையும் சில உற்பத்தி உண்மைகள் குறிப்பிடுகின்றன. எனவே, அறியப்பட்ட வழக்கு உள்ளது டான்டலம் பாகங்கள்துருப்பிடிக்காத எஃகு பாகங்களை விட 20 ஆண்டுகள் நீடித்தது.

மற்றொரு சுவாரஸ்யமான உண்மை என்னவென்றால், டான்டலம் தங்கத்தை வினையூக்கிப் பிரிக்கப் பயன்படுகிறது. கத்தோட்கள் அதிலிருந்து தயாரிக்கப்படுகின்றன, அதன் மீது உன்னத உலோகம் டெபாசிட் செய்யப்படுகிறது, பின்னர் அக்வா ரெஜியாவுடன் கழுவப்படுகிறது. அதே நேரத்தில், கேத்தோடு மற்றும் டான்டலம், அமிலங்களுக்கு அதன் சிறந்த எதிர்ப்பின் காரணமாக, அப்படியே இருக்கும்.
டான்டலத்தின் பயன்பாடுகள்
நீண்ட காலத்திற்கு முன்பு, இந்த உலோகம் ஒளிரும் விளக்குகளில் இழைகளை உற்பத்தி செய்ய பயன்படுத்தப்பட்டது. இன்று டான்டலம் மற்றும் டான்டலம் உலோகக்கலவைகள்பின்வரும் தொழில்கள் மற்றும் தயாரிப்புகளில் பயன்படுத்தப்படுகிறது:
- வெப்ப-எதிர்ப்பு மற்றும் அரிப்பை எதிர்க்கும் உலோகக் கலவைகளை உருக்கும் போது (எடுத்துக்காட்டாக, விமான இயந்திர பாகங்கள்);
- இரசாயனத் தொழிலில் அரிப்பை எதிர்க்கும் கருவிகளை உருவாக்குதல்;
- அரிதான பூமி உலோகங்களை உற்பத்தி செய்வதற்கான உலோகவியல் உற்பத்தியில்;
- அணு உலைகளின் கட்டுமானத்தின் போது (டான்டலம் சீசியம் நீராவிக்கு மிகவும் எதிர்ப்பு உலோகம்);
- அதன் உயர் உயிர் இணக்கத்தன்மை காரணமாக, டான்டலம் மருத்துவ உள்வைப்புகள் மற்றும் செயற்கை உறுப்புகளின் உற்பத்திக்கு பயன்படுத்தப்படுகிறது;
- சூப்பர் கண்டக்டர்களின் உற்பத்திக்கு - கிரையோட்ரான்கள் (இவை கணினி தொழில்நுட்பத்தின் கூறுகள்);
- குண்டுகள் தயாரிப்பதற்கு இராணுவத் தொழிலில் பயன்படுத்தப்படுகிறது. இந்த உலோகத்தின் பயன்பாடு வெடிமருந்துகளின் ஊடுருவல் சக்தியை அதிகரிக்கிறது;
- மிகவும் திறமையான குறைந்த மின்னழுத்த மின்தேக்கிகள் டான்டலத்திலிருந்து தயாரிக்கப்படுகின்றன;
- சமீபத்தில், டான்டலம் வணிகத்தில் உறுதியாக நிறுவப்பட்டுள்ளது. இது மேற்பரப்பில் வலுவான ஆக்சைடு படங்களை உருவாக்கும் உலோகத்தின் திறன் காரணமாகும், இது பல்வேறு வண்ணங்கள் மற்றும் நிழல்கள் இருக்கலாம்;
- ஒரு பெரிய எண் டான்டலத்தின் மாற்றங்கள்அணு உலைகளில் குவிகிறது. ஆய்வக அல்லது இராணுவ நோக்கங்களுக்காக, உலோகத்தின் இந்த மாற்றம் காமா கதிர்வீச்சின் ஆதாரமாக பயன்படுத்தப்படலாம்;
- இந்த உலோகமானது வெகுஜனத் தரங்களைத் தயாரிப்பதற்கு பிரதானமாக (பிளாட்டினத்திற்குப் பிறகு) பயன்படுத்தப்படுகிறது, இது அதிகரித்த துல்லியம் கொண்டது;
- சில இடை உலோகம் டான்டலம் கலவைகள்மிக அதிக கடினத்தன்மை மற்றும் வலிமை, அத்துடன் ஆக்சிஜனேற்றத்திற்கு அதிகரித்த எதிர்ப்பு. இந்த கலவைகள் விமான மற்றும் விண்வெளி தொழில்களில் பயன்படுத்தப்படுகின்றன;
- டான்டலம் கார்பைடுகள் அதிகரித்த சிவப்பு எதிர்ப்பைக் கொண்ட வெட்டுக் கருவிகளைத் தயாரிக்கப் பயன்படுத்தப்படுகின்றன. கார்பைடு பொடிகளின் கலவையை சின்டர் செய்வதன் மூலம் கருவி பெறப்படுகிறது. இந்த கருவிகள் மிகவும் கடினமான சூழ்நிலைகளில் பயன்படுத்தப்படுகின்றன, உதாரணமாக, தாள துளையிடுதலின் போது;
- பெண்டாவலன்ட் டான்டாலம் ஆக்சைடுஅணு தொழில்நுட்பத்தில் கண்ணாடியை வெல்டிங் செய்வதற்கு அவசியம்.
டான்டலம் வைப்பு மற்றும் சுரங்கம்
டான்டலம் ஒரு அரிய உலோகம். பூமியின் மேலோட்டத்தில் அதன் அளவு 0.0002% மட்டுமே. இந்த அளவு உலோகத்தின் இரண்டு மாற்றங்களை உள்ளடக்கியது: நிலையான மற்றும் கதிரியக்க. இந்த அரிய உலோகம் அதன் சொந்த சேர்மங்களின் வடிவத்தில் ஏற்படுகிறது மற்றும் பல தாதுக்களின் பகுதியாகும். டான்டலம் ஒரு கனிமத்தில் சேர்க்கப்பட்டால், அது எப்போதும் நியோபியத்துடன் ஒன்றாக இருக்கும்.

டான்டலம் சேர்மங்களின் வைப்புமற்றும் கனிமங்கள் பல நாடுகளில் காணப்படுகின்றன. ஐரோப்பாவில் இந்த தனிமத்தின் மிகப்பெரிய வைப்பு பிரான்சில் அமைந்துள்ளது. ஆப்பிரிக்கக் கண்டத்தில், எகிப்துதான் அதிக டான்டலம் கொண்டது. சீனா மற்றும் தாய்லாந்திலும் இந்த உலோகத்தின் அதிக இருப்பு உள்ளது. சிஐஎஸ், நைஜீரியா, கனடா, ஆஸ்திரேலியா மற்றும் பிற நாடுகளில் சிறிய வைப்புத்தொகைகள் உள்ளன. இருப்பினும், இன்றுவரை கண்டுபிடிக்கப்பட்ட மிகப்பெரிய வைப்புக்கள் ஆஸ்திரேலியாவில் உள்ளன.
உலகில் ஆண்டுதோறும் சுமார் 420 டன் டான்டலம் வெட்டப்படுகிறது. இந்த உலோகத்திற்கான முக்கிய செயலாக்க ஆலைகள் அமெரிக்கா மற்றும் ஜெர்மனியில் அமைந்துள்ளன. இந்த அரிய உலோகத்தின் உற்பத்தியை அதிகரிக்க வேண்டியதன் அவசியத்தை சர்வதேச சமூகம் பிரகடனப்படுத்தி வருகின்றமை குறிப்பிடத்தக்கது. இத்தகைய அறிக்கைகள் முதன்மையாக எலக்ட்ரானிக்ஸ் உற்பத்தியின் அதிகரிப்புடன் தொடர்புடையவை, இதில் இந்த உறுப்பு தீவிரமாக பயன்படுத்தப்படுகிறது.

இதனால், ஒவ்வொரு ஆண்டும் வளர்ந்த துறைகளின் எண்ணிக்கை அதிகரித்து வருகிறது. எடுத்துக்காட்டாக, உலகின் முக்கிய வளரும் துறைகளில், பிரேசில், அமெரிக்கா மற்றும் தென்னாப்பிரிக்காவில் அதிக இடங்கள் சேர்க்கப்பட்டன. இருப்பினும், கடந்த 10 ஆண்டுகளில் தீவிரம் ஏற்பட்டுள்ளது என்பது குறிப்பிடத்தக்கது டான்டலம் உற்பத்தியில் குறைப்பு. 21 ஆம் நூற்றாண்டின் மிகக் குறைந்த உற்பத்தி எண்ணிக்கை 2010 இல் நிகழ்ந்தது.
டான்டலம் விலை
கடந்த 15 ஆண்டுகளில் டான்டலத்தின் விலை மிகவும் ஏற்ற இறக்கமாக உள்ளது. எனவே, 2002-2003 இல் டான்டலம் வாங்கமிகக் குறைந்த விலையில் அது சாத்தியமாகியது. இந்த வருடம் டான்டலம் விலைஒரு கிலோவிற்கு 340 முதல் 375 டாலர்கள் வரை. இன்று ரஷ்யாவில் நீங்கள் வாங்கலாம் டான்டாலம், விலைஒரு கிலோவிற்கு 2950 ரூபிள் ஆகும்.
டான்டலம் என்பது உன்னத குழுவிற்கு சொந்தமான ஒரு சிறப்பு வகை உலோகமாகும். இது 1802 இல் மீண்டும் கண்டுபிடிக்கப்பட்டது, ஆனால் இது ஒரு இளம் உறுப்பு என்று கருதப்படுகிறது. அதன் அரிதான போதிலும், இது நகைகளில் மட்டுமல்ல, தொழில்துறையிலும் பரவலாகப் பயன்படுத்தப்படுகிறது. எலக்ட்ரானிக்ஸில் இது மிகவும் பொதுவானது - கிட்டத்தட்ட ஒவ்வொரு சாதனத்திலும் இது உள்ளது.
இந்த உலோகத்தின் வெகுஜன பயன்பாடு கடந்த நூற்றாண்டின் 40 களில் தொடங்கியது மற்றும் இன்றுவரை தொடர்கிறது. அதன் அதிகரித்த வலிமை பண்புகள் காரணமாக அதன் புகழ் பெற்றது. மேலும், இது பல தனித்துவமான இயற்பியல் மற்றும் வேதியியல் பண்புகளைக் கொண்டுள்ளது.
இயற்பியல் மற்றும் வேதியியல் பண்புகள்
இந்த உலோகத்தின் இயற்பியல் பண்புகளில், உயர் உருகும் புள்ளியை முன்னிலைப்படுத்த வேண்டும், இது 3017 டிகிரி செல்சியஸ் ஆகும், இது பல ஒப்புமைகளிலிருந்து வேறுபடுகிறது. இதன் காரணமாக, தீவிர நிலைமைகளுக்கு அதிகரித்த எதிர்ப்பு தேவைப்படும் பகுதிகளில் இது பயன்படுத்தப்படுகிறது. அதே நேரத்தில், டான்டலத்தின் குணாதிசயங்களில் டக்டிலிட்டி மற்றும் கடினத்தன்மை ஆகியவை அடங்கும், இதன் கலவையானது இயற்கையில் மிகவும் அரிதானது.
டான்டலத்தின் உருகுநிலை 3017 °C ஆகும்.
டான்டலத்தின் மேலே குறிப்பிடப்பட்ட பண்புகள் அதிக முயற்சி இல்லாமல் உலோகத்தை செயலாக்கவும் தேவையான வடிவங்கள் மற்றும் அளவுகளை உருவாக்கவும் உங்களை அனுமதிக்கின்றன. அதிகரித்த பொறுப்பின் கட்டமைப்புகளின் பாகங்கள் மற்றும் வழிமுறைகளை உருவாக்குவதற்கு அணுவின் சிறப்பு அமைப்பு மிகவும் முக்கியமானது. டான்டலம் மோசடி செய்வதற்கும் உருட்டுவதற்கும் நன்றாக உதவுகிறது. இந்த வழக்கில், குளிர் சிதைவு முறையும் வெற்றிகரமாக பயன்படுத்தப்படலாம். உயர் வெப்ப கடத்துத்திறன் முன்னிலைப்படுத்தப்பட வேண்டும்.
அதன் அதிக அடர்த்தி காரணமாக, இந்த உலோகம் சிறிய கியர்கள் மற்றும் மின் சாதனங்களின் பாகங்களைத் தயாரிக்கப் பயன்படுகிறது.
சில சந்தர்ப்பங்களில் இது வாயு உறிஞ்சியாகப் பயன்படுத்தப்படுகிறது. மின்னணு கட்டமைப்பு சிறப்பிக்கப்பட வேண்டும்: ஒரு உலோகம் அதன் இயல்பான நிலையிலும் அதிக வெப்பநிலையிலும் வெவ்வேறு மின் கடத்துத்திறன் பண்புகளைக் கொண்டுள்ளது.
டான்டலம் பாகங்களை சாலிடரிங், வெல்டிங் அல்லது ரிவெட்டிங் மூலம் இணைக்கலாம். வெல்டிங் முறை பெரும்பாலும் பயன்படுத்தப்படுகிறது, ஏனெனில் வெல்டின் தரம் அதிக வலிமை மற்றும் உடல் அழுத்தத்திற்கு எதிர்ப்பால் வகைப்படுத்தப்படுகிறது.
வேதியியல் பண்புகளில், ஆக்சிஜனேற்றம் மற்றும் காரத்திற்கு அதன் உயர் எதிர்ப்பை முன்னிலைப்படுத்துவது மதிப்பு. இருப்பினும், உருகும்போது, அது காரத்திற்கு ஓரளவு எளிதில் பாதிக்கப்படுகிறது. 250 டிகிரிக்கும் குறைவான வெப்பநிலையில் ஆக்சிஜனேற்றம் சாத்தியமற்றது.
இந்த உலோகத்தின் இரசாயன பண்புகள் கண்ணாடிக்கு மிகவும் ஒத்திருக்கிறது. நீங்கள் ஹைட்ரோஃப்ளூரிக் மற்றும் நைட்ரிக் அமிலத்தைப் பயன்படுத்தாவிட்டால், அதை அமிலத்தில் கரைப்பது கிட்டத்தட்ட சாத்தியமற்றது. சல்பூரிக் அமிலத்தின் வெளிப்பாடு கூட உலோகத்தின் கட்டமைப்பு மற்றும் வடிவத்தை பாதிக்காது. ஒரு சிறிய படம் மட்டுமே மேற்பரப்பில் தோன்றும். கடல் நீரில் நீண்ட நேரம் வெளிப்படும் போது இது அழிவுக்கு உட்பட்டது அல்ல.
இயற்கையில் நிகழ்வது மற்றும் டான்டலம் உற்பத்தி
டான்டலம், ஒரு வேதியியல் தனிமமாக, இயற்கையில் மிகவும் அரிதானது, பூமியின் மேலோட்டத்தில் 0.0002% மட்டுமே உள்ளது. இது அதன் தூய வடிவத்தில் மிகவும் அரிதாகவே காணப்படுகிறது, பெரும்பாலும் பல்வேறு தாதுக்களின் கலவையில், மற்றொரு உலோகத்தின் அருகாமையில் - நியோபியம்.
இந்த தனிமத்தின் வைப்பு பல நாடுகளில் காணப்படுகிறது. பிரான்ஸ், எகிப்து, சீனா மற்றும் தாய்லாந்தில் பெரிய வைப்புக்கள் காணப்படுகின்றன. ஆனால் இந்த தனிமத்தின் மிகப்பெரிய வைப்பு ஆஸ்திரேலியாவில் உள்ளது. டான்டலம் ஆண்டுதோறும் 400 டன்களுக்கும் அதிகமான அளவில் வெட்டப்படுகிறது. அதே நேரத்தில், அதன் பயன்பாட்டின் தேவை தொடர்ந்து வளர்ந்து வருகிறது, இது இந்த உலோகத்தைப் பயன்படுத்தி உற்பத்தி செய்யப்படும் மின் உபகரணங்களின் அளவின் அதிகரிப்புடன் தொடர்புடையது. இதன் அடிப்படையில், புதிய வைப்புத்தொகைகளின் நிலையான வளர்ச்சி உள்ளது.
நம் நாட்டில், டான்டலம் உற்பத்தி சோலிகாம்ஸ்க் மெக்னீசியம் ஆலையில் குவிந்துள்ளது. லோபரைட் செறிவுகளைச் செயலாக்கிய பிறகு உலோகம் பெறப்படுகிறது. மற்ற நாடுகளில், ரூட்டில், ஸ்ட்ரூரைட், டான்டலைட் மற்றும் கொலம்பைட் போன்ற பிற கனிமங்களும் பயன்படுத்தப்படுகின்றன.
உலகில் இந்த உலோகத்தின் மிகப்பெரிய உற்பத்தியாளர்கள் அமெரிக்கா, ஜப்பான் மற்றும் சீனா. உலகளாவிய உற்பத்தியாளர்களின் எண்ணிக்கை 40 நிறுவனங்களுக்கு மேல் இல்லை. விலை - ஒரு கிலோவிற்கு 1000 டாலர்கள்.
டான்டலம் அடிப்படையிலான உலோகக்கலவைகள்
அதன் சிறப்பு இயற்பியல் பண்புகள் காரணமாக, அதன் தூய வடிவத்தில் இந்த உலோகம் பெரும்பாலும் தொழில்துறையில் பயன்படுத்தப்படுகிறது. இருப்பினும், அதிக வெப்பநிலைக்கு வலிமை மற்றும் எதிர்ப்பை அதிகரிக்க, அதன் அடிப்படையில் உலோகக் கலவைகள் பயன்படுத்தப்படலாம் மற்றும் பொருத்தமான கலவை கூறுகளை சேர்க்கலாம்.
டான்டலம் கலவைகள் சுமார் 1700 டிகிரி வெப்பநிலையில் திடமாக இருக்கும். ஆற்றல் துறை, இரசாயனத் தொழில், உயர் துல்லியமான கருவிகளின் உற்பத்தி மற்றும் உலோகம் ஆகியவற்றில் டான்டலம் கலவைகளைப் பயன்படுத்தும் போது இது அவசியம். பெரும்பாலும், விண்வெளி ராக்கெட்டுகளின் கட்டுமானத்தில் பல்வேறு உலோகக் கலவைகள் பயன்படுத்தப்படுகின்றன.
பயன்படுத்தப்படும் கலப்பு கூறுகளின் வகை, தேவையான இறுதி பண்புகளைப் பொறுத்தது. வேலையின் தரத்தை மேம்படுத்த, அலாய் மேம்பட்ட டக்டிலிட்டி பண்புகளை வழங்கும் கூறுகள் பயன்படுத்தப்படுகின்றன.
உலோகக் கலவைகளில் உள்ள டான்டலம் ஒரு தளமாக அல்ல, ஆனால் ஒரு கலவை கூறுகளாகப் பயன்படுத்தப்படுகிறது என்பதை கவனத்தில் கொள்ள வேண்டும். பல்வேறு பொருட்களுடன் அதன் கூடுதலாக அதிக வெப்பநிலை மற்றும் அரிப்புக்கு எதிர்ப்பை அதிகரிக்கிறது.
டான்டலம் மின்தேக்கி சுற்று
டான்டலம் TAV-10 என்பது இந்த உலோகத்தின் அடிப்படையில் பரவலாகப் பயன்படுத்தப்படும் ஒரு கலவையாகும். இது டங்ஸ்டனைச் சேர்த்து உற்பத்தி செய்யப்படுகிறது, இதன் அளவு சுமார் 10% ஆகும். இது மேம்பட்ட வெப்ப எதிர்ப்பைக் கொண்ட ஒரு பொருளை விளைவிக்கிறது. இது வெப்பமூட்டும் கூறுகளின் உற்பத்திக்கும் மருத்துவ நோக்கங்களுக்காகவும் பயன்படுத்தப்படுகிறது, ஏனெனில் அதன் கூறுகள் மனித தோலை எரிச்சலூட்டுவதில்லை.
டான்டலத்தின் பயன்பாடுகள்
டான்டலத்தின் பயன்பாடு ஒரு பகுதிக்கு மட்டும் அல்ல. டான்டலம் தயாரிப்புகள் மிகவும் பரவலாகப் பயன்படுத்தப்படும் பகுதிகளை முன்னிலைப்படுத்துவது மதிப்பு:
- உலோகவியல். இந்த உலோகத்தின் கிட்டத்தட்ட பாதி உலோகவியல் துறையில் பயன்படுத்தப்படுகிறது. பல்வேறு உலோகக்கலவைகளை உருவாக்குவது எளிதானது, குறிப்பாக அதிக வெப்பநிலையை எதிர்க்கும் அரிப்பு எதிர்ப்பு எஃகு தரங்களை உருவாக்குவது இதற்குக் காரணம். அதிகரித்த வலிமை மற்றும் வெப்ப எதிர்ப்பு தேவைப்படும் பல்வேறு துறைகளில் டான்டலம் கம்பி பயன்படுத்தப்படுகிறது. டான்டலம் கார்பைடு, பயனற்ற உலோகங்களுக்கான சிலுவைகள் தயாரிப்பிலும் பரவலாகப் பயன்படுத்தப்படுகிறது.
- மின் பொறியியல். சுமார் 25% மின் பொறியியல் மற்றும் மின் சாதனங்களின் உற்பத்தியில் பயன்படுத்தப்படுகிறது. இந்த உறுப்பைப் பயன்படுத்தும் மின்தேக்கிகள் அதிகரித்த இயக்க நிலைத்தன்மையால் வகைப்படுத்தப்படுகின்றன. மேலும், மின்தேக்கியின் மேற்பரப்பு அழிக்கப்பட்டால், டான்டலம் ஆக்சைட்டின் ஒரு படம் உருவாகிறது, இது அதைப் பாதுகாக்கிறது. அனோட்கள், கேத்தோட்கள், விளக்குகள் மற்றும் பிற உலோக பாகங்கள் போன்ற கூறுகளையும் நீங்கள் முன்னிலைப்படுத்த வேண்டும், அவை அதன் அடிப்படையில் தயாரிக்கப்படுகின்றன.
- இரசாயன தொழில். உற்பத்தி செய்யப்படும் அளவின் ஐந்தில் ஒரு பங்கு இரசாயனத் தொழிலில் பயன்படுத்தப்படுகிறது. இது பெரும்பாலான அமிலங்கள், உப்புகள் மற்றும் காரங்களுக்கு எதிர்ப்புத் திறன் கொண்டது என்பதே இதற்குக் காரணம்.
- மருந்து. மருத்துவத்தில் டான்டலம் எலும்பு மற்றும் பிளாஸ்டிக் அறுவை சிகிச்சை போன்ற தொழில்களில் பயன்படுத்தப்படுகிறது. இந்த பொருளிலிருந்து தயாரிக்கப்படும் கூறுகள் கரிம திசுக்களை எரிச்சலடையச் செய்யாமல் அதிகரித்த வலிமையை அடைய எலும்புகளைக் கட்டுவதற்குப் பயன்படுத்தப்படுகின்றன.
- இராணுவக் கோளம். இராணுவத் துறையில், டான்டலம் இலக்குகள் மற்றும் ஒட்டுமொத்த ஏவுகணைகளுக்கான குண்டுகள் தயாரிக்கப்படுகின்றன.
- கருவிகள். இந்த உலோகமானது துல்லியமான கருவிகள், கட்டுப்பாட்டு உபகரணங்கள் மற்றும் பல்வேறு உதரவிதானங்கள், அத்துடன் வெற்றிட கருவிகள் ஆகியவற்றின் உற்பத்திக்கு பயன்படுத்தப்படுகிறது, ஏனெனில் இது அதன் வாயு உறிஞ்சுதல் பண்புகளால் வேறுபடுகிறது.
- அணு ஆற்றல். இந்த பகுதியில், உலோகம் வெப்பப் பரிமாற்றியாக செயல்படுகிறது.
டான்டலத்தின் பயன்பாட்டின் நோக்கம் அதன் உற்பத்தியின் சிறிய அளவால் மட்டுமே வரையறுக்கப்பட்டுள்ளது என்பதை கவனத்தில் கொள்ள வேண்டும். உற்பத்தி அளவு அதிகரித்தால், பயன்பாட்டின் நோக்கம் கணிசமாக விரிவடையும்.
- மேற்பரப்பு பதற்றத்தை தீர்மானிக்கும் சிக்கலில் ஒரு திரவ துளியின் விளிம்பை தனிமைப்படுத்துதல் ஒரு துளியின் விளிம்பை தனிமைப்படுத்துதல்
- கால்சியம் பெராக்சைடு தயாரிக்கும் முறை
- ஃபியோ நிறம். இரசாயன பண்புகள். பயனற்ற கருப்பு பைரோபோரிக் தூள், தண்ணீரில் கரையாதது. இரும்பு பெறுவதற்கான முறைகள்
- சோடியம் தியோசல்பேட் Natrii thiosulfas (ln) தியோசல்பேட் இரசாயன சூத்திரம்
- இரும்பை தீர்மானிக்க ரோடனைடு முறை
- பேக்கிங் சோடா: சூத்திரம், பயன்பாடு
- கார்பனேட்டுகள். பேக்கிங் சோடா ஃபார்முலா. பேக்கிங் சோடா: சூத்திரம், பயன்பாடு மனிதர்களுக்கான பேக்கிங் சோடாவின் பாதுகாப்பு
- நோய், அறிகுறிகள், சிகிச்சையின் விளக்கம்
- கல்லீரல் நோய்கள்: காரணங்கள், வகைகள், அறிகுறிகள் மற்றும் தடுப்பு கல்லீரலில் வைரஸ் என்றால் என்ன
- ஹெல்மின்திக் தொற்று: காரணங்கள், அறிகுறிகள், சிகிச்சை, தடுப்பு
- நாட்டுப்புற வைத்தியம்
- உணவு நொதித்தல் மற்றும் அதன் முக்கியத்துவம்
- பார்மகோகினெடிக்ஸ் மற்றும் உயிர் கிடைக்கும் தன்மை பற்றிய ஆய்வு - ஜர்னல் ஆஃப் பார்மகோகினெடிக்ஸ் மற்றும் பார்மகோடைனமிக்ஸ் உயர் செயல்திறன் திரவ நிறமூர்த்தம்
- சோதனை வேலை குளோரோஃபார்ம் குளோரோஃபார்ம் வீட்டில்
- உன்னத வாயுக்கள் மற்றும் அவற்றின் பண்புகள் நோபல் வாயுக்கள் இந்த வாயுக்களின் செயலற்ற தன்மையை ஏற்படுத்துகின்றன
- ராமன் மற்றும் என்ஐஆர் ஸ்பெக்ட்ரோஸ்கோபி என்ஐஆர் ஸ்பெக்ட்ரோமெட்ரியின் சிக்கல்கள் மற்றும் அவற்றை எவ்வாறு தீர்ப்பது
- டான்டலத்தின் பக்க சிறப்புகள்
- டான்டலம் என்றால் என்ன, அது எங்கே பயன்படுத்தப்படுகிறது?
- என்சைம் செயல்பாட்டின் மூலக்கூறு விளைவுகள்
- கர்ப்பப்பை வாய் டிஸ்ப்ளாசியா: முதல் அறிகுறிகள், அறிகுறிகள் மற்றும் சிகிச்சை