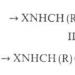Төмрийн роданид 3. Төмрийг тодорхойлох роданидын арга
Энэ арга нь төмрийн ион ба тиоцианатын ионуудаас үүссэн цогцолборуудын дарс-улаан өнгөний шинж чанарыг тодорхойлоход суурилдаг. Эдгээр цогцолборууд нь тогтворгүй байдаг тул цогцолборын диссоциацийг дарахын тулд их хэмжээний тиоцианатын ионууд шаардлагатай байдаг. Төмрийн төмрийн ионуудын тиоцианатын ионуудтай харилцан үйлчлэх үйл явц (1) тэгшитгэлийн дагуу явагдана.
|
Fe 3+ + 6 NH 4 CNS = 6NH 4 + + 3- |
3-аас гадна бусад, бага эрчимтэй өнгөт цогцолбор үүсч болохыг анхаарч үзэх хэрэгтэй, тиймээс аммонийн тиоцианатын концентраци нь шинжилгээнд хамрагдсан болон стандарт уусмалд ижил байх ёстой. Тодорхойлолтод тиоцианатын анионыг исэлдүүлдэг хүчтэй исэлдүүлэгч бодис (калийн перманганат, аммонийн персульфат, устөрөгчийн хэт исэл гэх мэт), түүнчлэн төмрийг (III) төмөр (II) болгон бууруулдаг бодисууд саад болдог. Хамгийн сайн орчин бол азотын хүчил бөгөөд уусмалын бага хүчиллэг нь төмрийн давсны гидролизээс (50 мл уусмал тутамд 1-2 мл концентрацитай азотын хүчил) урьдчилан сэргийлэхэд хангалттай.
Урвалж бодис
Аммонийн роданид (NH4CNS), 10% уусмал;
Азотын хүчил, төвлөрсөн;
Үндсэн стандарт шийдэл. Үндсэн стандарт уусмалыг бэлтгэхийн тулд бага хэмжээний нэрмэл усанд 0.8634 г төмөр аммонийн хөнгөн цагаан уусгана. Хэрэв уусмал тунгалаг болвол хэдэн дусал төвлөрсөн азотын хүчил нэмж, хэмжээг 1 литр болгон тохируулна. Уусмал нь 1 мл тутамд 0.1 мг төмөр агуулдаг;
Ажлын стандарт шийдэл. Ажлын стандарт уусмалыг нөөцийн стандарт уусмалыг 10 дахин шингэлж бэлтгэнэ. Уусмал нь 1 мл тутамд 0.01 мг төмөр агуулдаг.
Ахиц дэвшил
1 ба 5 мл ажлын стандарт уусмал, түүнчлэн 1 нэмнэ; 2.5 ба 5 мл төмрийн үндсэн стандарт уусмалыг нэрмэл усаар тэмдэглээд эзлэхүүнийг тохируулж, 0.1 концентрацитай уусмал авах; 0.5; 1.0; 2.5; ба 5.0 мкг/л тус тус. Бэлтгэсэн уусмал ба 100 мл туршилтын дээжийг 150 мл конус колбонд хийж, колбонд 5 мл концентрацитай HNO 3, 10 мл 10% NH 4 CNS уусмал нэмнэ. Уусмалыг сайтар хольж, 3 минутын дараа ижил урвалж нэмсэн нэрмэл устай харьцуулахад 5 мм-ийн оптик давхаргын зузаантай кюветтүүдийг ашиглан λ = 450 нм долгионы урттай фотометрээр хэмжинэ. Төмрийн массын концентрацийг тохируулсан график ашиглан олно. Абсцисса тэнхлэг дээр төмрийн массын концентрацийг мкг/дм3, ординатын тэнхлэгт харгалзах оптик нягтын утгыг харуулсан тохируулгын графикийг бүтээв.
Дифенилкарбазидыг ашиглан хромын агууламжийг тодорхойлох
Аргын зарчим
Энэ арга нь дифенилкарбазидтай хүчиллэг орчинд хромат ба бихроматуудын харилцан үйлчлэлцэж улаан ягаан өнгийн нэгдэл үүсгэхэд суурилдаг бөгөөд үүнд хром нь Cr(III)-ын бууруулсан хэлбэрээр агуулагдаж, дифенилкарбазид нь дифенилкарбазон болж исэлддэг. Илрүүлэх хязгаар нь 0.02 мг/л байна. Дээж дэх хромын хэмжсэн хэмжээ нь 1 мкг-аас 50 мкг хүртэл байна.
Усны шинжилгээ хийхдээ нэг дээжинд зөвхөн Cr(vi), нөгөөд Cr(iii) ба Cr(vi)-ийн нийт агууламжийг Cr(III) исэлдүүлэн Cr(VI) болгон тодорхойлно. Аммонийн персульфатыг исэлдүүлэгч бодис болгон ашигладаг. Исэлдэлтийн процесс (2) тэгшитгэлийн дагуу явагдана.
|
2Сr 3+ + 3S 2 O 8 2- + 7H 2 O Сr 2 O 7 2- + 6SO 4 2- + 14Н + |
Үр дүнгийн зөрүүг Cr 3+ агуулгыг тодорхойлоход ашигладаг.
Урвалж бодис
Давхар нэрмэл ус (бүх урвалж бэлтгэхэд ашигладаг);
Хүхрийн хүчил, 1: 1;
төвлөрсөн фосфорын хүчил;
Дифенилкарбазид (C 13 H 14 ON 4), ацетон дахь 0.5% уусмал (шинээр бэлтгэсэн ашиглах);
Натрийн гидроксидын уусмал, 10% ба 25%;
Калийн бихромат K 2 Cr 2 O 7-ийн үндсэн стандарт уусмал. Үндсэн стандарт уусмалыг 1500С-т хатаасан 2.8285 г урвалжийг давхар нэрмэл усанд уусгаж, эзэлхүүнийг 1 л (1 мл уусмалд 1 мгКр(VI) агуулна);
Ажлын стандарт уусмал 1. 5 мл үндсэн стандарт уусмалыг 100 мл нэрмэл усаар шингэлж бэлтгэнэ (1 мл уусмалд 50 мкг Cr(VI) агуулагдана);
Ажлын стандарт уусмал 2. 4 мл ажлын стандарт уусмал 1-ээс 100 мл-ийг нэрмэл усаар шингэлж бэлтгэнэ (1 мл уусмалд 2 мкг Cr(VI) агуулагдана).
Шалгалт тохируулгын график байгуулах
0-ийг 100 мл хэмжээст колбонд хийнэ; 0.5; 1.0; 2.0; 3.0; 5.0; 8.0; 10.0 мл ажлын стандарт уусмал 2, уусмалын эзэлхүүнийг 50-60 мл болгож, шүлтийн уусмалаар рН-ийг 8 болгож тохируулж, бүх нийтийн индикатор цаас ашиглан хяналт тавина. 1 мл H 2 SO 4 (1: 1), 0.3 мл H 3 PO 4 нэмээд эзлэхүүнийг 100 мл болгон тохируулна. Үүссэн уусмалууд нь Cr(VI) 0 агууламжтай; 10; 20; 40; 60; 100; 160; 200 мкг/л. Колбо бүрт 2 мл 0.5%-ийн дифенилкарбазидын уусмал нэмж сайтар холино. 10-15 минутын дараа үүссэн уусмалууд. ижил урвалж нэмсэн нэрмэл устай харьцуулахад 30 мм-ийн оптик давхаргын зузаантай кюветтүүдийг ашиглан λ=540 нм долгионы урттай фотометрээр хэмжинэ.
Агуулгын тодорхойлолтКр(VI)
Дээжний эзэлхүүнийг 0.005-0.1 мг хром агуулсан байхаар 100 мл хэмжээст колбонд хийж, хүчил эсвэл шүлтийн уусмалаар рН-ийг 8 болгож, бүх нийтийн индикатор цаас ашиглан хяналт тавина. 1 мл H 2 SO 4 (1: 1), 0.3 мл H 3 PO 4 нэмээд эзэлхүүнийг 100 мл болгож холино. Колбо бүрт 2 мл 0.5%-ийн дифенилкарбазидын уусмал нэмж дахин холино. 10-15 минутын дараа үүссэн уусмалууд. дээр дурдсанчлан фотометрээр хэмжинэ.
Төмрийн чанарын урвал (III)
Төмрийн ионууд (III ) уусмал дахь чанарын урвалыг ашиглан тодорхойлж болно. Тэдгээрийн заримыг нь авч үзье. Туршилтанд төмрийн хлоридын уусмалыг авч үзье ( III).
1. III) - шүлттэй урвал.
Хэрэв уусмалд төмрийн ион байгаа бол ( III ), төмрийн гидроксид үүсдэг ( III ) Fe(OH) 3 . Суурь нь усанд уусдаггүй, хүрэн өнгөтэй. (төмрийн гидроксид ( II ) Fe(OH) 2 . – бас уусдаггүй, гэхдээ саарал ногоон өнгөтэй). Бор тунадас нь анхны уусмалд төмрийн ион байгааг илтгэнэ ( III).
FeCl 3 + 3 NaOH = Fe(OH) 3 ↓+ 3 NaCl
2. Төмрийн ионы чанарын урвал ( III ) - шар цусны давстай урвал.
Шар цусны давс нь калийн гексацианоферрат юмК 4 [ Fe( CN) 6]. (төмрийг тодорхойлохын тулд (II) цусны улаан давс хэрэглэхК 3 [ Fe( CN) 6 ]). Цусан дахь шар давсны уусмалыг төмрийн хлоридын уусмалын нэг хэсэгт нэмнэ. Пруссын хөх*-ийн цэнхэр тунадас нь анхны уусмалд төмрийн ион байгааг илтгэнэ.
3 TO 4 +4 FeCl 3 = К Fe ) ↓ + 12 KCl
3. Төмрийн ионы чанарын урвал ( III ) – калийн тиоцианаттай урвал.
Эхлээд бид туршилтын уусмалыг шингэлнэ - эс тэгвээс бид хүлээгдэж буй өнгийг харахгүй. Төмрийн ион байгаа тохиолдолд (III) калийн тиоцианатыг нэмэхэд улаан бодис үүснэ. Энэ бол төмрийн тиоцианат (III). Грекийн "родеос" -аас Роданид - улаан.
FeCl 3 + 3 КТөв мэдрэлийн систем= Fe( Төв мэдрэлийн систем) 3 + 3 KCl
Пруссын цэнхэр өнгийг 18-р зууны эхээр Берлинд будагч мастер Дисбах санамсаргүйгээр олж авсан. Дисбах нэгэн худалдаачнаас ер бусын калийн (калийн карбонат) худалдаж авсан: энэ калийн уусмалыг төмрийн давс нэмбэл цэнхэр өнгөтэй болжээ. Поташыг шинжилж үзэхэд үхрийн цусаар шохойжуулсан нь тогтоогдсон. Будаг нь даавуунд тохиромжтой: тод, удаан эдэлгээтэй, хямдхан. Удалгүй будаг хийх жор тодорхой болов: калийг малын хатаасан цус, төмрийн үртэстэй хольсон. Ийм хайлшийг уусгаснаар цусны шар давс гаргаж авсан. Пруссын хөхийг одоо хэвлэлийн бэх, өнгөт полимер үйлдвэрлэхэд ашигладаг. .
Тоног төхөөрөмж:колбо, пипетк.
Аюулгүй байдлын урьдчилан сэргийлэх арга хэмжээ . Шүлт ба уусмалуудтай ажиллах дүрмийг дагаж мөрдөнө гексацианоферратууд. Гексацианоферрат уусмалыг төвлөрсөн хүчилтэй харьцахаас зайлсхий.
Туршилтыг тохируулах - Елена Махиненко, текст– Ph.D. Павел Беспалов.
Википедиагийн материал - үнэгүй нэвтэрхий толь
| Төмөр (III) тиоцианат | |
| Нийтлэг байдаг | |
|---|---|
| Системтэй Нэр |
Төмөр (III) тиоцианат |
| Уламжлалт нэрс | төмрийн тиоцианат; тиоцианат төмөр |
| Хими. томъёо | Fe(SCN) 3 |
| Физик шинж чанар | |
| муж | ногоон өнгөтэй улаан талстууд |
| Моляр масс | 230.09 г/ мэнгэ |
| Мэдээллийг өгсөн болно стандарт нөхцөл (25 °C, 100 кПа), өөрөөр заагаагүй бол. | |
Төмөр (III) тиоцианат- органик бус нэгдэл, металлын давс булчирхайТэгээд тиоцианатын хүчил Fe(SCN) 3 томьёотой, усанд уусдаг, үүсгэдэг талст гидрат- улаан талстууд.
Баримт
- Солилцооны урвал:
- Уусмалыг саармагжуулах тиоцианатын хүчилшинээр тарьсан төмрийн (III) гидроксид :
Физик шинж чанар
Төмөр (III) тиоцианат нь талст гидрат Fe(SCN) 3 3H 2 O -ийг үүсгэдэг. парамагнитулаан гигроскопикусанд уусдаг талстууд, этанол , агаарт, уусахад хэцүү нүүрстөрөгчийн дисульфид , бензол , хлороформ , толуол.
Усан уусмалууд нь Fe 6H 2 O dimers агуулдаг.
Химийн шинж чанар
- Бусад металлын тиоцианатуудтай координацын нэгдлүүдийг үүсгэдэг гексатиоцианатоферрат (III), жишээ нь Ли 3 n H 2 O, Na 3 12H 2 O, K 3 4H 2 O, Cs 3 2H 2 O, (NH 4) 3 4H 2 O.
"Төмөр(III) тиоцианат" нийтлэлийн тойм бичнэ үү.
Уран зохиол
- Химийн нэвтэрхий толь бичиг / Редакцийн зөвлөл: Кнунянц И.Л. ба бусад.- М.: Зөвлөлтийн нэвтэрхий толь бичиг, 1990. - Т. 2. - 671 х. - ISBN 5-82270-035-5.
- Рипан Р., Четеану И.Органик бус хими. Металлын хими. - М.: Мир, 1972. - T. 2. - 871 х.
| Энэ нийтлэл бэлтгэхО органик бус бодис. Та төсөл дээр нэмж тусалж чадна. |
Төмрийн (III) тиоцианатын шинж чанарыг харуулсан ишлэл
-Ирээдүйн амьдралд? - гэж хунтайж Андрей давтан хэлсэн боловч Пьер түүнд хариулах цаг өгөөгүй бөгөөд энэ давталтыг үгүйсгэсэн хэрэг гэж хүлээн авсан, ялангуяа хунтайж Андрейгийн өмнөх шашингүй үзэл бодлыг мэддэг байсан тул.– Та дэлхий дээрх сайн сайхан, үнэний хаант улсыг харж чадахгүй гэж хэлж байна. Хэрэв бид амьдралаа бүх зүйлийн төгсгөл гэж үзвэл би түүнийг хараагүй бөгөөд тэр ч харагдахгүй. Дэлхий дээр, яг энэ дэлхий дээр (Пьер талбарт заав) үнэн гэж байдаггүй - бүх зүйл худал, бузар муу юм; харин дэлхий дээр, бүх дэлхийд үнэний хаант улс байдаг бөгөөд бид одоо дэлхийн хүүхдүүд, мөн бүх дэлхийн үүрд мөнх хүүхдүүд юм. Би энэ асар том, эв нэгдэлтэй бүхэл бүтэн нэг хэсэг гэдгээ сэтгэлдээ мэдрэхгүй байна гэж үү. Би Тэнгэрлэг чанар илэрдэг энэ тоо томшгүй олон тооны оршнолуудын дотор - таны хүссэнээр хамгийн дээд хүч - доод оршихуйгаас дээд оршихуй руу нэг алхам, нэг холбоосыг бүрдүүлдэг гэж би мэдрэхгүй байна гэж үү. Хэрэв би харвал ургамлаас хүн рүү хөтөлдөг энэ шатыг тод харвал яагаад энэ шат надтай хамт эвдэрч, цаашаа явахгүй гэж бодох ёстой гэж. Хорвоо дээр юу ч алга болдоггүйн адил би алга болж чадахгүй ч, би үргэлж байх болно, байсаар ч байгаа гэдгээ мэдэрдэг. Надаас гадна миний дээр сүнснүүд амьдардаг, энэ ертөнцөд үнэн байдаг гэдгийг би мэдэрдэг.
"Тийм ээ, энэ бол Малчдын сургаал" гэж хунтайж Андрей хэлэв, "гэхдээ сэтгэл минь энэ бол намайг итгүүлдэг зүйл биш, харин амьдрал, үхэл намайг итгүүлдэг." Хамгийн үнэмшилтэй зүйл бол та өөрт чинь хайртай, чамтай холбоотой, өмнө нь буруутай байсан, өөрийгөө зөвтгөх гэж найдаж байсан (Ханхүү Андрейгийн хоолой чичирч, эргэж харав) гэнэт энэ амьтан зовж шаналж, тарчлаан зовоож, байхаа больсон. ... Яагаад? Хариулт байхгүй байж болохгүй! Тэгээд би түүнийг гэдэгт итгэж байна ... Энэ бол намайг итгүүлж, итгүүлсэн зүйл" гэж хунтайж Андрей хэлэв.
"За, тийм ээ, за" гэж Пьер хэлэв, "би үүнийг хэлж байгаа юм биш үү!"
- Үгүй. Ирээдүйн амьдрал хэрэгтэй гэдэгт маргалдах зүйл биш, харин хүнтэй хөтлөлцөн алхах үед энэ хүн гэнэт хаашаа ч юм алга болж, чи өөрөө урд нь зогсдог гэдгийг л хэлэх гэсэн юм. энэ ангал болон түүн рүү хараарай. Тэгээд би харсан ...
- Тэгэхээр дараа нь! Та тэнд юу байгааг, хэн нэгэн байгааг мэдэх үү? Тэнд ирээдүйн амьдрал бий. Хэн нэгэн бол Бурхан.
Ханхүү Андрей хариулсангүй. Сүйх тэрэг, морьдыг аль хэдийн нөгөө тал руу аваачиж, аль хэдийн хэвтсэн байсан бөгөөд нар аль хэдийн тал талдаа алга болж, үдшийн хяруу гатлага онгоцны ойролцоох шалбааг одод, Пьер, Андрей хоёрыг бүрхэж, тэднийг гайхшруулав. явган зорчигчид, вагончид, тээвэрлэгчид гатлага онгоцон дээр зогсоод ярилцсаар байв.
– Бурхан байгаа бол ирээдүйн амьдрал байгаа бол үнэн, буян гэж бий; Хүний хамгийн дээд аз жаргал бол түүнд хүрэхийн төлөө хичээх явдал юм. Бид амьдрах ёстой, хайрлах ёстой, итгэх ёстой гэж Пьер хэлэв, бид одоо зөвхөн энэ газар нутагт амьдардаггүй, харин тэнд бүх зүйлд амьдарч байсан бөгөөд үүрд мөнх амьдрах болно (тэр тэнгэр рүү заалаа). Ханхүү Андрей гатлага онгоцны хашлага дээр тохойгоо барьж зогсоод, Пьерийг сонсож, нүдээ салгалгүй цэнхэр үерийн нарны улаан тусгалыг харав. Пьер чимээгүй болов. Энэ нь бүрэн чимээгүй байв. Гарам аль эрт газардсан бөгөөд зөвхөн урсгалын давалгаа л үл мэдэг чимээ гарган гатлага онгоцны ёроолыг цохив. Хунтайж Андрейд долгионыг угаах нь Пьерийн "үнэн, итгээрэй" гэж хэлсэн юм шиг санагдав.
Ханхүү Андрей санаа алдаж, гэрэлтсэн, хүүхэд шиг, эелдэг харцаар Пьерийн улайсан, урам зоригтой, гэхдээ улам бүр аймхай царайг нь сайн найзынхаа өмнө харав.
- Тийм ээ, хэрэв тийм байсан бол! - тэр хэлсэн. "Гэсэн хэдий ч сууцгаая" гэж хунтайж Андрей нэмж хэлээд гатлага онгоцноос буухдаа Пьер өөрт нь зааж өгсөн тэнгэрийг хараад, Аустерлицийн дараа анх удаа тэр өндөр, мөнх тэнгэрийг харав. тэр Аустерлицийн талбар дээр хэвтэж байхыг харсан бөгөөд удаан унтаж байсан, түүний хамгийн сайн зүйл нь гэнэт сэтгэлд нь баяр баясгалантай, залуухан сэрэв. Энэ мэдрэмж хунтайж Андрей амьдралын ердийн нөхцөлд буцаж ирэнгүүт алга болсон боловч хэрхэн хөгжүүлэхээ мэдэхгүй байсан энэ мэдрэмж түүнд амьдарч байсныг тэр мэдэж байв. Пьертэй хийсэн уулзалт нь хунтайж Андрейгийн хувьд гадаад төрхөөрөө адилхан боловч дотоод ертөнцөд түүний шинэ амьдрал эхэлсэн эрин үе байв.
Ханхүү Андрей, Пьер хоёр Лисогорскийн байшингийн гол хаалган дээр ирэхэд аль хэдийн харанхуй болсон байв. Тэднийг ойртож байх үед хунтайж Андрей инээмсэглэн Пьерийн анхаарлыг арын үүдний танхимд болсон үймээн самууныг татав. Нуруундаа үүргэвчтэй бөхийлгөсөн хөгшин эмэгтэй, урт үстэй хар дээлтэй намхан эр сүйх тэрэг орж ирэхийг хараад хаалгаар ухасхийн гүйв. Тэдний араас хоёр эмэгтэй гүйж гарч ирэхэд дөрөв нь тэргэнцэр рүү эргэж хараад айсандаа арын үүдний танхим руу гүйв.
"Эдгээр бол Бурханы машинууд" гэж хунтайж Андрей хэлэв. "Тэд биднийг аав гэж хүлээж авсан." Энэ бол түүний түүнд дуулгавартай байдаггүй цорын ганц зүйл юм: тэр эдгээр тэнүүлчдийг хөөж явуулахыг тушааж, тэр тэднийг хүлээж авав.
- Бурханы хүмүүс гэж юу вэ? гэж Пьер асуув.
Ханхүү Андрей түүнд хариулах цаг байсангүй. Зарц нар түүнтэй уулзахаар гарч ирэхэд тэр хөгшин хунтайж хаана байгаа, түүнийг удахгүй хүлээж байгаа эсэхийг асуув.
Хуучин ханхүү хотод хэвээр байсан бөгөөд тэд түүнийг минут тутамд хүлээж байв.
Ханхүү Андрей Пьерийг эцгийнхээ гэрт үргэлж төгс эмх цэгцтэй хүлээж байсан хагас руу нь хөтөлж, өөрөө цэцэрлэгт явав.
"Эгч рүүгээ явцгаая" гэж хунтайж Андрей Пьер рүү буцаж ирэв; - Би түүнийг хараахан хараагүй, тэр одоо нуугдаж, Бурханы ард түмэнтэйгээ сууж байна. Түүний зөв үйлчилж, тэр ичиж зовох болно, мөн та нар Бурханы ард түмнийг харах болно. C "est curieux, ma parole. [Үнэнийг хэлэхэд сонирхолтой юм.]
– Qu"est ce que c"est que [Ямар] Бурханы хүмүүс вэ? гэж Пьер асуув
-Гэхдээ та харах болно.
Марья гүнж түүн дээр ирэхэд үнэхээр ичиж, толбо нь улаан болж хувирав. Түүний тохилог өрөөнд, дүрсний гэрлийн өмнө чийдэн, буйдан дээр, самовар дээр түүний хажууд урт хамар, урт үстэй, сүм хийдийн дээл өмссөн залуу сууж байв.
Ойролцоох сандал дээр үрчлээтсэн туранхай хөгшин эмэгтэй хүүхэд шиг эелдэг зөөлөн царайтай сууж байв.
"Андре, pourquoi ne pas m"avoir prevenu? [Андрей, чи яагаад надад анхааруулаагүй юм бэ?]" гэж тэр эелдэгхэн зэмлэн, тэнүүлчдийнхээ өмнө тахианыхаа өмнө зогсож буй тахиа шиг хэлэв.
a) Калийн гексацианоферрат (II) - калийн ферроцианид K 4 (фармакопея) -тай урвалд орох.Хүчиллэг орчинд Fe 3+ катионууд калийн ферроцианидтай урвалд орж, төмрийн (III) гексацианоферрат (II) Fe 4 3-ийн нийлмэл нэгдэл болох “Пруссын хөх” хар хөх өнгийн тунадас үүсгэдэг. XХувьсах тооны усны молекул бүхий H 2 O. Хур тунадасны нөхцлөөс хамааран "Пруссын хөх" тунадас нь "Турнбулийн хөх" тунадас шиг (дээрээс харна уу) уусмалаас бусад катионуудыг шингээж, найрлага нь өөрчлөгдөж, KFe томьёотой тохирч болохыг харуулсан. 3+:
Fe 3+ + K + + 4- →FeK↓
Урвал нь өвөрмөц юм. Урвалжийг исэлдүүлэх исэлдүүлэгч бодисоор урвалд саад учруулдаг.
Урвалыг гүйцэтгэж байна. Туршилтын хоолойд төмрийн (III) давсны уусмалаас 2-3 дусал нэмж, HCI-ийн уусмалаас 1-2 дусал, К4-ийн уусмалаас 2 дусал нэмнэ. Уусмал нь цэнхэр болж, хар хөх Пруссын хөх тунадас үүснэ.
б) Тиоцианатын ионуудтай урвалд орох (фармакопея). Fe 3+ давс нь улаан төмрийн (III) тиоцианат үүсгэдэг. Урвал нь хүчиллэг орчинд явагддаг. Үүссэн цогцолборын найрлага нь тогтмол биш бөгөөд Fe 3+ ба SCN ионуудын концентрацаас хамааран 2+-аас 3- хооронд хэлбэлзэж болно. Энэ урвалыг заримдаа 1-р урвал, калийн гексацианоферрат (II)-тай хослуулан төмрийг илрүүлэхэд ашигладаг. Нэгдүгээрт, NH 4 SCN нэмснээр улаан төмрийн тиоцианатын цогцолборыг олж авдаг бөгөөд дараа нь калийн гексацианоферрат (II) нэмснээр калийн төмрийн (III) гексацианоферрат (II) -ийн цэнхэр тунадас болгон хувиргадаг.
Fe 3+ + 3SCN - →Fe(SCN) 3
Урвалын мэдрэмж нь 0.25 мкг байна. Хүчилтөрөгчийн хүчлийн анионууд (фосфор, хүнцэл гэх мэт), Fe 3+ ба NO 2-тай нэгдлүүд үүсгэдэг фторууд нь SCN - улаан нэгдэл NOSCN-ийг үүсгэдэг.
Урвалыг гүйцэтгэж байна. Туршилтын хоолойд төмрийн (III) давсны уусмалаас 3-4 дусал нэмж, аммонийн тиоцианатын NH4NCS эсвэл калийн тиоцианатын KNCS уусмалаас 2-3 дусал нэмнэ. Уусмал нь цэнхэр өнгөтэй болно.
в) Натрийн сульфидтэй урвалд орох (фармакопея).Натрийн сульфид нь төмрийн (III) давсны төвийг сахисан ба бага зэрэг шүлтлэг уусмалаас Fe 2 S 3 хар тунадас үүсгэдэг.
2Fe 3+ + 3S 2- → Fe 2 S 3 ↓
Fe 2 S 3 тунадас нь эрдэс хүчилд уусдаг.
Урвалыг гүйцэтгэж байна. Туршилтын хоолойд төмрийн (III) давсны уусмалаас 3-4 дусал нэмж, аммонийн сульфидын уусмал эсвэл устөрөгчийн сульфидын уусмалаас 2-3 дусал нэмнэ. Төмрийн (III) сульфидын хар тунадас ялгарна.
d) Гидроксидтэй урвалд орох. Fe 3+ гидроксидын ионуудтай харилцан үйлчлэлийн үр дүнд үүссэн төмрийн (III) гидроксидын Fe(OH) 3 тунадас нь шүлтийн уусмалд уусдаггүй тул хүчил-суурь ангиллын дагуу Fe 3+-ийг бүлэгт ангилдаг. гидроксид нь шүлтэнд уусдаггүй катионуудын . Fe(OH) 3 тунадас нь шингэрүүлсэн хүчилд уусдаг; аммонийн хлоридын ханасан уусмалд уусдаггүй (цагаан тунадас Fe (OH) 2-ээс ялгаатай).
Урвалыг гүйцэтгэж байна. Туршилтын хоолойд 3-4 дусал төмрийн (III) давсны уусмал нэмж, 3-4 дусал NaOH нэмнэ. Төмрийн (III) гидроксидын Fe(OH) 3-ийн улаан хүрэн тунадас үүснэ.
e) Сульфосалицилийн хүчилтэй урвалд орох (фармакопея). Fe 3+ катион нь рН ≈ 9-11.5 үед сульфосалицилийн хүчилтэй усан уусмалд урвалд орж шар өнгийн комплекс үүсгэдэг: Fe 3+ + L 2- → 3- ,
Энд L 2- нь бүлгээс хоёр протоныг гарган авах үед сульфосалицилын хүчлээс үүссэн сульфосалицилат анионы тэмдэглэгээ юм.
–COOH ба –SO 3 H.
Хамгийн тогтвортой цогцолбор нь шар өнгөтэй, төмрийн (III) молийн харьцаагаар төмрийн (III) ба сульфосалицилийн хүчлийн анионуудыг агуулдаг: 1: 3-тай тэнцүү сульфосалицилатын анионууд, i.e. Төмрийн атом тутамд гурван сульфосалицилатын лиганд байдаг. Аммиакийн уусмалд энэ цогцолбор давамгайлдаг. Уусмал дахь цогцолборуудын нарийн бүтэц тодорхойгүй байна. Урвалын мэдрэмж нь 5-10 мкг байна.
Урвалыг гүйцэтгэж байна. Туршилтын хоолойд ~5 дусал төмрийн (III) давсны уусмал нэмж, ~10 дусал сульфосалицилийн хүчлийн уусмал, ~0.5 мл концентрацитай аммиакийн уусмал нэмнэ. Уусмал нь шаргал өнгөтэй болдог.
Магнийн (II) катионуудын аналитик урвалууд.
a) Шүлттэй урвалд орох.Шүлтлэг уусмалууд нь магнийн давсны уусмалаас хүчил ба аммонийн давсны уусмалд амархан уусдаг магнийн гидроксидын Mg(OH) 2-ийн цагаан желатин тунадас ялгаруулдаг.
Mg(OH) 2 ↓+ 2HCI→MgCI 2 + 2H 2 O
Mg(OH) 2 ↓+ 2NH 4 CI→ MgCI 2 + 2NH 4 OH
Урвалыг гүйцэтгэж байна. Магнийн ион агуулсан уусмалын 1-2 дусал дээр 2-3 дусал 1М NaOH нэмнэ. Цагаан желатин тунадас үүснэ. Үүссэн тунадасыг 2 туршилтын хоолойд хуваана. Эхний туршилтын хоолойд 3-4 дусал HCl нэмэхэд тунадас уусна. 2-р туршилтын хоолойд 3-4 дусал NH 4 Cl нэмэхэд тунадас мөн уусна.
б) Калийн гипоиодиттой урвал.Иод нь шүлттэй урвалд ороход калийн гипоиодит KIO үүсдэг; Энэ тохиолдолд уусмал дахь тэнцвэр баруун тийш шилжиж, өнгө нь өөрчлөгдөнө.
I 2 + 2OH - ↔I - + IO - + H 2 O
Магнийн давс нэмэхэд Mg 2+ ионууд нь OH ионуудтай Mg(OH) 2 тунадас үүсгэдэг бөгөөд энэ нь тэнцвэрийг зүүн тийш шилжүүлэхэд хүргэдэг. Энэ процессын явцад ялгарсан иодыг Mg(OH) 2 тунадас шингээж, улаан хүрэн өнгөтэй болгодог.
Урвалыг гүйцэтгэж байна. Люголын уусмалыг дусал дусал KOH уусмал нэмж өнгөгүй болгоно. Үүссэн өнгөгүй уусмалд магнийн давсны уусмал нэмнэ. Улаан хүрэн өнгөтэй аморф тунадас нэн даруй гарч ирдэг.
в) Натрийн устөрөгчийн фосфаттай урвалд орох (фармакопея).Натрийн устөрөгчийн фосфат нь рН ~ 9-д NH 3 байх үед магнийн ионтой цагаан талст тунадас үүсгэдэг.
рН>10 үед Mg(OH) 2 ба Mg 3 (PO 4) 2 үүсч болно. Туршилтын хүчиллэг уусмалд рН ~9 хүртэл NH 3 нэмэхийг зөвлөж байна. NH 4 C1 үүссэн тул уусмалын рН тогтмол байна. Тунадас нь хүчтэй хүчил ба цууны хүчилд уусдаг.
MgNH 4 PO 4 ↓+ 3HCI→ H 3 PO 4 + MgCI 2 + NH 4 CI
MgNH 4 PO 4 ↓+ 2CH 3 COOH →Mg(CH 3 COO) 2 + NH 4 H 2 PO 4
Магнийн илрүүлэх хязгаар нь 10 мкг байна. Муу уусдаг фосфат үүсгэдэг ионууд саад болдог; NH 4 +, K (I) болон Na (I) нь саад болохгүй.
Урвалыг гүйцэтгэж байна. Магнийн ион агуулсан уусмалын 1-2 дусал дээр 2-3 дусал 2 М HCl, 1 дусал Na 2 HPO 4 уусмал нэмж, хутгах явцад аммиакийн үнэр гарч иртэл 2 M NH 3 дуслаар нэмнэ ( рН ~ 9). Цагаан талст тунадас үүснэ.
d) 8-гидроксикинолины урвал (гэрэлтэгч урвал). 8-гидроксихинолин нь рН 9 - 12-д магнийн ионтой гидроксихинолинат үүсгэдэг бөгөөд энэ нь ногоон өнгөтэй болдог.
Магнийн илрүүлэх хязгаар нь 0.025 мкг байна. Нойтон толбыг магнийн оксикинолинат ба NH 3 уусмалаар эмчлэхэд гэрэлтүүлгийн эрч хүч нэмэгддэг. A1(III), Zn(II) хөндлөнгийн нөлөө үзүүлдэг.
Хариу үйлдэл үзүүлж байна. Магнийн ион агуулсан уусмалын дусал, урвалжийн этилийн спиртийн дусал дуслыг шүүлтүүрийн цаасан дээр хийнэ. Үүссэн магнийн гидроксихинолинатыг 10% аммиакийн уусмалаар дуслаар эмчилнэ. Хэт ягаан туяаны дор нойтон толбыг харахад ногоон туяа ажиглагддаг.
e) Квинализарин (1,2,5,8-тетраоксиантракинон)(I)-тэй хийсэн урвал.Магнийн ионтой квинализарин (1,2,5,8-тетраоксиантракинон)(I) нь шүлтлэг уусмалд бага зэрэг уусдаг хөх өнгийн нэгдэл үүсгэдэг бөгөөд энэ нь бүтэцтэй (II) юм:
 |
|||
 |
|||
Квинализарины лак нь урвалж бүхий магнийн гидроксидын шингээх нэгдэл гэж үздэг. Хувьсах найрлагатай хелат үүсэх магадлал маш өндөр байна.
Магнийн илрүүлэх хязгаар нь 5 мкг байна. Илрүүлэхэд шүлтлэг шороон металлын ионууд саад болохгүй; хангалттай их хэмжээний шүлт байгаа тохиолдолд хөнгөн цагаан ионууд саад болохгүй.
Аммонийн ион нь магнийн гидроксид үүсэхэд саад учруулдаг тул магнийн ионыг илрүүлэхэд саад болдог. Шүлтлэг орчин дахь урвалжийн уусмал нь нил ягаан өнгөтэй тул хяналтын туршилт хийх шаардлагатай.
Урвалыг гүйцэтгэж байна. Магнийн ион агуулсан уусмалын 1-2 дусал дээр 1 дусал хинализарины уусмал, 2 дусал 30% NaOH уусмал нэмнэ. Цэнхэр тунадас үүснэ. Хяналтын туршилт хийхийн тулд 1-2 дусал усанд нэг дусал квинализарины уусмал, 2 дусал 30% NaOH уусмал нэмнэ. Уусмал нь нил ягаан өнгөтэй болно.
4. Туршилтын хяналт 1
- Гадаргуугийн хурцадмал байдлыг тодорхойлох асуудалд шингэний дуслын контурыг тусгаарлах Дуслын контурыг тусгаарлах
- Кальцийн хэт исэл үйлдвэрлэх арга
- Фео өнгө. Химийн шинж чанар. Усанд уусдаггүй галд тэсвэртэй хар пирофор нунтаг. Төмөр авах арга
- Натрийн тиосульфат Natrii thiosulfas (ln) Тиосульфатын химийн томъёо
- Төмрийг тодорхойлох роданидын арга
- Хүнсний сод: томъёо, хэрэглээ
- Карбонатууд. Хүнсний содын томъёо. Хүнсний сода: томъёо, хэрэглээ Хүнсний содын аюулгүй байдал
- Өвчний тодорхойлолт, шинж тэмдэг, эмчилгээ
- Элэгний өвчин: шалтгаан, төрөл, шинж тэмдэг, урьдчилан сэргийлэлт Элэгний вирус гэж юу вэ
- Helminthic infestation: шалтгаан, шинж тэмдэг, эмчилгээ, урьдчилан сэргийлэх
- Ардын эмчилгээ
- Хүнсний исгэх, түүний ач холбогдол
- Фармакокинетик ба био хүртээмжийн судалгаа - фармакокинетик ба фармакодинамикийн сэтгүүл Өндөр хүчин чадалтай шингэний хроматографи
- Туршилтын ажил хлороформ хлороформ гэртээ
- Эрхэм хий ба тэдгээрийн шинж чанар Эдгээр хийн идэвхгүй байдлыг үүсгэдэг үнэт хийнүүд
- Раман ба NIR спектроскопи NIR спектрометрийн асуудлууд ба тэдгээрийг хэрхэн шийдвэрлэх вэ
- Танталын хажуугийн онцлог
- Тантал гэж юу вэ, хаана хэрэглэдэг вэ?
- Ферментийн үйл ажиллагааны молекулын нөлөө
- Умайн хүзүүний дисплази: анхны шинж тэмдэг, шинж тэмдэг, эмчилгээ