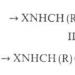Vad är tantal och var används det? Vad är tantal? Funktioner, produkter, egenskaper och applikationer. Tantalpriser
Tantal (Ta) är ett grundämne med atomnummer 73 och atomvikt 180,948. Det är ett element i en sekundär undergrupp av den femte gruppen, den sjätte perioden i det periodiska systemet för Dmitry Ivanovich Mendeleev. Tantal i fritt tillstånd under normala förhållanden är en platina-grå metall med en lätt blyaktig nyans, vilket är en följd av bildandet av en oxidfilm (Ta 2 O 5). Tantal är en tung, eldfast, ganska hård, men inte spröd metall, samtidigt som den är mycket formbar, lättbearbetad, särskilt i sin rena form.
I naturen finns tantal i form av två isotoper: stabil 181 Ta (99,99 %) och radioaktiv 180 Ta (0,012 %) med en halveringstid på 10 12 år. Av det artificiellt erhållna radioaktiva materialet används 182 Ta (halveringstid 115,1 dagar) som isotopindikator.
Grundämnet upptäcktes 1802 av den svenske kemisten A. G. Ekeberg i två mineraler som finns i Finland och Sverige. Den fick sitt namn efter hjälten i antika grekiska myter Tantalus på grund av svårigheten att isolera honom. Länge ansågs mineralerna kolumbit, som innehåller kolumbium (niob), och tantalit, som innehåller tantal, vara en och samma. När allt kommer omkring är dessa två element frekventa följeslagare till varandra och liknar varandra på många sätt. Denna åsikt ansågs korrekt under lång tid bland kemister i alla länder, först 1844 studerade den tyske kemisten Heinrich Rose igen kolumbiter och tantaliter från olika platser och fann i dem en ny metall, liknande egenskaper som tantal. Det var niob. Plast, ren metalltantal, erhölls först av den tyske vetenskapsmannen W. von Bolton 1903.
De huvudsakliga fyndigheterna av tantalmineral finns i Finland, Skandinaviska länder, Nordamerika, Brasilien, Australien, Frankrike, Kina och ett antal andra länder.
På grund av det faktum att tantal har ett antal värdefulla egenskaper - god duktilitet, hög hållfasthet, svetsbarhet, korrosionsbeständighet vid måttliga temperaturer, eldfasthet och ett antal andra viktiga egenskaper - är användningen av det sjuttiotredje elementet mycket omfattande. De viktigaste användningsområdena för tantal är elektronik och maskinteknik. Ungefär en fjärdedel av världens tantalproduktion går till el- och vakuumindustrin. Inom elektronik används den för tillverkning av elektrolytiska kondensatorer, anoder av högeffektslampor och galler. Inom den kemiska industrin används tantal för att tillverka maskindelar som används vid produktion av syror, eftersom detta element har exceptionell kemisk resistens. Tantal löser sig inte ens i en så kemiskt aggressiv miljö som aqua regia! Metaller, som sällsynta jordartsmetaller, smälts i tantaldeglar. Värmare för högtemperaturugnar är gjorda av det. På grund av det faktum att tantal inte interagerar med levande vävnader i människokroppen och inte skadar dem, används det vid kirurgi för att hålla ihop benen under frakturer. Men huvudkonsumenten av en sådan värdefull metall är metallurgi (över 45%). På senare år har tantal i allt större utsträckning använts som legeringselement i specialstål - ultrastark, korrosionsbeständig, värmebeständig. Dessutom förlorar många strukturella material snabbt värmeledningsförmåga: en oxid- eller saltfilm som leder värme dåligt bildas på deras yta. Strukturer gjorda av tantal och dess legeringar möter inte sådana problem. Oxidfilmen som bildas på dem är tunn och leder värme bra, och har också skyddande rostskyddsegenskaper.
Inte bara ren tantal är värdefull, utan också dess föreningar. Således används den höga hårdheten hos tantalkarbid vid tillverkning av hårdmetallverktyg för höghastighetsskärning av metall. Tantal-volframlegeringar ger värmebeständighet till delar tillverkade av dem.
Biologiska egenskaper
På grund av sin höga biologiska kompatibilitet - förmågan att komma överens med levande vävnader utan att orsaka irritation eller avstötning av kroppen - har tantal fått stor användning inom medicin, främst inom rekonstruktiv kirurgi - för att återställa människokroppen. Tunna plattor av tantal används för skador på skallen - de stänger brott i skallen. Medicinen känner till ett fall där ett konstgjort öra tillverkades av en tantalplatta, och huden som transplanterats från låret slog rot så bra och snabbt att snart det konstgjorda organet inte kunde särskiljas från det riktiga. Tantaltrådar används för att återställa skadad muskelvävnad. Kirurger använder tantalplattor för att fästa väggarna i bukhålan efter operationer. Även blodkärl kan anslutas med tantalklämmor. Nätverk gjorda av detta unika material används vid tillverkning av ögonproteser. Trådar gjorda av denna metall används för att ersätta senor och till och med sy ihop nervfibrer.
Inte mindre utbredd är användningen av tantalpentoxid Ta 2 O 5 - dess blandning med en liten mängd järntrioxid föreslås användas för att påskynda blodkoagulering.
Under det senaste decenniet har en ny gren av medicinen utvecklats, baserad på användningen av statiska elektriska fält med kort räckvidd för att stimulera positiva biologiska processer i människokroppen. Dessutom bildas elektriska fält inte på grund av traditionella elektriska energikällor med nätverks- eller batteriströmförsörjning, utan på grund av autonomt fungerande elektretbeläggningar (ett dielektrikum som behåller en okompenserad elektrisk laddning under lång tid), applicerade på implantat för olika ändamål, i stor utsträckning används inom medicin.
För närvarande har positiva resultat från användningen av elektretfilmer av tantalpentoxid erhållits inom följande medicinområden: käkkirurgi (användningen av implantat belagda med Ta 2 O 5 eliminerar förekomsten av inflammatoriska processer och minskar tiden för implantatläkning) ; ortopedisk tandvård (beläggning av proteser gjorda av akrylplast med en film av tantalpentoxid eliminerar alla möjliga patologiska manifestationer orsakade av intolerans mot akrylater); kirurgi (användning av en elektretapplikator vid behandling av defekter i hud och bindväv i långvariga icke-läkande sårprocesser, liggsår, neurotrofiska sår, termiska skador); traumatologi och ortopedi (acceleration av benvävnadsutveckling vid behandling av frakturer och sjukdomar i det mänskliga muskuloskeletala systemet under påverkan av ett statiskt fält skapat av en elektretbeläggningsfilm).
Alla dessa unika vetenskapliga utvecklingar blev möjliga tack vare det vetenskapliga arbetet från specialister från St. Petersburg State Electrotechnical University (LETI).
Utöver de områden som anges ovan där unika tantalpentoxidbeläggningar redan används eller introduceras, finns det utvecklingar som är i ett mycket tidigt skede. Dessa inkluderar utvecklingar för följande medicinområden: kosmetologi (tillverkning av ett material baserat på tantalpentoxidbeläggningar, som kommer att ersätta "gyllene trådar"); hjärtkirurgi (applicering av elektretfilmer på den inre ytan av konstgjorda blodkärl, förhindrar bildandet av blodproppar); endoprotetik (minskar risken för avstötning av proteser som är i konstant interaktion med benvävnad). Dessutom skapas ett kirurgiskt instrument belagt med tantlepentoxidfilm.
Det är känt att tantal är mycket resistent mot aggressiva miljöer, vilket framgår av ett antal fakta. Så vid en temperatur på 200 °C påverkas inte denna metall av sjuttio procent salpetersyra! I svavelsyra vid en temperatur på 150 °C observeras inte heller tantalkorrosion, och vid 200 °C korroderar metallen, men bara med 0,006 mm per år!
Det finns ett känt fall där delar av rostfritt stål vid ett företag som använde väteklorid misslyckades efter bara ett par månader. Men så snart stål ersattes med tantal visade sig även de tunnaste delarna (0,3...0,5 mm tjocka) vara praktiskt taget obestämd - deras livslängd ökade till 20 år!
Tantal, tillsammans med nickel och krom, används ofta som en rostskyddsbeläggning. Den täcker delar av en mängd olika former och storlekar: deglar, rör, plåt, raketmunstycken och mycket mer. Dessutom kan materialet på vilket tantalbeläggning appliceras vara mycket varierande: järn, koppar, grafit, kvarts, glas och andra. Det som är mest intressant är att hårdheten på tantalbeläggningen är tre till fyra gånger högre än hårdheten hos teknisk tantal i glödgat form!
På grund av det faktum att tantal är en mycket värdefull metall, fortsätter sökandet efter dess råvaror idag. Mineraloger har upptäckt att vanliga graniter, förutom andra värdefulla grundämnen, även innehåller tantal. Ett försök att utvinna tantal från granitstenar gjordes i Brasilien, metallen erhölls, men sådan utvinning nådde inte industriell skala - processen visade sig vara extremt dyr och komplex.
Moderna elektrolytiska tantalkondensatorer är stabila, pålitliga och hållbara. Miniatyrkondensatorer gjorda av detta material, som används i olika elektroniska system, utöver ovanstående fördelar, har en unik kvalitet: de kan utföra sina egna reparationer på egen hand! Hur går det till? Antag att isoleringens integritet är skadad på grund av ett spänningsfall eller av annan anledning - omedelbart bildas en isolerande oxidfilm igen på platsen för sammanbrottet, och kondensatorn fortsätter att fungera som om ingenting hade hänt!
Utan tvekan kan termen "smart metall", som dök upp i mitten av 1900-talet, det vill säga en metall som hjälper smarta maskiner att fungera, med rätta tilldelas tantal.
I vissa områden ersätter tantal och konkurrerar ibland med platina! I smyckesarbete ersätter tantal således ofta en dyrare ädelmetall vid tillverkning av armband, klockfodral och andra smycken. På ett annat område konkurrerar tantal framgångsrikt med platina - standardanalytiska balanser gjorda av denna metall är inte sämre i kvalitet än platina.
Dessutom ersätter tantal det dyrare iridium vid tillverkningen av spetsar för automatiska pennor.
På grund av dess unika kemiska egenskaper har tantal funnits som ett material för katoder. Således används tantalkatoder vid elektrolytisk separation av guld och silver. Deras värde ligger i det faktum att sedimentet av ädelmetaller kan tvättas bort med aqua regia, vilket inte skadar tantal.
Man kan definitivt tala om att det finns något symboliskt, för att inte säga mystiskt, i det faktum att den svenska kemisten Ekeberg, som försökte mätta ett nytt ämne med syror, slogs av sin "törst" och gav det nya grundämnet ett namn i ära för den mytomspunna skurken som dödade sin egen son och förrådde gudarna. Och tvåhundra år senare visade det sig att detta element är kapabelt att bokstavligen "sy" en person och till och med "ersätta" hans senor och nerver! Det visar sig att martyren, som försmäktar i underjorden, sonar sin skuld genom att hjälpa människan, försöker be om förlåtelse från gudarna...
Berättelse
Tantalus är en hjälte från antika grekiska myter, en lydisk eller frygisk kung, Zeus son. Han avslöjade de olympiska gudarnas hemligheter, stal ambrosia från deras fest och behandlade olympierna på en maträtt tillagad av kroppen av hans egen son Pelops, som han dödade. För sina grymheter dömdes Tantalus av gudarna till evig plåga av hunger, törst och rädsla i Hades undre värld. Sedan dess har han stått upp till halsen i genomskinligt kristallklart vatten, grenar böjt sig mot hans huvud under tyngden av mogna frukter. Bara han kan inte släcka sin törst eller hunger - vattnet går ner så fort han försöker dricka, och grenarna lyfts av vinden, från händerna på en hungrig mördare. En sten hänger över Tantalus huvud, som kan kollapsa när som helst och tvinga den olyckliga syndaren att för alltid lida av rädsla. Tack vare denna myt uppstod uttrycket "Tantalums plåga", som betecknar outhärdligt lidande, eteriska försök att befria sig från plåga. Under de misslyckade försöken från den svenske kemisten Ekeberg att lösa upp den "jord" han upptäckte 1802 i syror och isolera ett nytt grundämne från den, var det tydligen detta uttryck som kom att tänka på. Mer än en gång trodde forskaren att han var nära sitt mål, men han kunde aldrig isolera den nya metallen i dess rena form. Så här dök namnet "martyrskap" på det nya elementet ut.
Upptäckten av tantal är nära besläktad med upptäckten av ett annat grundämne - niob, som föddes ett år tidigare och ursprungligen hette Columbia, som gavs till det av dess upptäckare Hatchet. Detta element är en tvilling av tantal och är nära det i ett antal egenskaper. Det var denna närhet som vilseledde kemister, som efter mycket debatt kom till den felaktiga slutsatsen att tantal och columbium var samma grundämne. Denna missuppfattning varade i mer än fyrtio år, tills 1844 den berömda tyske kemisten Heinrich Rose, under en upprepad studie av columbites och tantalites från olika fyndigheter, bevisade att columbium är ett oberoende grundämne. Columbia som studerades av Gatchet var niob med en hög tantalhalt, vilket vilseledde den vetenskapliga världen. För att hedra ett så nära förhållande mellan de två elementen gav Rose Colombia det nya namnet Niobium - för att hedra dottern till den frygiska kungen Tantalus Niobia. Även om Rose också gjorde misstaget att påstås ha upptäckt ett annat nytt element, som han döpte till Pelopius (efter Tantalus son Pelops), blev hans arbete grunden för en strikt distinktion mellan niob (Columbium) och tantal. Först, även efter Roses bevis, förväxlades tantal och niob under en lång tid. Så tantal kallades columbium, i Ryssland columbus. Hess talar i sin "Principles of Pure Chemistry" fram till dess sjätte upplaga (1845) endast om tantal, utan att nämna Columbia; Dvigubsky (1824) nämner namnet tantalium. Sådana fel och reservationer är förståeliga - metoden för att separera tantal och niob utvecklades först 1866 av den schweiziska kemisten Marignac, och som sådan existerade inte ren elementär tantal ännu: trots allt kunde forskare erhålla denna metall i dess rena kompakta bildades först på 1900-talet. Den första som kunde få tag i tantalmetall var den tyske kemisten von Bolton, och detta hände först 1903. Tidigare gjordes naturligtvis försök att få fram ren tantalmetall, men alla ansträngningar från kemister var misslyckade. Till exempel fick den franske kemisten Moissan ett metallpulver, som han hävdade var rent tantal. Detta pulver, erhållet genom att reducera tantalpentoxid Ta 2 O 5 med kol i en elektrisk ugn, var dock inte rent tantal, pulvret innehöll 0,5 % kol.
Som ett resultat blev en detaljerad studie av de fysikalisk-kemiska egenskaperna hos det sjuttiotredje elementet möjlig först i början av 1900-talet. Under flera år fick tantal ingen praktisk användning. Först 1922 kunde den användas i AC-likriktare.
Att vara i naturen
Medelhalten av det sjuttiotredje elementet i jordskorpan (clarke) är 2,5∙10 -4 viktprocent. Tantal är ett karakteristiskt element i sura bergarter - granit och sedimentära skal, där dess genomsnittliga innehåll når 3,5∙10 -4%, som för ultrabasiska och basiska bergarter - de övre delarna av manteln och de djupa delarna av jordskorpan, koncentrationen av tantal där är mycket lägre: 1 ,8∙10 -6%. Tantal är spridd i bergarter av magmatiskt ursprung, såväl som i biosfären, eftersom det är isomorft med många kemiska element.
Trots det låga innehållet av tantal i jordskorpan är dess mineraler mycket utbredda - det finns mer än hundra av dem, både tantalmineraler i sig och tantalhaltiga malmer, alla bildade i samband med magmatisk aktivitet (tantalit, columbite, loparit, pyroklor och andra). I alla mineraler är tantals följeslagare niob, vilket förklaras av den extrema kemiska likheten mellan elementen och de nästan identiska storlekarna på deras joner.
Tantalmalmer har själva förhållandet Ta 2 O 5: Nb 2 O 5 ≥1. Huvudmineralerna i tantalmalmer är kolumbit-tantalit (Ta 2 O 5-halt 30-45%), tantalit och manganotantalit (Ta 2 O 5 45-80%), wodginit (Ta, Mn, Sn) 3 O 6 (Ta 2 O5 60-85%), mikrolit Ca2 (Ta, Nb)2O6 (F, OH) (Ta2O5 50-80%) och andra. Tantalit (Fe, Mn)(Ta, Nb) 2 O 6 har flera varianter: ferrotantalit (FeO>MnO), manganotalit (MnO>FeO). Tantalite finns i olika nyanser från svart till rödbrunt. Huvudmineralerna i tantal-niobmalmer, från vilka man utvinner mycket dyrare tantal, tillsammans med niob, är kolumbit (Ta 2 O 5 5-30%), tantalinnehållande pyroklor (Ta 2 O 5 1-4%) , loparit (Ta2O5 0,4-0,8%), gatchettolit (Ca, Tr, U)2 (Nb, Ta)2O6 (F, OH)∙nH2O (Ta2O5 8-28%), ixiolit (Nb, Ta, Sn, W, Sc)3O6 och några andra. Tantalniobater som innehåller U, Th, TR är metamiska, mycket radioaktiva och innehåller varierande mängder vatten; polymorfa modifieringar är vanliga. Tantalniobater bildar små spridningar, stora tilldelningar är sällsynta (kristaller är typiska främst för loparit, pyroklor och columbit-tantalit). Färg svart, mörkbrun, brungul. Vanligtvis genomskinlig eller något genomskinlig.
Det finns flera huvudsakliga industriella och genetiska typer av tantalmalmfyndigheter. Sällsynta metallpegmatiter av natro-litiumtyp representeras av zonerade venkroppar bestående av albit, mikroklin, kvarts och, i mindre utsträckning, spodumen eller petalit. Tantalhaltiga graniter (apograniter) av sällsynt metall representeras av små bestånd och kupoler av mikroklin-kvarts-albitgraniter, ofta berikade med topas- och litiumglimmer som innehåller tunn spridning av kolumbit-tantalit och mikrolit. Vitrande skorpor, deluvial-alluvial och alluvial placers som uppstår i samband med destruktion av pegmatiter innehåller kassiterit och mineraler från columbit-tantalitgruppen. Loparitbärande nefelinsyeniter av lujavrit- och foyalitsammansättning.
Dessutom är avlagringar av komplexa tantal-niobmalmer, representerade av karbonatiter och tillhörande forsterit-apatit-magnetitbergarter, involverade i industriell användning; mikroklin-albit riebeckit alkaliska graniter och granosyeniter och andra. En del tantal utvinns från wolframiter av greisenavlagringar.
De största fyndigheterna av titanmalmer finns i Kanada (Manitoba, Bernick Lake), Australien (Greenbushes, Pilbara), Malaysia och Thailand (tantalbärande tennplacerare), Brasilien (Paraiba, Rio Grande do Norte) och ett antal afrikanska stater (Zaire, Nigeria, södra Rhodesia).
Ansökan
Tantal hittade sin tekniska tillämpning ganska sent - i början av 1900-talet användes det som material för glödtrådar av elektriska lampor, vilket berodde på kvaliteten på denna metall, såsom eldfasthet. Men det förlorade snart sin betydelse på detta område, ersatt av det billigare och mer eldfasta volframet. Tantal blev återigen "tekniskt olämpligt" fram till tjugotalet av 1900-talet, då det började användas i växelströmslikriktare (tantal, belagd med en oxidfilm, passerar ström i endast en riktning), och ett år senare - i radiorör . Varefter metallen fick erkännande och började snart erövra fler och fler nya industriområden.
Nuförtiden, på grund av sina unika egenskaper, används tantal i elektronik (tillverkning av kondensatorer med hög specifik kapacitans). Ungefär en fjärdedel av världens tantalproduktion går till el- och vakuumindustrin. På grund av den höga kemiska trögheten hos både tantal själv och dess oxidfilm är elektrolytiska tantalkondensatorer mycket stabila i drift, pålitliga och hållbara: deras livslängd kan nå mer än tolv år. Inom radioteknik används tantal i radarutrustning. Tantal minikondensatorer används i radiosändare, radarinstallationer och andra elektroniska system.
Den största konsumenten av tantal är metallurgi, som använder över 45 % av den producerade metallen. Tantal används aktivt som legeringselement i specialstål - ultrastark, korrosionsbeständig, värmebeständig. Tillsatsen av detta element till konventionella kromstål ökar deras hållfasthet och minskar sprödheten efter härdning och glödgning. Tillverkning av värmebeständiga legeringar är ett stort behov av raket- och rymdteknik. I de fall där raketmunstycken kyls av flytande metall som kan orsaka korrosion (litium eller natrium) är det helt enkelt omöjligt att klara sig utan en tantal-volframlegering. Dessutom är värmare för högtemperaturvakuumugnar, värmare och blandare tillverkade av värmebeständigt stål. Tantalkarbid (smältpunkt 3 880 °C) används vid tillverkning av hårda legeringar (blandningar av volfram och tantalkarbider - kvaliteter med TT-index, för de svåraste förhållandena vid metallbearbetning och roterande slagborrning av de starkaste materialen (sten, kompositer) ).
Stål legerade med tantal används i stor utsträckning, till exempel inom kemiteknik. Sådana legeringar har trots allt exceptionell kemisk beständighet, de är formbara, värmebeständiga och värmebeständiga; det är tack vare dessa egenskaper som tantal har blivit ett oumbärligt strukturmaterial för den kemiska industrin. Tantalutrustning används vid tillverkning av många syror: saltsyra, svavelsyra, salpetersyra, fosforsyra, ättiksyra, såväl som brom, klor och väteperoxid. Spolar, destillerare, ventiler, blandare, luftare och många andra delar av kemiska apparater är gjorda av det. Ibland - hela enheter. Tantalkatoder används vid elektrolytisk separation av guld och silver. Fördelen med dessa katoder är att guld- och silveravlagringar kan tvättas bort med aqua regia, vilket inte skadar tantal.
Dessutom används tantal vid instrumenttillverkning (röntgenutrustning, kontrollinstrument, diafragma); inom medicin (material för rekonstruktiv kirurgi); inom kärnenergi - som värmeväxlare för kärnenergisystem (tantal är den mest stabila av alla metaller i överhettade smältor och cesium-133-ångor). Tantals höga förmåga att absorbera gaser används för att upprätthålla högt vakuum (elektriska vakuumanordningar).
På senare år har tantal använts som smyckesmaterial på grund av dess förmåga att bilda hållbara oxidfilmer av vilken färg som helst på ytan.
Tantalföreningar används också i stor utsträckning. Tantalpentoxid används inom kärnteknik för att smälta glas som absorberar gammastrålning. Kaliumfluorotantalat används som katalysator vid tillverkning av syntetiskt gummi. Tantalpentoxid spelar också samma roll när man framställer butadien från etylalkohol.
Produktion
Det är känt att malmer som innehåller tantal är sällsynta och fattiga på detta element. De huvudsakliga råvarorna för framställning av tantal och dess legeringar är tantalit- och loparitkoncentrat som endast innehåller 8 % Ta 2 O 5 och mer än 60 % Nb 2 O 5. Dessutom bearbetas även de malmer som bara innehåller hundradelar av en procent (Ta, Nb) 2 O 5!
Tantalproduktionstekniken är ganska komplex och utförs i tre steg: öppning eller nedbrytning; separation av tantal från niob och erhållande av deras rena kemiska föreningar; återhämtning och förädling av tantal.
Öppnandet av tantalkoncentrat, med andra ord, utvinningen av tantal från malmer utförs med hjälp av alkalier (fusion) eller med användning av fluorvätesyra (sönderdelning) eller en blandning av fluorvätesyra och svavelsyra. Därefter går de vidare till det andra produktionssteget - extraktionsextraktion och separation av tantal och niob. Den sista uppgiften är mycket svår på grund av likheten mellan de kemiska egenskaperna hos dessa metaller och den nästan identiska storleken på deras joner. Fram till nyligen separerades metaller endast med den metod som föreslogs redan 1866 av den schweiziska kemisten Marignac, som drog fördel av den olika lösligheten av kaliumfluorotantalat och kaliumfluorniobat i utspädd fluorvätesyra. Modern industri använder flera metoder för att separera tantal och niob: extraktion med organiska lösningsmedel, selektiv reduktion av niobpentaklorid, fraktionerad kristallisering av komplexa fluoridsalter, separation med jonbytarhartser, rektifiering av klorider. För närvarande är den vanligaste separationsmetoden (den är också den mest avancerade) extraktion från lösningar av tantal- och niobfluoridföreningar som innehåller fluorväte- och svavelsyror. Samtidigt renas tantal och niob också från föroreningar från andra element: kisel, titan, järn, mangan och andra relaterade element. När det gäller loparitmalmer bearbetas deras koncentrat med klormetoden för att producera ett kondensat av tantal- och niobklorider, som separeras ytterligare genom rektifikation. Separationen av en blandning av klorider består av följande steg: preliminär rektifikation (separation av tantal- och niobklorider från medföljande föroreningar sker), huvudrektifikation (för att erhålla rent NbCl 5- och TaCl 5-koncentrat) och slutlig rektifikation av tantalfraktionen (till erhålla ren TaCl 5). Efter separationen av besläktade metaller fälls tantalfasen ut och renas för att producera kaliumfluorotantalat med ökad renhet (med användning av KCl).
Tantalmetall erhålls genom att reducera dess högrena föreningar, för vilka flera metoder kan användas. Detta är antingen reduktion av tantal från pentoxid med sot vid en temperatur på 1800-2000 ° C (karbotermisk metod), eller reduktion av kaliumfluorotantalat med natrium vid upphettning (natriumtermisk metod), eller elektrokemisk reduktion från en smälta som innehåller kaliumfluorotantalat och tantaloxid (elektrolytisk metod). På ett eller annat sätt erhålls metallen i pulverform med en renhet på 98-99%. För att få metall i göt sintras den i form av förkomprimerade ämnen från pulver. Sintring sker genom att ström passerar vid en temperatur på 2 500–2 700 °C eller genom uppvärmning i vakuum vid 2 200–2 500 °C. Därefter ökar metallens renhet avsevärt och blir lika med 99,9-99,95%.
För vidare raffinering och produktion av tantalgöt används elektrisk vakuumsmältning i ljusbågsugnar med en förbrukningsbar elektrod, och för djupare raffinering används elektronstrålesmältning, vilket avsevärt minskar innehållet av föroreningar i tantal, ökar dess duktilitet och sänker temperaturen övergång till ett sprött tillstånd. Tantal av sådan renhet bibehåller hög duktilitet vid temperaturer nära absolut noll! Ytan på ett tantalgöt smälts (för att ge de erforderliga egenskaperna till ytan på götet) eller bearbetas på en svarv.
Fysikaliska egenskaper
Först i början av 1900-talet fick forskare tag i ren tantalmetall och kunde i detalj studera egenskaperna hos denna ljusgrå metall med en lätt blåaktig blyton. Vilka egenskaper har detta element? Tantal är definitivt en tungmetall: dess densitet är 16,6 g/cm 3 vid 20 ° C (som jämförelse har järn en densitet på 7,87 g/cm 3, densiteten av bly är 11,34 g/cm 3) och för att transportera en kubikmeter Detta element skulle kräva sex tre-tons lastbilar. Hög hållfasthet och hårdhet kombineras med utmärkta plastegenskaper. Ren tantal lämpar sig väl för mekanisk bearbetning, är lätt att stansa, bearbetas till de tunnaste arken (ca 0,04 mm tjocka) och tråd (elasticitetsmodul för tantal 190 Hn/m2 eller 190·102 kgf/mm2 vid 25 °C). I kyla kan metallen bearbetas utan nämnvärd arbetshärdning och är föremål för deformation med ett kompressionsförhållande på 99 % utan mellanbränning. Övergången av tantal från ett plastiskt till ett sprött tillstånd observeras inte ens när det kyls till -196 °C. Draghållfastheten hos glödgat tantal med hög renhet är 206 MN/m2 (20,6 kgf/mm2) vid 27 °C och 190 MN/m2 (19 kgf/mm2) vid 490 °C; relativ töjning 36 % (vid 27 °C) och 20 % (vid 490 °C). Tantal har ett kroppscentrerat kubiskt gitter (a = 3,296 A); atomradie 1,46 A, jonradier Ta 2+ 0,88 A, Ta 5+ 0,66 A.
Som nämnts tidigare är tantal en mycket hård metall (Brinell-hårdheten för tantalark i glödgat tillstånd är 450-1250 MPa, i deformerat tillstånd 1250-3500 MPa). Dessutom är det möjligt att öka metallens hårdhet genom att tillsätta ett antal föroreningar till den, till exempel kol eller kväve (Brinell-hårdheten hos en tantalskiva efter att ha absorberat gaser under uppvärmning ökar till 6000 MPa). Som ett resultat bidrar interstitiella föroreningar till en ökning av Brinells hårdhet, draghållfasthet och sträckgräns, men de minskar plasticitetsegenskaperna och ökar kallsprödheten, med andra ord, de gör metallen spröd. Andra karakteristiska egenskaper hos det sjuttiotredje elementet är dess höga värmeledningsförmåga, vid 20–100 °C är detta värde 54,47 W/(m∙K) eller 0,13 cal/(cm·sek·°С) och eldfasthet (kanske den mest en viktig fysisk egenskap hos tantal) - den smälter vid nästan 3 000 °C (mer exakt, vid 2 996 °C), näst efter volfram och rhenium. Kokpunkten för tantal är också extremt hög: 5 300 °C.
När det gäller andra fysikaliska egenskaper hos tantal är dess specifika värme vid temperaturer från 0 till 100 °C 0,142 kJ/(kg K) eller 0,034 cal/(g °C); temperaturkoefficienten för linjär expansion av tantal är 8,0·10 -6 (vid temperaturer på 20–1 500 °C). Den elektriska resistiviteten för det sjuttiotredje elementet vid 0 °C är 13,2 10 -8 ohm m, vid 2000 ° C 87 10 -8 ohm m. Vid 4,38 K blir metallen en supraledare. Tantal är paramagnetisk, specifik magnetisk känslighet 0,849·10 -6 (vid 18 °C).
Så tantal har en unik uppsättning fysikaliska egenskaper: hög värmeöverföringskoefficient, hög förmåga att absorbera gaser, värmebeständighet, eldfasthet, hårdhet och plasticitet. Dessutom kännetecknas den av hög hållfasthet - den lämpar sig väl för tryckbehandling med alla befintliga metoder: smide, stämpling, rullning, ritning, vridning. Tantal kännetecknas av god svetsbarhet (svetsning och lödning i argon, helium eller i vakuum). Dessutom har tantal enastående kemisk och korrosionsbeständighet (med bildandet av en anodfilm), lågt ångtryck och låg elektronarbetsfunktion, och dessutom kommer det bra överens med levande vävnad i kroppen.
Kemiska egenskaper
Definitivt, en av de mest värdefulla egenskaperna hos tantal är dess exceptionella kemiska beständighet: i detta avseende är den näst efter ädelmetaller, och även då inte alltid. Den är resistent mot saltsyra, svavelsyra, salpetersyra, fosforsyra och organiska syror i alla koncentrationer (upp till en temperatur på 150 ° C). När det gäller sin kemiska stabilitet liknar tantal glas - det är olösligt i syror och deras blandningar, inte ens regenvatten löser det, mot vilket guld och platina och ett antal andra värdefulla metaller är maktlösa. Det sjuttiotredje grundämnet är lösligt endast i en blandning av fluorvätesyra och salpetersyra. Dessutom sker reaktionen med fluorvätesyra endast med metalldamm och åtföljs av en explosion. Även i heta salt- och svavelsyror är tantal mer resistent än sin tvillingbror niob. Tantal är dock mindre resistent mot alkalier - heta lösningar av kaustiska alkalier korroderar metallen. Salter av tantalsyror (tantalater) uttrycks med den allmänna formeln: xMe 2 O yTa 2 O 5 H 2 O, dessa inkluderar metatantalater MeTaO 3, ortotantalater Me 3 TaO 4, salter som Me 5 TaO 5, där Me är en alkalimetall ; i närvaro av väteperoxid bildas även pertantalater. De viktigaste alkalimetalltantalaten är KTaO 3 och NaTaO 3; dessa salter är ferroelektriska.
Tantals höga korrosionsbeständighet indikeras också av dess interaktion med atmosfäriskt syre, eller snarare dess höga motståndskraft mot denna påverkan. Metallen börjar oxidera först vid 280 °C och täcks med en skyddande film av Ta 2 O 5 (tantalpentoxid är den enda stabila metalloxiden), som skyddar metallen från inverkan av kemiska reagenser och förhindrar flödet av elektrisk ström från metallen till elektrolyten. Men med en ökning av temperaturen till 500 ° C blir oxidfilmen gradvis porös, delamineras och separerar från metallen, vilket berövar ytan av skyddsskiktet mot korrosion. Därför är det tillrådligt att utföra varmtrycksbehandling i vakuum, eftersom metallen i luft oxiderar till ett betydande djup. Närvaron av kväve och syre ökar hårdheten och styrkan hos tantal, samtidigt som den minskar dess duktilitet och gör metallen spröd, och, som tidigare nämnts, bildar tantal en fast lösning och oxiderar Ta 2 O 5 med syre (med en ökning av O 2 -halt i tantal, en kraftig ökning av hållfasthetsegenskaper inträffar och en kraftig minskning av duktilitet och korrosionsbeständighet). Tantal reagerar med kväve för att bilda tre faser - en fast lösning av kväve i tantal, tantalnitrider: Ta 2 N och TaN - i temperaturintervallet från 300 till 1 100 ° C. Det är möjligt att göra sig av med kväve och syre i tantal under höga vakuumförhållanden (vid temperaturer över 2 000 °C).
Tantal reagerar svagt med väte tills det värms upp till 350 °C; reaktionshastigheten ökar markant först från 450 °C (tantalhydrid bildas och tantal blir spröd). Samma uppvärmning i vakuum (över 800 °C) hjälper till att bli av med väte, under vilket de mekaniska egenskaperna hos tantal återställs och vätet avlägsnas helt.
Fluor verkar på tantal redan vid rumstemperatur, och vätefluorid reagerar också med metallen. Torrt klor, brom och jod har en kemisk effekt på tantal vid temperaturer på 150 °C och över. Klor börjar aktivt interagera med metallen vid en temperatur på 250 °C, brom och jod vid en temperatur av 300 °C. Tantal börjar interagera med kol vid mycket höga temperaturer: 1 200–1 400 °C, och bildning av eldfasta tantalkarbider som är mycket resistenta mot syror. Tantal kombineras med bor för att bilda borider - fasta, eldfasta föreningar som är resistenta mot effekterna av aqua regia. Tantal bildar kontinuerliga fasta lösningar med många metaller (molybden, niob, titan, volfram, vanadin och andra). Tantal bildar begränsade fasta lösningar med guld, aluminium, nickel, beryllium och kisel. Tantal bildar inga föreningar med magnesium, litium, kalium, natrium och några andra grundämnen. Ren tantal är resistent mot många flytande metaller (Na, K, Li, Pb, U-Mg och Pu-Mg legeringar).
Tantal intar en speciell plats i gruppen av kända kemiska grundämnen. Denna metall är inte en ädel, men dess prestandaegenskaper gör den efterfrågad inom en mängd olika områden. Dessutom gäller detta inte bara bygg- och tillverkningsindustrin utan även smycken. Idag är användningen av tantal i sig mycket begränsad på grund av dess sällsynthet. Och ändå finns det ett brett utbud av produkter gjorda av detta material på marknaden.
Allmän information om metall
Tantal finns inte i naturen i sin rena form. Det bryts vanligtvis tillsammans med andra mineraler med liknande egenskaper. Denna egenskap hos elementet ledde till dess ganska sena upptäckt. Men nu för tiden finns det effektiva sätt att isolera tantal, varav ett är extraktionsmetoden. Elektrolys används också specifikt för att producera metalliskt material. Med hjälp av en grafitdegel smälts basen som innehåller elementet, varefter pulver blir kvar på behållarens väggar. Ytterligare teknologi för bearbetning av råvaran beror på hur tantal kommer att användas: det kan ges i form av ett göt, tråd, ark, del av en viss form eller lämnas i form av en blandning för sprutning. Teknologier för att bilda legeringar från tantalpulver är också populära. Kombination med legeringsämnen gör det möjligt att förbättra materialets individuella egenskaper.

Fysikaliska egenskaper
Metallen har en hög smältpunkt på cirka 3017 °C, vilket gör att den kan användas under extrema termiska förhållanden i produktionen. Samtidigt har den en sällsynt kombination av egenskaper av duktilitet och hårdhet. När det gäller den första är den mjuk som guld. I detta fall är hårdheten hos tantal 16,65 g/cm 3 . Denna kombination av fysiska egenskaper gör det möjligt att enkelt bearbeta materialet, ge det olika former och storlekar, och även använda det i kritiska mekanismer och strukturer. Små element fungerar bra som växlar och delar av elektriska apparater. Tantal är slitstarkt och hållbart, så förbrukningsbara komponenter är gjorda av det med förväntan på långvarig drift. Dessutom kan denna metall fungera som en effektiv gasabsorbator. Vid höga temperaturer uppvisar tantaldelar också höga ledande egenskaper.
Kemiska egenskaper

I sin rena form motstår metallen effektivt effekterna av alkalier, organiska och oorganiska sura ämnen, såväl som påverkan av andra aktiva medier. Om inte alkalier i smält form har en märkbar effekt på tantal. Oxidationsprocesser sker vid temperaturer som inte är lägre än 280 °C, och den reagerar med halogenkomponenter vid 250 °C. De kemiska egenskaperna hos tantal i kontakt med reagens kan jämföras med glas. Det löser sig inte i sura miljöer med undantag för salpeter- och fluorvätesyror. Detta material är också resistent mot svavelsyra, oavsett dess koncentration. Aktivitetsprocesser har dock i de flesta fall en obetydlig effekt på metallens struktur. Vanligtvis uppträder förändringarna antingen i form av filmbeläggning eller korrosion.
Var används tantal?

Denna metall är inte utbredd, men det finns många användningsområden. Först och främst är detta industri. Elementet används inom metallurgi, livsmedelssektorn, tillverkningsindustri, radioteknik, maskinteknik, etc. Inom byggbranschen är denna metall inte så efterfrågad just på grund av de begränsade produktionsvolymerna, men enskilda konstruktionselement tillverkas fortfarande av detta material - som regel hårdvara avsedd för kritiska uppgifter för att stärka strukturer. För att förstå var tantal används är det viktigt att vara uppmärksam på dess prestandaegenskaper. Det har redan konstaterats att han kan fungera som en god dirigent. Därför används den som en supraledare inom elektroteknik. Å andra sidan öppnar dess värmebeständighet upp möjligheter för dess användning vid värmebehandling av andra metaller. Tack vare sin ökade densitet har tantal blivit en optimal lösning inom försvarsindustrin. Den används för att tillverka projektiler med hög penetrerande kraft.
Tantaltråd
Valsad metall i allmänhet är den mest omfattande formen av presentation av detta material på marknaden. Wire upptar en betydande nisch i segmentet. Det är ovanligt eftersom den, på grund av sin blygsamma storlek, kan användas som en tråd. Detta förklarar värdet av tantal för det medicinska området - produkter av detta slag används för suturer och bandage. Men detta är bara ett exempel som visar en av de utmärkande egenskaperna hos en sådan tråd. Större format används inom maskinteknik, flyg, verktygsmaskiner och kapitalkonstruktion. Dessutom, beroende på syftet, kan mjuk och hård metall användas. Tantal tillåter, på grund av sin flexibilitet vid bearbetning, produktion av långa trådar från 1500 cm med en tjocklek på 0,15 mm eller mer. På färdiga produkter, som användarna noterar, upptäcks sällan grader, sprickor och andra defekter. Den tunna strukturen ställer dock fortfarande krav på lagrings- och transportförhållanden - i synnerhet rekommenderas det inte att utsätta tråden för kontakt med fukt och aggressiva miljöer.

Tantaltejp
Detta format för tillverkning av valsade metallprodukter är också utbrett. Band används inom medicin, inom oljeindustrin, maskinteknik och även inom energiindustrin. Konsumenter värdesätter denna produkt för dess biokompatibilitet, höga hållfasthet med fin struktur, goda bearbetbarhet och motståndskraft mot korrosionsprocesser. Om vi jämför liknande produkter gjorda av tantal med analoger gjorda av stål eller aluminium, kommer slitstyrka och hållbarhet att komma i förgrunden. Tejpen tål höga dragbelastningar och kemisk påverkan. Å andra sidan tillåter hög plasticitet inte sådana produkter att stabilt bibehålla en viss form. Även lätt tryck leder till deformation.
Tantalbaserade legeringar

Legeringar modifierade med legeringskomponenter får övervägande högre kvaliteter av fysisk styrka och värmebeständighet. Det räcker med att säga att en produkt med genomsnittliga egenskaper kommer att klara temperaturer på 1650 °C utan att förlora sina prestandaegenskaper. Detta tillåter faktiskt användningen av tantallegeringar inom kemisk industri, energi, metallurgi och instrumenttillverkning. Dessutom använder vissa företag detta material vid tillverkning av element för raket- och rymdsfären. Beroende på användningsriktningen utvecklar teknologer olika kompositioner för legering av tantal. I vissa fall gör modifiering det möjligt att uppnå högre duktilitet och i andra till exempel att göra materialet lämpligt för svetsoperationer med elektronstrålemetoden. Tantal i sig kan också fungera som en legeringskomponent. Vanligtvis används denna metod för att förbättra prestandaegenskaper för att ge basmetaller anti-korrosion och värmebeständighet.
Tantal i radioteknik
Vid tillverkning av elektriska apparater och delar kommer förmågan att upprätthålla optimal strömledningsförmåga och bibehålla frekvenssignaler samtidigt som storleken på elementbasen minskar i förgrunden. Av denna anledning används tantal ofta vid tillverkning av kondensatorer, tyristorer, transistorer och semistorer. Tidigare användes rullar av aluminiumplåt till samma kondensatorer. Denna lösning förutsatte möjligheten att öka driftsparametrarna endast om storleken på själva delen ökades. Och detta är inte att nämna den omvända minskningen av andra egenskaper förknippade med att öka volymen på kondensatorn. Användningen av tantal, som också är resistent mot negativa processer där radioelektroniska komponenter deltar, gjorde det möjligt att öka den elektriska volymen samtidigt som delens dimensioner bibehölls. En annan sak är att aluminium inte misslyckas på detta område, eftersom det är billigare.
Slutsats

Denna metall har inte alls unika eller icke-standardiserade egenskaper. Den har många attraktiva egenskaper, inklusive korrosionsskydd, hårdhet eller värmebeständighet. Men dessa egenskaper finns individuellt i andra metaller. Dessutom är de i vissa mycket mer uttalade. Men kombinationen av till synes motsatta egenskaper i ett element är verkligen unik. Teknologer strävar efter att uppnå speciella kombinationer i arbetskvaliteten hos material med konstgjorda medel, och i det här fallet bestäms de av ursprungets natur. Till exempel ställer användningen av tantal i medicin och inom metallurgi helt andra mål. I ett fall värderas hög hållfasthet med små produktstorlekar, och i det andra värderas flexibilitet i bearbetningen. Men det finns också en negativ egenskap hos tantal, som gäller för alla områden av dess användning - det är höga kostnader och i vissa fall fysisk otillgänglighet.
Tantal har en hög smältpunkt -- 3290 K (3017 °C); kokar vid 5731 K (5458 °C).
Tantaldensiteten är 16,65 g/cm. Trots sin hårdhet är den lika flexibel som guld. Ren tantal lämpar sig väl för bearbetning, stämplas lätt, rullas till tråd och tunna plåtar som är hundradels millimeter tjocka. Tantal är en utmärkt getter (gasabsorbator), vid 800 °C kan den absorbera 740 volymer gas. Tantal har ett kroppscentrerat kubiskt gitter. Har paramagnetiska egenskaper. Vid 4,38 K blir det en supraledare. Ren tantal är en seg metall som kan bearbetas genom tryck i kyla utan nämnvärd härdning. Den kan deformeras med en reduktionsgrad på 99 % utan mellanliggande glödgning. Övergången av tantal från ett duktilt till ett sprött tillstånd vid kylning till -196 °C detekterades inte. Tantals egenskaper beror till stor del på dess renhet; föroreningar av väte, kväve, syre och kol gör metallen spröd.
Atomens elektroniska struktur.
1s 22s 22p 63s 23p64s 23d104p65s24d105p66s24f145d3
serienummer-73
Tillhör gruppen - A
d-element
Tantal(V)oxid är ett vitt pulver, olösligt i antingen vatten eller syror (förutom H2F2). Mycket eldfast (smälta = 1875°C). Oxidens sura natur är ganska svagt uttryckt och yttrar sig huvudsakligen under reaktionen med alkalismältor: tantalatomoxidation av niob
Ta2O5 + 2NaOH = 2NaTaO3 + H2O
eller karbonater:
Ta2O5 + 3Na2CO3 = 2Na3TaO4 + 3CO2
Salter som innehåller tantal i oxidationstillståndet -4, -5 kan vara av flera typer: metatantalater NaTaO3, ortotantalater Na3TaO4, men det finns polyjoner penta- och hexa-, som kristalliserar tillsammans med vattenmolekyler, 7- och 8-. Femladdat tantal bildar TaO3+-katjonen och salterna TaO(NO3)3 eller Nb2O5(SO4)3 i reaktioner med syror, vilket fortsätter "traditionen" för sidoundergruppen som introduceras av vanadinjonen VO2+.
Vid 1000°C reagerar Ta2O5 med klor och väteklorid:
Ta2O5+ 10HC1==2ТаС15+5Н2О
Följaktligen kan det hävdas att tantal(V)oxid också kännetecknas av amfotericitet med överlägsna sura egenskaper jämfört med egenskaperna hos en bas.
Hydroxiden som motsvarar tantal(V)oxid erhålls genom att neutralisera sura lösningar av tantaltetraklorid. Denna reaktion bekräftar också instabiliteten hos +4-oxidationstillståndet.
Vid låga oxidationstillstånd är de mest stabila föreningarna halogenider (se fig. 3) Det enklaste sättet att få fram dem är genom pyridinkomplex. Pentahalider TaX5 (där X är Cl, Br, I) reduceras lätt av pyridin (betecknad med Py) för att bilda komplex av kompositionen MX4(Py)2.
Tantalsalter. Salter från den sjätte undergruppen är övervägande färglösa kristaller eller vita pulver. Många av dem är mycket hygroskopiska och diffusa i luften. Oxiderna av dessa metaller har amfotära egenskaper, så de flesta av deras salter hydrolyseras lätt och omvandlas till basiska salter som är något eller helt olösliga i vatten. Salter är också kända där dessa metaller ingår i anjonerna (till exempel niobater och tantalater). ) Återfuktning och uttorkning. Alla katalysatorer av denna klass har en stark affinitet för vatten. Huvudrepresentanten för b-klassen är aluminiumoxid. Fosforsyra eller dess sura salter används också på bärare såsom aluminosilikatgel och silikagel med tantal-, zirkonium- eller hafniumoxider. I de första arbetena om separation av tantal och niob genom fraktionerad extraktion föreslogs systemen saltsyra-xylen-metyldioktylamin (1952), samt saltsyra-fluorvätesyra-diisopropylketon (1953). Båda metallerna löses i vattenhaltiga syralösningar som salter, och sedan extraheras tantal med ett organiskt lösningsmedel. I systemet 6/W svavelsyra--9 Ai fluorvätesyra
7. Tantal används för att göra stansar för att dra trådar vid tillverkning av konstgjorda fibrer. Tidigare var sådana formar gjorda av platina och guld. De hårdaste legeringarna är gjorda av tantalkarbid med nickel som cementartad tillsats. De är så hårda att de lämnar repor även på diamant, vilket anses vara hårdhetsstandarden.
Första platsen när det gäller den kritiska temperaturen för övergången till supraledande tillstånd gavs till niobgermanid Nb3Ge. Dess kritiska temperatur är 23,2K (cirka -250 °C). En annan förening, niobstannid, blir en supraledare vid en något lägre temperatur på -255 °C. För att mer fullständigt förstå detta faktum påpekar vi att de flesta supraledare är kända endast för temperaturer av flytande helium (2,172 K). Supraledare gjorda av niobmaterial gör det möjligt att producera magnetspolar som skapar extremt kraftfulla magnetfält. En magnet med en diameter på 16 cm och en höjd av 11 cm, där lindningen är en tejp gjord av sådant material, kan skapa ett fält med kolossal intensitet. Det är bara nödvändigt att överföra magneten till ett supraledande tillstånd, det vill säga att kyla den, och kylning till en lägre temperatur är naturligtvis lättare att göra.
Niobens roll vid svetsning är viktig. Medan vanligt stål svetsades gav denna process inga speciella svårigheter och skapade inga svårigheter. Men när de började svetsa strukturer gjorda av specialstål med komplex kemisk sammansättning, började svetsarna att förlora många värdefulla egenskaper hos metallen som svetsades. Varken förändringar i elektrodernas sammansättning eller förbättringar av svetsmaskinernas konstruktioner eller svetsning i en atmosfär av inerta gaser hade någon effekt. Det är här niob kommer till undsättning. Stål som niob införs i som en liten tillsats kan svetsas in utan rädsla för svetskvaliteten (fig. 4). Svetsens bräcklighet orsakas av de karbider som bildas under svetsning, men förmågan hos niob att kombinera med kol och förhindra bildning av karbider av andra metaller som bryter mot legeringarnas egenskaper räddade situationen. Karbider av niob i sig, liksom tantal, har tillräcklig viskositet. Detta är särskilt värdefullt vid svetsning av pannor och gasturbiner som arbetar under tryck och i aggressiva miljöer.
Niob och tantal kan absorbera betydande mängder gaser som väte, syre och kväve. Vid rumstemperatur kan 1 g niob absorbera 100 cm3 väte. Men även med stark uppvärmning försvagas denna egenskap praktiskt taget inte. Vid 500°C kan niob fortfarande absorbera 75 cm3 väte och tantal 10 gånger mer. Denna egenskap används för att skapa höga vakuum eller i elektroniska enheter där det är nödvändigt att bibehålla exakta egenskaper vid höga temperaturer. Niob och tantal, avsatt på ytan av delar som en svamp, absorberar gaser, vilket säkerställer stabil drift av enheter. Rekonstruktiv kirurgi har nått stora framgångar med hjälp av dessa metaller. Medicinsk praxis inkluderade inte bara plattor av tantal, utan också trådar av tantal och niob. Kirurger har framgångsrikt använt sådana trådar för att sy ihop trasiga senor, blodkärl och nerver. Tantal "garn" tjänar till att kompensera för muskelstyrka. Med dess hjälp stärker kirurger väggarna i bukhålan efter operationen. Tantal har extremt starka bindningar mellan atomer. Detta orsakar dess extremt höga smält- och kokpunkter. Mekaniska egenskaper och kemisk beständighet för tantal närmare platina. Den kemiska industrin använder denna gynnsamma kombination av tantalkvaliteter. Det används för att förbereda delar för syrafast utrustning i kemiska anläggningar, värme- och kylanordningar som kommer i kontakt med aggressiva miljöer.
Två egenskaper hos niob används i den snabbt växande kärnenergiindustrin. Niob har fantastisk "transparens" för termiska neutroner, det vill säga det kan passera dem genom ett lager av metall utan att praktiskt taget reagera med neutroner. Den artificiella radioaktiviteten av niob (framställd vid kontakt med radioaktiva material) är låg. Därför kan den användas för att tillverka behållare för lagring av radioaktivt avfall och installationer för deras bearbetning. En annan lika värdefull (för en kärnreaktor) egenskap hos niob är frånvaron av märkbar interaktion med uran och andra metaller även vid en temperatur på 1000 °C. Smält natrium och kalium, som används som kylmedel i vissa typer av kärnreaktorer, kan cirkulera fritt genom niobrör utan att skada dem.
Metall Tantalöppnade ganska nyligen, nämligen 1802. Den svenska kemisten A.G. hade turen att upptäcka denna metall. Ekeberg. När man studerade två nya mineral som hittades i de skandinaviska länderna visade det sig att de förutom de kända grundämnena även innehöll tidigare ostuderade. Forskaren lyckades aldrig isolera metallen från mineralet i dess rena form, eftersom stora svårigheter uppstod med detta.
I detta avseende namngavs den outforskade metallen efter en hjälte från mytologin i antikens Grekland, och efter vilken den skrevs myten om Tantalus. Efter detta, i mer än 40 år, trodde man att tantal och niob- dessa är samma metall. Men en tysk kemist bevisade skillnaden mellan metallerna, och efter det isolerade en annan tysk tantal i sin rena form, och detta hände först 1903.
Serietillverkning av valsade produkter och tantalprodukter började först under andra världskriget. Idag får detta element namnet "smart metall", eftersom snabbt utvecklande elektronik inte kan klara sig utan det.
Beskrivning och egenskaper hos tantal
Tantalär en metall med hög hårdhet och atomdensitet. I de periodiska kemiska grundämnena finns tantal i position 73. I världspraxis är det vanligt att beteckna denna metall med en kombination av två bokstäver, nämligen Ta. Vid atmosfärstryck och rumstemperatur har tantal en karakteristisk silverfärgad metallisk färg. Oxidfilmen som bildas på ytan av metallen kommer att ge den en blyaktig nyans.
Tantal element inaktiv vid rumstemperatur. Oxidation av ytan på denna metall med luft är endast möjlig vid temperaturer över 280 grader. Tantal reagerar med halogener vid en temperatur som är 30 grader lägre än med luft. I detta fall bildas en skyddande film på ytan, vilket förhindrar ytterligare penetrering av oxiderande element i hela metallens djup.

Tantal kemiskt element med en ganska hög smältpunkt. Så det är 3290 K, och kokpunkten når 5731 K. Trots den höga densiteten (16,7 g/cm3) och hårdheten är den ganska plastig. När det gäller duktilitet kan tantal jämföras med. Ren metall är väldigt lätt och bekväm att arbeta med.
Den är lätt att bearbeta, till exempel kan den rullas ut till en tjocklek av 1-10 mikron. Det bör också noteras att tantal är paramagnetiskt. En intressant egenskap hos denna metall börjar dyka upp vid en temperatur på 800 grader: tantal absorberar 740 av sina gasvolymer.
Det finns redan ett antal fakta i världspraxis som indikerar den utmärkta hållbarheten hos denna metall i mycket aggressiva miljöer. Till exempel är det känt att tantal inte skadas ens av 70% salpetersyra. Svavelsyra upp till 150 grader leder inte heller till korrosiv förstörelse, men redan vid 200 grader kommer metallen att börja lösas upp med en hastighet av 0,006 mm/år.
Vissa produktionsfakta indikerar också att tantal är mycket mer resistent än austenitiska rostfria stål. Därför finns det ett känt fall där tantal delar höll 20 år längre än delar av rostfritt stål.

Ett annat intressant faktum är att tantal används för katalytisk separation av guld. Katoder är gjorda av det, på vilka ädelmetallen i sin tur avsätts och tvättas sedan av med aqua regia. Samtidigt förblir katoden och tantal, på grund av dess utmärkta motstånd mot syror, intakta.
Tillämpningar av tantal
För länge sedan användes denna metall för att tillverka glödtrådar i glödlampor. Idag tantal och tantallegeringar används i följande industrier och produkter:
— Vid smältning av värmebeständiga och korrosionsbeständiga legeringar (till exempel delar av flygplansmotorer).
— Inom den kemiska industrin att skapa korrosionsbeständig utrustning.
— inom metallurgisk produktion för framställning av sällsynta jordartsmetaller.
— under konstruktionen av kärnreaktorer (tantal är den metall som är mest motståndskraftig mot cesiumånga).
— På grund av sin höga biokompatibilitet används tantal för tillverkning av medicinska implantat och proteser.
- för produktion av supraledare - kryotroner (dessa är delar av datorteknik);
- används inom den militära industrin för tillverkning av snäckor. Användningen av denna metall ökar ammunitionens penetrerande kraft;
- effektivare lågspänningskondensatorer är gjorda av tantal;
– På senare tid har tantal blivit fast etablerat i näringslivet. Detta beror på metallens förmåga att bilda starka oxidfilmer på ytan, som kan ha olika färger och nyanser;
- Ett stort antal modifieringar av tantal ackumuleras i kärnreaktorer. För laboratorie- eller militära ändamål kan denna modifiering av metallen användas som en källa för gammastrålning;
— denna metall används som huvudmetall (efter platina) för tillverkning av massstandarder, som har ökad noggrannhet;
- Något intermetalliskt tantalföreningar har mycket hög hårdhet och styrka, samt ökat motståndskraft mot oxidation. Dessa föreningar används inom flyg- och rymdindustrin;
— Tantalkarbider används för tillverkning av skärverktyg med ökat rött motstånd. Verktyget erhålls genom att sintra en blandning av karbidpulver. Dessa verktyg används under mycket svåra förhållanden, till exempel vid slagborrning;
- femvärt tantaloxid nödvändig för att svetsa glas inom kärnteknik.
Tantalfyndigheter och gruvdrift
Tantal är en sällsynt metall. Dess mängd i jordskorpan är bara 0,0002 %. Denna mängd inkluderar två modifieringar av metallen: stabil och radioaktiv. Denna sällsynta metall förekommer i form av sina egna föreningar och är en del av många mineraler. Om tantal ingår i ett mineral kommer det alltid att vara tillsammans med niob.

Avlagringar av tantalföreningar och mineraler finns i många länder. Den största fyndigheten av detta element i Europa ligger i Frankrike. På den afrikanska kontinenten har Egypten mest tantal. Kina och Thailand har också höga reserver av denna metall. Mindre fyndigheter finns i OSS, Nigeria, Kanada, Australien och andra länder. De största fyndigheterna som hittills upptäckts finns dock i Australien.
Cirka 420 ton tantal bryts årligen i världen. De huvudsakliga bearbetningsanläggningarna för denna metall finns i USA och Tyskland. Det är värt att notera att det internationella samfundet deklarerar behovet av att öka produktionen av denna sällsynta metall. Sådana uttalanden är främst relaterade till ökningen av produktionen av elektronik, där detta element används intensivt.

Således ökar antalet utvecklade fält varje år. Till de viktigaste utvecklingsområdena i världen lades till exempel fler platser till i Brasilien, USA och Sydafrika. Det är dock värt att notera att det under de senaste 10 åren har skett en intensiv minskad tantalproduktion. Den lägsta produktionssiffran under 2000-talet inträffade 2010.
Tantal pris
Kostnaden för tantal har fluktuerat kraftigt under de senaste 15 åren. Så, 2002-2003 köpa tantal det var möjligt till lägsta pris. Det här året tantal pris varierade från 340 till 375 dollar per kilogram. I Ryssland idag kan du köpa tantal, pris vilket är 2950 rubel per kilogram.
Tantal är en speciell typ av metall som tillhör ädelgruppen. Det upptäcktes redan 1802, men anses vara ett ungt element. Trots sin sällsynthet används den i stor utsträckning inte bara i smycken utan också i industrin. Det är särskilt vanligt inom elektronik - nästan varje enhet innehåller det.
Massanvändning av denna metall började på 40-talet av förra seklet och fortsätter till denna dag. Det fick sin popularitet på grund av dess ökade hållfasthetsegenskaper. Dessutom har den många unika fysikaliska och kemiska egenskaper.
Fysiska och kemiska egenskaper
Bland de fysiska egenskaperna hos denna metall bör man lyfta fram den höga smältpunkten, som är 3017 grader Celsius, vilket skiljer den från många analoger. På grund av detta används den i områden där ökat motstånd mot extrema förhållanden krävs. Samtidigt inkluderar egenskaperna hos tantal duktilitet och hårdhet, en kombination av dessa är ganska sällsynt i naturen.
Smältpunkten för tantal är 3017 °C.
De ovan nämnda egenskaperna hos tantal gör att du kan bearbeta metallen utan större ansträngning och skapa de nödvändiga formerna och storlekarna. Atomens speciella struktur är mycket viktig för att skapa delar och mekanismer av strukturer med ökat ansvar. Tantal lämpar sig väl för smide och rullning. I detta fall kan kalldeformationsmetoden också användas framgångsrikt. Hög värmeledningsförmåga bör framhållas.
På grund av sin höga densitet kan metallen användas för att producera små växlar och delar av elektriska apparater som är slitstarka och inte försämras efter en längre tids användning.
I vissa fall används den som en gasabsorbator. Den elektroniska konfigurationen bör framhållas: en metall har olika elektriska konduktivitetsegenskaper i sitt normala tillstånd och vid höga temperaturer.
Tantaldelar kan anslutas genom lödning, svetsning eller nitning. Svetsmetoden används oftast, eftersom kvaliteten på svetsen kännetecknas av hög hållfasthet och motståndskraft mot fysisk stress.
Bland de kemiska egenskaperna är det värt att lyfta fram dess höga motståndskraft mot oxidation och alkali. Men när det smält är det delvis mottagligt för alkali. Oxidation är omöjlig vid temperaturer under 250 grader.
De kemiska egenskaperna hos denna metall är mycket lika glas. Det är nästan omöjligt att lösa det i syra, om du inte använder fluorvätesyra och salpetersyra. Även exponering för svavelsyra påverkar inte metallens struktur och form. Endast en liten hinna kan synas på ytan. Det är inte heller föremål för förstörelse under långvarig exponering för havsvatten.
Förekomst i naturen och produktion av tantal
Tantal, som ett kemiskt element, är mycket sällsynt i naturen och utgör endast 0,0002% av jordskorpan. Det finns mycket sällan i sin rena form, oftast i sammansättningen av olika mineraler, i närheten av en annan metall - niob.
Avlagringar av detta element finns i många länder. Stora fyndigheter finns i Frankrike, Egypten, Kina och Thailand. Men de största fyndigheterna av detta element finns i Australien. Tantal bryts i kvantiteter på mer än 400 ton årligen. Samtidigt växer behovet av dess användning ständigt, vilket är förknippat med en ökning av volymen av elektrisk utrustning som produceras med denna metall. Utifrån detta sker en ständig utveckling av nya fyndigheter.
I vårt land är tantalproduktionen koncentrerad till magnesiumfabriken i Solikamsk. Metallen erhålls efter bearbetning av loparitkoncentrat. I andra länder används även andra mineraler som rutil, struverit, tantalit och columbit.
De största tillverkarna av denna metall i världen är USA, Japan och Kina. Antalet globala tillverkare överstiger inte 40 företag. Kostnad - från 1000 dollar per kg.
Tantalbaserade legeringar
På grund av dess speciella fysikaliska egenskaper används denna metall i sin rena form mycket ofta inom industrin. Men för att öka hållfastheten och motståndskraften mot höga temperaturer kan legeringar baserade på det användas och lämpliga legeringskomponenter kan läggas till.
Tantallegeringar kan förbli fasta vid temperaturer på cirka 1700 grader. Detta är nödvändigt vid användning av tantalföreningar inom energisektorn, kemisk industri, produktion av högprecisionsinstrument och metallurgi. Mycket ofta används olika legeringar vid konstruktionen av rymdraketer.
Vilken typ av legeringskomponenter som används beror på de slutliga egenskaper som krävs. För att förbättra kvaliteten på arbetet används element som ger legeringen förbättrade duktilitetsegenskaper.
Det bör noteras att mycket ofta tantal i legeringar används inte som bas, utan som en legeringskomponent. Dess tillägg till olika material möjliggör ökad motståndskraft mot höga temperaturer och korrosion.
Tantal kondensatorkrets
Tantal TAV-10 är en mycket använd legering baserad på denna metall. Den tillverkas med tillsats av volfram, vars mängd är cirka 10%. Detta resulterar i ett material med förbättrad värmebeständighet. Det används för produktion av värmeelement och för medicinska ändamål, eftersom dess komponenter inte irriterar mänsklig hud.
Tillämpningar av tantal
Användningen av tantal är inte begränsad till ett område. Det är värt att lyfta fram de områden där tantalprodukter används mest:
- Metallurgi. Nästan hälften av denna metall används inom den metallurgiska industrin. Detta beror på att det är lätt att använda för att skapa olika legeringar, särskilt korrosionsskyddande stålsorter som är resistenta mot höga temperaturer. Tantaltråd används inom olika områden där ökad styrka och värmebeständighet krävs. Tantalkarbid används också i stor utsträckning vid tillverkning av deglar för eldfasta metaller.
- Elektroteknik. Cirka 25 % används i produktionen av elektroteknik och elektriska apparater. Kondensatorer som använder detta element kännetecknas av ökad driftsstabilitet. Dessutom, i händelse av förstörelse av kondensatorns yta, bildas en film av tantaloxid, som skyddar den. Du bör också lyfta fram element som anoder, katoder, lampor och andra metalldelar, som också produceras på grundval av det.
- Kemisk industri. En femtedel av den producerade volymen används inom den kemiska industrin. Detta beror på att det är resistent mot de flesta syror, salter och alkalier.
- Medicin. Tantal i medicin används i sådana industrier som ben- och plastikkirurgi. Element gjorda av detta material används för att fästa ben för att uppnå ökad styrka utan att irritera organisk vävnad.
- Militär sfär. Inom den militära sfären produceras tantalmål och granater för kumulativa projektiler.
- Instrumentation. Denna metall används för tillverkning av precisionsinstrument, styrutrustning och olika membran, samt vakuuminstrument, eftersom den kännetecknas av sina gasabsorptionsegenskaper.
- Kärnenergi. I detta område fungerar metallen som en värmeväxlare.
Det bör noteras att tillämpningsområdet för tantal endast begränsas av den lilla volymen av dess produktion. Om produktionsvolymen ökar kommer tillämpningsområdet att utökas avsevärt.
- Isolera konturen av en vätskedroppe i problemet med att bestämma ytspänningen Isolera konturen av en droppe
- Metod för framställning av kalciumperoxid
- Feo färg. Kemiska egenskaper. Eldfast svart pyroforiskt pulver, olösligt i vatten. Metoder för att få järn
- Natriumtiosulfat Natrii thiosulfas (ln) Tiosulfat kemisk formel
- Rhodanidmetod för att bestämma järn
- Bakpulver: formel, applikation
- Karbonater. Bakpulverformel. Bakpulver: formel, tillämpning Säkerhet av bakpulver för människor
- Beskrivning av sjukdomen, tecken, behandling
- Leversjukdomar: orsaker, typer, symtom och förebyggande Vad är ett virus i levern
- Helminthic angrepp: orsaker, symtom, behandling, förebyggande
- Folkläkemedel
- Matjäsning och dess betydelse
- Studie av farmakokinetik och biotillgänglighet - journal of pharmacokinetics and pharmacodynamics Högpresterande vätskekromatografi
- Testa arbete kloroform Kloroform hemma
- Ädelgaser och deras egenskaper Ädelgaser vad som orsakar dessa gasers tröghet
- Raman och NIR-spektroskopi Problem med NIR-spektrometri och hur man löser dem
- Sidospecialiteter av tantal
- Vad är tantal och var används det?
- Molekylära effekter av enzymverkan
- Cervikal dysplasi: första tecken, symtom och behandling