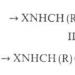Kloroform och dess effekt på människor. Testa arbete kloroform Kloroform hemma
(Kloroformium, triklormetan) är en färglös genomskinlig vätska med en säregen sötaktig lukt och stickande smak.
Kloroform är blandbart i alla proportioner med alkohol, eter, feta och eteriska oljor och är ett bra lösningsmedel för många organiska (paraffin, harts, gummi, lecitin) och vissa oorganiska ämnen (jod, svavel, fosfor).
Kloroform är ganska instabilt. I ljuset oxideras den av syre och bildar klor, saltsyra och särskilt giftig fosgen, så det är viktigt att undvika klorobildning i öppen låga. För att skydda kloroform från nedbrytning bör den förvaras i orange glasflaskor. För samma ändamål tillsätts alkohol och ibland metenamin.
Kloroform tillhör gruppen feta läkemedel som orsakar reversibel förlamning av alla vitala funktioner. Denna effekt finns i alla organismer - bakterier, protozoer, växter, djur.
Den lokala effekten av kloroform uttrycks i irritation av både känsliga nervändar och andra vävnadselement. På huden orsakar flytande kloroform först en känsla av kyla i samband med dess avdunstning, sedan sveda och rodnad, och när den skyddas från avdunstning, inflammation med bildandet av blåsor.
På slemhinnor är irritationseffekten ännu mer uttalad och intag av kloroform kan leda till svåra skador på magen, blodiga kräkningar och diarré.
Kloroformångor är mindre irriterande, men när de andas in leder de till en mängd olika reflexer som stör andningsrörelser, hjärtaktivitet och andra funktioner.
Ämnets höga toxicitet kan orsaka hjärtarytmier, dystrofiska förändringar i hjärtmuskeln, cirros och leveratrofi.
Kloroform var ett av de första läkemedlen som föreslogs som bedövningsmedel (generell anestesi). Sedan mitten av 1800-talet har det använts flitigt i anestesiologisk praxis.
Med en överdriven dos av kloroform under anestesi kan primärt andningsstopp inträffa på grund av förlamning av andningscentrum.
De farligaste komplikationerna under anestesi observerades vid hjärtaktivitet - till och med plötsligt hjärtstopp.
På grund av introduktionen av nya läkemedel och metoder för allmän anestesi i medicinen uteslöts 1985 läkemedlet kloroform för anestesi (Chloroformium pro narcosi) från läkemedelssortimentet. Samtidigt har läkemedlet "Kloroform", avsett för extern användning, behållits i nomenklaturen. På grund av dess irriterande effekt på huden används detta läkemedel (vanligtvis blandat med metylsalicylat, terpentin och andra medel) för att gnugga för neuralgi och myosit. I sällsynta fall föreskrivs kloroform i form av droppar för kräkningar, hicka (blandat med valerianatinktur), såväl som i form av en speciell "Anti-rökblandning" för skador på luftvägarna genom irriterande arsines (en giftig färglös gas - en kemisk förening av arsenik och väte).
Upptäckten av många kemiska ämnen var inte avsiktlig, utan oavsiktlig, under syntesen eller studien av ett ämnes egenskaper. Men många av de oavsiktligt upptäckta ämnena blev mycket viktiga, de användes inte bara inom kemi, utan också inom medicin, industri och andra områden. Kloroform, som kommer att diskuteras vidare, är ett av dessa ämnen.
namn
Namnet på detta ämne har flera varianter. När allt kommer omkring, som alla organiska föreningar, lyder den lagarna i den allmänna nomenklaturen av molekyler, triviala namn och ett namn baserat på molekylens sammansättning.
Därför finns det flera möjliga namn för kloroform:
- koltriklorid;
- kloroform;
- triklormetan.
Kloroform: vad är det? Du kan förstå det från namnen på föreningarna, eller så kan du överväga molekylens geometriska struktur.
Molekylstruktur
Kloroformmolekylen består av tre kloratomer och en väteatom, varje atom bunden till ett centralt kol. I huvudsak är triklormetanmolekylen produkten av väteatomer på kloratomer i en metanmolekyl när den utsätts för vissa förhållanden.
Dessutom är alla C-CL-bindningar helt likvärdiga och mycket polära. CH-bindningen, mot bakgrund av andra bindningar som har uppstått i molekylen, blir ännu mer polariserad och blir extremt sårbar. Därför, med vidare bearbetning av molekylen, bryts CH-bindningen lätt och väte ersätts med andra atomer (till exempel även klor med bildning av koltetraklorid).
Låt oss titta på hur kloroform ser ut. Formeln ser ut så här: CHCL 3. Strukturformeln kommer att se ut så här:

Båda strukturerna återspeglar den kemiska essens som kloroform bär. Formeln visar att molekylen är ganska stabil och strikta villkor måste tillämpas för att komma in i reaktioner.
Fysikaliska egenskaper
De fysikaliska egenskaperna hos triklormetan kan karakteriseras enligt följande:
- Under normala förhållanden (rumstemperatur, normalt atmosfärstryck 100 kPa, luftfuktighet inte högre än 80%) är detta ämne en starkt luktande, färglös vätska. Lukten av kloroform är ganska skarp, tung, omslutande, påminner om lukten av eter. Ämnet smakar sött, men du bör inte prova det, eftersom det är extremt giftigt.
- Det löser sig inte i vatten, det kan bara lösas upp i olika typer.Med vatten kan det bilda lågkoncentrationslösningar (0,23%).
- Kokpunkten för denna förening är lägre än för vatten, cirka 62 0 C.
- Smältpunkten är kraftigt negativ, -63,5 0 C.
- Densiteten för kloroform är större än och är 1,483 g/cm3.
- Ämnets starka, uttalade giftiga natur i dess effekt på kroppen tillhör gruppen narkotiska föreningar.
När koltriklorid löses i vatten kan den bilda azeotropa blandningar. I detta fall kommer kloroformen i lösningen att vara 97,5% och vatten endast 2,5%. Kokpunkten för en sådan lösning är lägre jämfört med den för ren triklormetan och är 52 0 C.

Kemiska egenskaper
Liksom alla klorerade derivat av metan, uppvisar kloroform inte kemisk aktivitet. Därför är det få reaktioner som är utmärkande för det. Till exempel behandling med klormolekyler i processen för teknisk produktion av alla metanderivat genom klorering. För att göra detta tas flytande kloroform, reaktionerna fortskrider enligt en radikal mekanism, vilket kräver närvaro av ultraviolett strålning som en förutsättning och ljuskvanta.
CHCL3 + CL2 = CCL4 + HCL
Enligt reaktionsekvationen är det tydligt att produkten är helt klorsubstituerad metan - koltetraklorid. Sådana reaktioner är ett av sätten att producera koltetraklorid i industrin.
Kemiska egenskaper inkluderar också en azeotrop blandning med vatten, som kloroform kan producera. Vad det är? Det vill säga en där komponenterna i lösningen inte genomgår några förändringar vid kokning. Det är omöjligt att separera en sådan blandning i fraktioner med hjälp av kokningsmetoden.
En annan typ av reaktion som kloroform kan genomgå är ersättning av halogenatomer med andra atomer eller funktionella grupper. Till exempel, när den reagerar med en vattenlösning bildar den natriumacetat:
kloroform + NaOH (vattenlösning) = + natriumklorid + vatten
Dessutom är en praktiskt taget signifikant reaktion interaktionen av kloroform med ammoniak och kaliumhydroxid (koncentrerad lösning), eftersom som ett resultat av sådan interaktion,
Kloroform + ammoniak + kaliumhydroxid = KCN + + vatten
Kloroformförvaring
I ljuset sönderdelas triklormetan och bildar farliga, giftiga produkter:
Kloroform = fosgen + saltsyra + molekylärt klor + kolsyraanhydrid
Därför måste förvaringsvillkoren för kloroform vara speciella - mörka glasflaskor med täta inslipade proppar. Själva flaskan bör förvaras borta från solljus.

Mottagande
Kloroform framställs på flera sätt.
1. En flerstegsprocess av metanklorering, som sker genom en radikal mekanism under påverkan av ultraviolett ljus och hög temperatur. Resultatet är inte bara kloroform, utan även tre andra produkter: klormetan, diklormetan och koltetraklorid. Reaktionen ser ut så här:
CH 4 + CL 2 = CH 3 CL + HCL - klormetan och väteklorid bildas
CH 3 CL + CL 2 = CH 2 CL 2 + HCL - diklormetan och väteklorid bildas
CH 2 CL 2 + CL 2 = CHCL 3 + HCL - triklormetan (kloroform) och väteklorid bildas
CHCL 3 + CL 2 = CCL 4 + HCL - koltetraklorid och väteklorid bildas
På så sätt syntetiseras triklormetan i industrin.
2. Interaktion mellan blekkalk och etylalkohol. Detta är en laboratoriemetod.
3. Framställning av kloroform genom elektrolys (verkan av elektrisk ström) på alkalimetallklorider i en atmosfär av aceton eller etylalkohol. Även en laboratoriemetod för framställning av triklormetan.

Rengöring
När kloroform väl har erhållits måste den renas. När allt kommer omkring, om det används för medicinska ändamål, är innehållet av föroreningar i det helt enkelt oacceptabelt. Om syftet med användningen är tekniskt bör innehållet av främmande ämnen begränsas.
Det kan finnas olika föroreningar som kloroform innehåller. Vad det är? Vad är dem?
- Etanol.
- Väteklorid.
- Fosgen.
- Klor.
Det finns två huvudsakliga sätt att rena kloroform från dessa föroreningar:
- riklig sköljning med vatten följt av torkning (låter dig bli av med etanol helt);
- triklormetan tvättas med en stark syra, sedan med en stark alkali och sedan med vatten. Efterföljande bearbetning består av torkning med ett vattenavlägsnande medel - kalciumklorid. Ämnet destilleras sedan i en fraktionerad kolonn.

Upptäcktshistoria
Sedan när har kloroform varit känt? Vad är det och vad användes det till tidigare? Låt oss försöka lista ut det.
Det första omnämnandet av detta ämne går tillbaka till 1831. Det var då som triklormetan erhölls av kemisten Guthrie från Harbor. Men hans mål var inte alls detta ämne, det var en framgångsrik biprodukt. Kemisten letade efter lösningsmedel för gummi, experimenterade och fick av misstag kloroform.
Samma år och ett år senare erhöll ytterligare två forskare oberoende av varandra detta ämne som ett resultat av experiment. Dessa är Eustace Liebig (som gjorde ett enormt bidrag till utvecklingen av kemi) och Eugen Suberein. Deras uppgift var att hitta ett bedövningsmedel, och de hittade det. Det är sant att de lärde sig om denna effekt av kloroform och började använda den lite senare, först på 1840-talet.
Strukturformeln och interaktionen mellan atomer inuti molekylen studerades och konstruerades av kemisten Dumas 1834. Han föreslog och tilldelade namnet till kloroform, som han gav för att hedra myror. På latin uttalas myra formiata, och innehållet i dessa insekter kan bildas från kloroform. Utifrån detta bestämdes dess namn.
Biologisk effekt på människor
Kloroform motiverar fullt ut dess användning som bedövningsmedel. Effekten på människor är mycket specifik och täcker flera stora organsystem.
Graden av påverkan beror på faktorer som:
- koncentration av inhalerat ämne;
- användningstid;
- sätt att komma in.
Om vi talar om ren, medicinsk kloroform, är dess användning strikt doserad, exakt och lokal. Av de möjliga kontraindikationerna är därför endast några implementerade. Om vi pratar om förångad kloroform i luften och inandning av en person, är effekten här mycket mer allvarlig och destruktiv.
Så när du andas in triklormetan i 10 minuter kan svullnad av luftvägarna, lungspasmer, hosta och halsont uppstå. Om exponeringen inte stoppas kommer förgiftning att inträffa omedelbart. Nervsystemet (både hjärnan och ryggmärgen) kommer att påverkas, vilket leder till döden.
Kloroform har också en skadlig effekt på levern, matsmältningsorganen och njurarna. Dess effekt är särskilt destruktiv om lösningen tas oralt. Följande reaktioner från kroppen på att ta kloroform observeras:
- yrsel;
- kräkningar och illamående;
- ihållande huvudvärk;
- depression av nervsystemet och, som ett resultat, trötthet;
- höjd temperatur;
- allergiska utslag, rodnad i huden.

Studier och experiment på olika djur visade följande resultat:
- Långvarigt intag av kloroform oralt i form av vätska orsakar abort, flera patologier och mutagenes hos framtida generationer.
- När de levde i en atmosfär av kloroform var djuren deprimerade, slöa och deras förväntade livslängd minskade avsevärt.
- Baserat på experiment på möss drogs slutsatsen att triklormetan är cancerframkallande.
Sådana resultat erhölls av kemister och medicinska forskare när de studerade effekterna av kloroform på levande organismer.
Tillämpning inom medicin
Det första omnämnandet av användningen av detta ämne för medicinska ändamål går tillbaka till 1847. Det var då som vetenskapsmannen, läkaren och kemisten Holmes Coote först föreslog användningen av kloroform som anestesi. Detta hade en positiv effekt på personen under operationen - fullständig förlust av medvetande, frånvaro av några förnimmelser.
Men senare, när patienten återfick medvetandet, visade det sig att hans illamående och kräkningar inte upphörde. Senare fastställdes mer exakta standarder för användningen av detta ämne för att undvika sådana konsekvenser.
Den engelske obstetrikern James Simpson spelade en mycket viktig roll i införandet av kloroform i medicinen. Det var han som bevisade den positiva betydelsen och effekten av föreningen under förlossningen.
Men med tiden har nyare, säkrare och modernare anestesimetoder än kloroform dykt upp. Dess användning inom medicin har praktiskt taget försvunnit. Idag används det i formen:
- salvakomponent för extern användning;
- som ett extra bedövningsmedel i kombination med andra substanser och endast i mycket små koncentrationer;
- som droppar för att lindra illamående och kräkningar.
Industriella applikationer
Kloroform används även inom industrin. Dess användning hänför sig till olika kemiska synteser, där det spelar rollen som lösningsmedel, avfettningsmedel, huvud- eller ytterligare komponent för produktion av viktiga ämnen som används inom alla områden av mänsklig aktivitet.
Kloroform är en organisk kemisk förening vars formel visas nedan. Under normala förhållanden är det en färglös vätska med söt smak och eterisk lukt. Det är nästan olösligt i vatten och brinner inte.

Detta är ett klorerat derivat av metan, som erhålls genom att värma blekmedel med etylalkohol. Denna reaktion består av 3 delar:

Du måste sätta ihop enheten enligt bilden nedan. Termometern måste föras in i Wurtz-kolvens provrör, den måste nå botten av kolven. Häll blekmedel (63,5 g) i en 0,5 liters Wurtz-kolv och fyll den med vatten (250 ml). Du kommer att få en halvflytande blandning, till vilken du ska lägga etylalkohol (14,5 ml). Efter det, stäng kolven med en propp med en termometer och värm den på gallret efter att ha anslutit den till kylskåpet. En exoterm reaktion måste börja, även om reaktionen till en början sker utan extern energitillförsel, temperaturen är konstant, och kloroformen i form av en vätska destilleras med vatten in i cylindern. Lagret av kloroform kommer att vara under lagret av vatten i cylindern. Med hjälp av en separertratt kan du separera kloroformen från vattnet. Du bör få cirka 20 ml av ämnet.

Hur man får kloroform från etylalkohol
Ta 430 g blekmedel (med en CaO2Cl2-halt på cirka 23,4%), blanda med en och en halv liter vatten, tillsätt 100 g kaustikkalk och 100 ml. 88,5% alkohol. Den resulterande blandningen destilleras. Mjölk av kalk och kalciumklorid tillsätts till destillatet, sedan separeras den separerade kloroformen. Blanda kloroform med svavelsyra och utför restifiering.
Hur man gör kloroform av aceton
Du bör ta 275 g blekmedel och späda det med 800 ml. vatten, tillsätt långsamt en blandning av 70 ml. vatten och 22 g aceton.
Framställning av kloroform av natrium- och kaliumhypoklorit
I denna metod elektrolyserar du en vattenlösning av kaliumklorid och alkohol (du kan använda aceton eller aldehyd istället för alkohol). Denna metod ger ganska bra resultat när det gäller mängden ämne som frigörs.
Elektrokemisk metod
Platinaplattor används för katoden och anoden (katoden ska vara i porös lera).
Katodvätskans sammansättning: saltsyra (1.19) – 30 ml.
Anodvätskans sammansättning: 80 g kristallint Ba(OH)2∙8H2O, som löses i 300 ml. vatten vid 50 C; 1 g. BaСl2∙2H2O.
30 ml tillsätts till anodvätskan. alkohol En ström på 2 A och en spänning på 8 V krävs, med en förbrukad ström på 6,3 Ah. Temperaturen höjs från 50 till 70 grader, gradvis tillsätts alkohol. Den erforderliga strömtätheten är 4 A per 100 cm2 och 10 A per 100 cm2 vid anoden respektive katoden. Katodvätskan bör också bytas. Den resulterande kloroformen isoleras tillsammans med överskott av alkohol.
Kloroform på recept. På 1800-talet ansågs ämnet, tillsammans med kokain och heroin, vara ett läkemedel. Kloroformlösning Kimball White Pine såldes på apotek som en host- och bronkitblandning. Läkare ordinerade föreningen för astmatiker.
Kloroform rekommenderades också som bedövningsmedel. På 2000-talet är ämnet förbjudet för internt bruk. Vad förändrades? Tydligen egenskaper hos kloroform och dess effekt på människor har klargjorts och dessa klargöranden är uppenbarligen inte till förmån för den berömda blandningen.
Egenskaper hos kloroform
Triklormetan - vetenskapligt namn kloroform. Formelämnen – CHCL 3. Det är flytande. Den har ingen färg, men den smakar sött. Sötman åtföljs av en brännande känsla, och lukten av kompositionen är stickande. Kloroform apotek 1800-talet erbjuds i kombination med organiska lösningsmedel. Ämnet blandas inte med vatten.
I början av 1900-talet registrerade läkare hundratals fall av hjärt- och andningsstillestånd. Alla avlidna tog mediciner som innehöll kloroform. Var Läkare antog omedelbart ett samband mellan substansen och patienters död. Men läkemedlets skadliga effekter bevisades först på 1960-talet. Triklormetan förbjöds 1967.
Kloroformånga orsakar sömn, förlust av motorisk aktivitet och känslighet. Livsprocesser saktar ner. Det finns en förlust av styrka. Därför har triklormetan länge varit ett smärtstillande medel under operationer och en populär bedövning.
Efter att ha genomgått operation utvecklade patienter ibland levercirros och hjärtrytmrubbningar. De var en följd av drogens toxicitet. För försvagade organismer var det ofta katastrofalt. Så anestesi togs bort från listan över mediciner.
Kloroformeffekt på människor har en effekt i tre steg. Efter inandning börjar ett stadium av ofullständigt medvetande. Sedan är det spänning. Anestesi är bara det tredje steget. Det förlamar kopplingar i ryggmärgen och hjärnan.
Det vill säga fullständig anestesi uppstår. Styrkan av läkemedlet beror på dess lagring. Ämnet måste isoleras från syre. Triklormetan interagerar med det och sönderfaller långsamt.
En 1%-ig tillsats av etylalkohol kan bromsa nedbrytningsprocessen av kloroform. Utan "skydd" sönderfaller triklormetan till väteklorid, myrsyra och fosgen. Kloroform - sövande betyder att.

Men om en reaktion inträffar med kaliumhydroxid, kommer blandningen att få dig att sova för alltid. Resultatet av interaktionen är den välkända kaliumcyaniden. En mer ofarlig förening är triklormetan med koncentrerade alkalier. Kolmonoxid bildas.
Vissa reaktioner kräver förhöjda temperaturer. För kloroform anses detta vara 50-60 grader. Vid 62 Celsius kokar ämnet, vilket ger vatten nästan 40 grader. Tätheten av triklormetan, tvärtom, är större än den för vatten - 1 483 gram per kubikcentimeter. Den trögflytande vätskan ser ut som eter.
Beredning av kloroform
Köp kloroform problematisk. Men ämnet kan erhållas i laboratoriet. Det finns 3 sätt. Den första är flerstegs. Grunden är metan. Det måste kloreras. Reaktionen är endast möjlig under ultraviolett ljus och vid höga temperaturer.
Men det är möjligt att få inte bara kloroform. Handling reaktionen är också inriktad på bildning av koltetraklorid, diklormetan och klormetan. Den första används som lösningsmedel vid tillverkning av freoner, det vill säga köldmedier. Diklormetan löser upp färger och används för att ta bort dem. Klorid behövs för att syntetisera silikoner.
Den första metoden för att producera kloroform har 4 steg. Först frigörs klorväte parat med klormetan. Det andra steget är bildningen av samma väteklorid och diklormetan. Kloroform extraheras i det tredje steget. Den andra produkten av reaktionen är väteklorid. Det frigörs också i det sista skedet, när tetraklormetan syntetiseras.
Kloroform - anestesi, som tidigare erhållits genom att kombinera etylalkohol och blekkalk. Reaktionen är enstegs och mest lämpad för laboratorieimplementering. Under förenklade förhållanden kan även elektrolysmetoden användas. En atmosfär av etylalkohol krävs.

Ibland ersätts det med aceton. Reaktionens huvudkaraktärer är alkalimetallklorider. Det är genom dem som elektrisk ström passerar och sönderdelas till komponenter, bland vilka det finns kloroform.
Söva människan, även i gamla dagar, var tillåten endast med ren kloroform. Men efter alla tre metoderna för att få det förblir ämnet kontaminerat. Bland föroreningarna: - fosgen, väteklorid, etylalkohol och klor. Etanol avlägsnas genom att upprepade gånger tvätta triklormetanen med vatten. Sedan kommer behandlingen med kalciumklorid. Den drar ut det återstående vattnet.
Om föroreningarna inte bara inkluderar etylalkohol, är det nödvändigt att tvätta kloroformen först med en stark syra, sedan med samma alkali och först sedan med vatten. Kalciumklorid dyker upp igen i finalen. När dess uppdrag är avslutat skickas triklormetan för destillation. Det utförs i en fraktionerad kolonn.
Användning av kloroform
Även om kloroform inte längre är relevant inom medicinen, fortsätter det att användas inom industrin. Ämnet är nödvändigt för dussintals kemiska synteser. I dem spelar triklormetan rollen som lösningsmedel. Kloroform kan också avfetta. I reaktioner fungerar den som en huvud- eller hjälpkomponent.
Kloroform pris också intresserad av de som vill köpa en lösning för hushållsändamål. Ämnet kan ersätta terpentin. Det förvaras hemma och i garage som lösningsmedel. Med hjälp av triklormetan blir du av med fläckar från torkande olja, fetter, lim och hartser.
Kloroform fortsätter att användas i bårhus. Här saktar ämnet ner kroppars nedbrytningsprocesser. Levande varelser får triklormetan endast på vissa veterinärkliniker. Syftet är detsamma som tidigare gällt för människor - anestesi. I sällsynta fall ges det till grisar och hundar.

Ryktena om kloroforms roll i brottmål slutar inte. Kommer du ihåg scener från filmer, fragment från deckare, där brottslingar sövde offer genom att hålla en näsduk indränkt i triklormetan mot näsan?
Medan personen är medvetslös rånar angriparna, letar efter hemliga dokument och dödar. På 1900-talet förekom sådana fall inte bara i filmer och litteratur.
Men efter förbudet mot kloroform blev det problematiskt att få det. Nu är brott som begås med ett giftigt ämne sällsynta. Men utredarna säger att detta också händer.
Som regel används kloroform av dem som har officiell tillgång till det, samma bårhusarbetare eller studenter vid medicinska institut som genomgår praktik där.
Under normala förhållanden är detta ämne en färglös flyktig vätska med en uttalad eterisk lukt och söt smak. Kloroform i läkemedel är en emulsion som är avsedd för lokal användning och finns i en mörk glasflaska.
Användningen av kloroform är nu inte lika utbredd som tidigare, när läkemedlet användes flitigt i medicinsk praxis för allmän anestesi. På grund av dess skadliga effekter på människokroppen övergavs kloroform till förmån för andra, säkrare droger.
Det är värt att notera att ett sätt att använda kloroform på ett säkert sätt har ännu hittats. För att göra detta förses läkemedlet med en stor mängd syre, och samtidigt bibehålls den exakta dosen. Men ändå används det extremt sällan för smärtlindring under kirurgiska ingrepp.
farmakologisk effekt
- Verkan av kloroform som bedövningsmedel är förknippad med en minskning av fasövergångstemperaturen för membranlipider, vilket i sin tur ökar fluiditeten hos nervcellsmembranen.
- Den sövande effekten av kloroform på människor är baserad på ämnets förmåga att kraftigt trycka ner det centrala nervsystemet, som ett resultat av vilket förmågan att agera frivilligt går förlorad, medvetandet är deprimerat och det finns ingen reaktion på yttre stimuli
- Kloroformanestesi kännetecknas av illusioner, vanföreställningar, ångest, omotiverade, okoordinerade rörelser. Hos vissa personer är reaktionen kliniskt-toniska anfall
- Ämnet är mycket giftigt, det trycker ned hjärt-, nerv- och andningssystemet och förstör levern. Enligt statistiken är var tionde invånare på planeten allergisk mot detta läkemedel
- Om läkemedlet appliceras lokalt är dess verkningsmekanism baserad på irritation av receptornervändar och andra delar av vävnadssystemet
- Väl på huden börjar kloroform avdunsta, vilket gör att en person känner sig kall. Efter detta kommer patienten att känna en brännande känsla och notera rodnad i huden. Om det finns skydd mot avdunstning kommer allvarlig inflammation att uppstå på huden med bildning av blåsor
- Vid kontakt med slemhinnor blir effekten av kloroform mer uttalad och irritationen blir mycket starkare.
- Om kloroform kommer in i människokroppen oralt, kommer resultatet att bli blodiga kräkningar, diarré och allvarliga skador på mag-tarmkanalen.
- Ämnets ångor har inte en så uttalad irriterande effekt, men på ett eller annat sätt är de giftiga och kan störa funktionen hos vissa organ och system i människokroppen (myokarddystrofi, allvarlig hjärtdysfunktion, cirros och leveratrofi )
- Kloroformbedövning har fyra stadier - analgesi, spänning, kirurgiskt stadium, uppvaknande.
- I det första skedet, när patienten är i ett tillstånd av slöhet eller dåsighet, men samtidigt är medveten, utförs diagnostiska tester eller enkla kirurgiska operationer. I analgesistadiet går ytlig känslighet för smärta förlorad, men samtidigt förblir känsligheten för termiska effekter, personen känner beröring
- I det andra steget kan medicinska manipulationer inte utföras, eftersom patienten inte längre är vid medvetande, men motor- och talaktiviteten är fortfarande bevarad (personen kan försöka resa sig från bordet, slita av sig masken, skrika). I detta skede fortsätter narkosläkaren att mätta kroppen med kloroform för att uppnå ett djupare tillstånd.
- Det tredje steget kännetecknas av nedsänkning i djup anestesi; det är i detta skede som de huvudsakliga kirurgiska operationerna utförs. Det tredje stadiet nås på grund av ämnets påverkan på reflexcentra som finns i medulla oblongata. På grund av detta tappar patienten muskeltonus, hans reflexfunktion minskar och det finns ingen känslighet för yttre stimuli
- Användningen av läkemedlet för närvarande (vi har redan nämnt detta) är ganska säker. Exakt dosering av ämnet, kombinerat med en stor mängd syre, gör att du omedelbart kan gå vidare till det tredje steget och kringgå excitationssteget. Dessutom gör detta ämnet mindre giftigt
Indikationer
- Huvudindikationen för användningen av läkemedlet är situationer när patienten behöver läggas under allmän narkos (för kirurgiska ingrepp)
- I kombination med metylalkohol av salicylsyra och terpentin används det som ett lokalt botemedel med irriterande effekt. Används för neuralgi och myosit (inflammation i skelettmuskler)
- Kloroformvatten i kombination med valerianarottinktur används för att behandla buksmärtor, flatulens, hicka och som ett antiemetikum
Kontraindikationer
- Sjukdomar i det kardiovaskulära systemet
- Njur- och leversvikt
- Asteniskt syndrom
- Hud purulenta-inflammatoriska sjukdomar - för extern användning
Bieffekter
- Om läkemedlet används för att inducera anestesi genom inandning, är en försvagning av hjärtaktiviteten (upp till hjärtstillestånd), blodtrycksfall och kollaps möjlig.
- Om ångor kommer på slemhinnan kan allvarlig irritation uppstå, som kännetecknas av rodnad, sveda, kraftig slemutsöndring, tårbildning och salivutsöndring, kraftiga hostattacker, illamående, kräkningar
- Vid extern användning finns risk för allvarlig irritation eller till och med inflammation i huden.
Viktig! Om du ofta andas in ångor av ett ämne kan ett beroende utvecklas - missbruk.
Användningsinstruktioner
- För att inducera anestesi tillförs en blandning av syre och kloroform i en koncentration av 3-4 vol.%. För att upprätthålla det kirurgiska skedet krävs 1-1,5 vol.%.
- Endast kloroformvatten används oralt, där ämneshalten är 0,5 %. Det rekommenderas att ta en matsked 3-4 gånger om dagen
- När det används för utvärtes bruk appliceras läkemedlet på önskat område och gnuggas mycket försiktigt
Överdos
Även en låg koncentration av ämnet kan orsaka allvarlig förgiftning med leverskador. Samtidigt förvärras alla biverkningar. Särskilt farligt är depression av andningscentrum och allvarliga störningar i hjärtats funktion (rytmrubbningar, frekvens av sammandragningar av hjärtmuskeln, upp till hjärtstillestånd).
Vid överdosering kopplas patienten först till en ventilator och hyperventileras.
För att rena blodet utförs hemodialys.
För kloroformförgiftning är hydrokortisoninjektioner indikerade i en koncentration av 1 ml per kg kroppsvikt.
Symtomatisk terapi utförs.
Viktig! Under återhämtningsperioden efter kloroformförgiftning är det kontraindicerat att dricka alkohol och fet mat.
Jag skapade det här projektet för att på ett enkelt språk berätta om anestesi och anestesi. Om du har fått svar på din fråga och sidan var användbar för dig, tar jag gärna emot support, den kommer att hjälpa till att vidareutveckla projektet och kompensera för kostnaderna för dess underhåll.
- Isolera konturen av en vätskedroppe i problemet med att bestämma ytspänningen Isolera konturen av en droppe
- Metod för framställning av kalciumperoxid
- Feo färg. Kemiska egenskaper. Eldfast svart pyroforiskt pulver, olösligt i vatten. Metoder för att få järn
- Natriumtiosulfat Natrii thiosulfas (ln) Tiosulfat kemisk formel
- Rhodanidmetod för att bestämma järn
- Bakpulver: formel, applikation
- Karbonater. Bakpulverformel. Bakpulver: formel, tillämpning Säkerhet av bakpulver för människor
- Beskrivning av sjukdomen, tecken, behandling
- Leversjukdomar: orsaker, typer, symtom och förebyggande Vad är ett virus i levern
- Helminthic angrepp: orsaker, symtom, behandling, förebyggande
- Folkläkemedel
- Matjäsning och dess betydelse
- Studie av farmakokinetik och biotillgänglighet - journal of pharmacokinetics and pharmacodynamics Högpresterande vätskekromatografi
- Testa arbete kloroform Kloroform hemma
- Ädelgaser och deras egenskaper Ädelgaser vad som orsakar dessa gasers tröghet
- Raman och NIR-spektroskopi Problem med NIR-spektrometri och hur man löser dem
- Sidospecialiteter av tantal
- Vad är tantal och var används det?
- Molekylära effekter av enzymverkan
- Cervikal dysplasi: första tecken, symtom och behandling