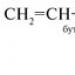Pekerjaan mandiri pada topik kimia alkena. Kumpulan karya independen pada bagian "hidrokarbon tak jenuh". Kumpulan karya mandiri bidang kimia
Cabang Yurgamysh
GBPOU "Perguruan Tinggi Kedokteran Dasar Kurgan"
Kumpulan karya mandiri bidang kimia
di bawah bagian “Hidrokarbon tak jenuh”
untuk spesialisasi 34.02.01 “Keperawatan”
disusun oleh guru kimia: N.S. Trofimova
Yurgamysh 2017
Pekerjaan mandiri
“Alkena. Komposisi, struktur. Isomerisme dan tata nama.
Sifat fisik dan kimia. Hubungan dengan alkana"
1. Sebutkan rumus umum alkena dan rumus umum alkana.
2. Buatlah rumus struktur zat-zat berikut ini:
3-metilbutena-1
2-metilbutena-1
2,2-dimetilpropana
3. Sebutkan hidrokarbon: A) CH 2 = CH-CH 2 -CH(CH 3) 2 B) (CH 3) 2 CH- C(CH 3) = CH- CH 2 - CH 3
4. Tuliskan rumus struktur isomer 2-metilpentena-1.
5. Tuliskan rumus struktur setiap homolog butena-1.
6. Jenis isomerisme apa yang menjadi ciri alkena? Buatlah rumusnya: A) trans-butena-1
B) cis-1-bromopropena
7. Tentukan reaksi hidrogenasi
C 2 H 4 + H 2 → C 2 H 6
C 2 H 4 + H 2 O → C 2 H 5 OH
C 2 H 6 → C 2 H 4 + H 2
C 2 H 4 + Cl 2 → C 2 H 6 Cl 2
8. Mengapa reaksi adisi merupakan ciri khas alkena, tetapi reaksi seperti itu umumnya tidak mungkin terjadi pada alkana?
9. Tunjukkan penilaian yang benar: A) Aturan Markovnikov - ketika hidrogen halida ditambahkan ke alkena, hidrogen terikat pada atom karbon melalui ikatan rangkap, yang mana lebih banyak atom hidrogen terikat; B) polimer adalah senyawa dengan berat molekul tinggi yang molekulnya terdiri dari banyak unit struktural yang identik.
10. Gas diperoleh di laboratorium. Untuk menetapkan strukturnya, ia dilewatkan melalui larutan brom kuning. Solusinya menjadi tidak berwarna. Gas yang dihasilkan dapat diklasifikasikan menjadi hidrokarbon apa dan mengapa?
_____________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________
11. Larutan kalium permanganat ungu dapat dihilangkan warnanya dengan menggunakan
Dukung jawaban Anda dengan persamaan reaksi.
12. Selesaikan rangkaiannya:
Tidak? ? +H 2 O +O 2
kloroetana → butana → klorobutana → butena-1 → A → ?
14. Buatlah reaksi polimerisasi yang melibatkan butena-2.
15. Berikan persamaan reaksi kimia yang menunjukkan aturan Markovnikov.
Pilihan 1
Tuliskan persamaan reaksi produksi 2-metilbutena-2 melalui dehidrasi alkohol yang sesuai dan dehidrohalogenasi haloalkana.
CH 3 -CH 2 -CH 2 OH→CH 2 =CH-CH 3 →CH 3 -CHCl-CH 3 →CH 3 -CH(CH 3)-CH(CH 3)-CH 3 →CH 3 -C(CH 3)=C(CH 3)-CH 3
Apa rumus struktur etilen hidrokarbon jika 11,2 gnya, bila direaksikan dengan HBr berlebih, diubah menjadi 27,4 g bromoalkana dengan posisi halogen pada atom karbon tersier?
Pekerjaan mandiri dengan topik “Alkena”
pilihan 2
Tuliskan persamaan reaksi untuk produksi 2,3-dimetilbutena-1 melalui dehidrasi alkohol yang sesuai dan dehidrohalogenasi haloalkana.
Reaksi apa yang dapat digunakan untuk melakukan transformasi berikut? Jika perlu, tunjukkan kondisi reaksi
C 6 H 12 →C 6 H 14 →C 3 H 6 →[ -CH 2 -CH(CH 3)- ] p
Hidrokarbon etilen seberat 7,0 g menghilangkan warna 640 g air brom dengan fraksi massa brom 2,5%. Tentukan rumus molekul alkena.
| Kartu 1. Topik: Alkena 1. Ke kelasalkena berlaku 1) C 2 H 6 2) C 3 H 4 3) C 2 H 4 4) C 5 H 12 2. Alkena dicirikan oleh isomerisme 1) kerangka karbon 2) geometris 3) posisi obligasi rangkap 4) antar kelas air dalam reaksi pembakaran etilen 4. Sebagai akibathidroklorinasi butena-1 terbentuk 1) 1-klorobutana 2) 2-klorobutana 3) 1-klorobutena-1 4) 2-klorobutena-1 5) Anda bisa mendapatkan etilen melalui reaksi 1) dehidrasi alkohol 2) dehidrogenasi alkana 3) retak 4) polimerisasi |
| Kartu 2. Topik: Alkena 1. Suatu alkena yang molekulnya mengandung 6 atom karbon memiliki rumus 1) C 6 H 14 2) C 6 H 12 3) C 6 H 10 4) C 6 H 6 2. Isomer pentena-1 adalah 1) 2-metilbeten - 1 2) siklopentana 3) penten-3 4) penten-2 3. Koefisien sebelum rumusair dalam reaksi pembakaran propena 4. Akibatnyahidrasi butena-1 terbentuk 1) butanol-1 2) butanol-2 3) 1-metilbutena-1 4) 2-metilbutena-1 5. Reaksi kualitatif terhadap alkena adalah 1) hidrogenasi 2) pembakaran 3) brominasi 4) oksidasi dengan kalium permanganat |
| Kartu 3. Topik: Alkena 1. Ke kelasalkena berlaku 1) C 5 H 12 2) C 7 H 14 3) C 6 H 10 4) C 7 H 16 2. Berapa banyak isomer yang dapat ada untuk suatu zat dengan komposisi C 4 N 8 ? 3. Koefisien sebelum rumusair dalam reaksi pembakaran butena 4. Akibat penambahan hidrogen bromida menjadi butena-1 terbentuk 1) 1-bromobutana 2) 2-bromobutana 3) 1-bromobutena-1 4) 2-bromobutena-1 5. Propena dapat diperoleh melalui reaksi 1) hidrogenasi butana 2) hidrasi propin 3) dehidrogenasi propana 4) hidrogenasi etena |
| Kartu 4. Topik: Alkena 1. Komposisialkena mencerminkan rumus umum 1) C n H 2n+2 2) C n H 2n 3) C n H 2n-2 4) C n H 2n-6 2. Isomer cis-butena-2 adalah 1) metil propana 2) trans-beten-2 3) metilsiklopropana 4) siklobutana 3. Koefisien sebelum rumusair dalam reaksi pembakaran pentena 4. Akibatnya penambahan hidrogen klorida ke pentena-1 terbentuk 1) 1-kloropentana 2) 2-kloropentana 3) 1-kloropenten-1 4) 2-kloropenten-1 5. Ketika etilen dioksidasi dengan kalium permanganat, ia terbentuk 1) karbon dioksida 4) etilen glikol |
Karya ini ditawarkan kepada mahasiswa dengan tujuan untuk memantau asimilasi materi program hidrokarbon tak jenuh (alkuna dan alkena) dan tugas: memeriksa tingkat asimilasi tata nama dan isomerisme, kemampuan memperoleh alkena dan alkuna, menyusun persamaan reaksi dengan partisipasi mereka, untuk memecahkan masalah kualitatif dan perhitungan pada topik ini.
Karya ini disusun dengan mempertimbangkan pendekatan individual:
Opsi 1 – ringan;
Opsi 2 – tingkat menengah;
Opsi 3 – rumit.
Tes
1 tugas
Pilihan 1
Berapa jumlah alkena isomer dengan komposisi C 5 H 10? Buatlah rumusnya dan beri nama.
Pilihan 2.
Buatlah rumus isomer untuk zat yang diusulkan, beri nama, tunjukkan jenis isomernya. 2,5-dimetilheksin-3
Pilihan 3
Manakah dari pasangan zat yang diusulkan yang merupakan isomer?
Sebutkan zat, sebutkan jenis isomernya.


2 tugas
1 pilihan .
Tuliskan persamaan reaksi dan beri nama semua zat.

Pilihan 2.
Lakukan transformasi, sebutkan nama zat, jenis reaksi kimia, kondisi pelaksanaannya:
Pilihan 3.
Rantai transformasi diberikan:
Lakukan transformasi, beri nama zat, tunjukkan jenis reaksinya.
3 tugas
1 pilihan
Bagaimana cara mengenali zat berikut: etana, etena, etuna?
Tuliskan persamaan reaksi.
Pilihan 2.
Sarankan metode untuk mengenali senyawa: butana, butena - 1, propuna.
Tuliskan persamaan reaksi.
Pilihan 3.
Sarankan metode untuk mengenali zat: propana, pentena - 2, pentin - 2, pentin - 1.
Tuliskan persamaan reaksinya.
4 tugas
Tugas.
1 pilihan
Berapa liter hidrogen yang diperlukan untuk menghidrogenasi sempurna 16,2 g butin - 2?
pilihan 2
Berapa massa kalsium karbida yang mengandung 15% pengotor yang harus diambil untuk memperoleh 40 liter asetilena (n.o.)?
Pilihan 3
Karbon dioksida yang dihasilkan dari pembakaran 8,4 liter etilen (n.o.) dilewatkan melalui 472 ml larutan NaOH 6% (densitas = 1,06 g/ml). Bagaimana komposisi garam yang dihasilkan dan berapa fraksi massanya dalam larutan?
Karya mandiri dengan topik “ALKYNE”.
1. Untuk senyawa 6-metilheptin-3, tuliskan rumus dua homolog dan 2 isomer.
2. Tuliskan reaksinya:
Hidrasi asetilena
Hidrogenasi 4-metilpentin-2
Pembakaran propin
Halogenasi 2,5 –dimetilhexine-3
Brominasi butin-1
Hidrogenasi 2,2,5-trimetilhexine-3
Penambahan hidrogen halida pada propuna
Polimerisasi asetilena
Dehidrogenasi metana
Dehidrogenasi etilen
8. Apa yang terbentuk jika larutan alkohol alkali bereaksi dengan 2,3-dibromoetana.
Tuliskan persamaan reaksinya.
9. Jalankan rantai:
Metana----etilen----asetilen-----aldehida asetat
1,2-dibromoetilen
10. Hitung volume asetilena yang dapat diperoleh dari 130 g kalsium karbida,
Karya mandiri dengan topik “Alkadienes. Alkuna"
Pilihan 1.
Buatlah rumus elektronik dan struktur molekul propuna, tentukan valensi dan st. oksidasi atom karbon. Tunjukkan keadaan hibridisasi di mana atom karbon pada ikatan rangkap tiga berada.
Dengan menggunakan contoh anggota kelima dari deret alkuna homolog, buatlah rumus struktur:
a) 2 isomer posisi ikatan rangkap tiga;
c) 2 isomer dari deret homolog lainnya. Sebutkan semua isomer.
Lakukan transformasi:
C 2 H 5 COONa C 2 H 6 C 2 H 4 C 2 H 2 X
Ketika 4,1 g hidrokarbon dibakar, diperoleh 13,2 g karbon monoksida (IV) dan 4,5 g air. Massa jenis uap suatu zat hidrogen adalah 41. Tentukan rumus zat tersebut.
_______________________________________________________________________
Pilihan 2.
Buatlah rumus elektronik dan struktur molekul 2,3-dimetilbutadiena-1, tentukan valensi dan st. oksidasi atom karbon. Tunjukkan keadaan hibridisasi di mana karbon pada ikatan rangkap berada.
Dengan menggunakan contoh anggota keenam dari deret homolog alkadiena, buatlah rumus struktur:
a) 2 isomer posisi ikatan;
b) 2 isomer rantai karbon;
c) isomer cis dan trans;
d) 2 isomer dari deret homolog lainnya. Sebutkan semua isomer.
3. Melakukan transformasi:
Polimer C 2 H 2 C 2 H 4 C 2 H 5 Br C 2 H 4
4. Ketika 2,8 g hidrokarbon dibakar, diperoleh 0,2 mol karbon dioksida dan 0,2 mol air. 3,64 g zat ini menempati volume 1,456 l (n.s.). Tentukan rumus molekul zat tersebut.
Tes dengan topik “Alkadienes. Alkuna"
1 .Pentine sesuai dengan rumus umum:
a) C n H 2 n -6; b) C n H 2 n -2 ; c) C n H 2 n ; d) C n H 2 n +2
2 . Panjang ikatan karbon-karbon adalah yang terpendek dalam suatu molekul:
a) C 2 H 4 b) C 2 H 2 c) C 4 H 10 d) C 5 H 10.
3 . Hidrokarbon yang orbital semua atom karbonnya terhibridisasi sp:
a) propadiena; b) propin, c) etina, d) butadiena – 1.3.
4. Pentadiena-1,4 dan 2-metilbutadiena-1,3 adalah:
a) homolog, b) zat yang sama, c) isomer geometri, d) isomer struktur.
5 . Hidrokarbon jenuh tidak berbeda dengan hidrokarbon tak jenuh:
a) jenis hibridisasi, b) kelarutan dalam air, c) adanya ikatan yang berbeda antar atom karbon, d) struktur molekul.
6 . Reaksi hidrasi melibatkan:
a) etilen, butin-2, propadiena; b) propilena, pentana, etuna;
c) butadiena -1,3, butana, siklopropana; d) etena, etana, etuna.
7 . Mereka berinteraksi dengan kalium permanganat:
a) metana, etilen, propena; b) propadiena, 2-kloropropana, propena;
c) propuna, butena-2, butadiena-1,3 d) siklopentana, etilen, etena.
8 . Asetilena tidak berinteraksi dengan:
a) air brom, b) hidrogen bromida,
c) larutan amonia perak (I) oksida, d) nitrogen.
9 . Pentin-1 dan 2-methylpentadiene-1,3 dapat dikenali:
a) larutan alkohol natrium hidroksida, b) air brom,
c) asam nitrat pekat, d) larutan amonia perak (I) oksida.
10 . Air bromin mengalami dekolorisasi dalam kondisi normal:
a) metana, etena, etuna, b) propuna, butadiena-1,3, sikloheksana,
c) butadiena-1,3, etena, propuna, d) butana, butena-1, etilen.
11. Pentin-1 dan pentin-2 dapat dikenali:
a) larutan kalium permanganat, b) air brom, c) larutan hidrogen klorida,
d) larutan amonia tembaga (I) klorida.
12 . Volume sebagian propuna (n.s.) yang mengandung 6 * 10 23 atom hidrogen adalah:
a) 22,4 liter, b) 5,6 liter, c) 7,5 liter, d) 11,2 liter.
13 . Untuk pengelasan dan pemotongan logam digunakan gas dengan fraksi massa karbon dan hidrogen masing-masing sebesar 92,31 dan 7,69%. Ini gasnya:
a) etana, b) etilen, c) asetilena, d) metana.
14 . Untuk hidrogenasi lengkap 7,8 g asetilena, Anda memerlukan hidrogen dalam volume (n.s.)…..(l).
15. Ketika 10 g sampel kalsium karbida diolah dengan air, diperoleh 2,24 liter asetilena. Fraksi massa kalsium karbida dalam sampel adalah ....(%).
16 . Dari 1,2-dikloropropana seberat 62,15 g, diperoleh 10 l (n.s.) propin. Hasil praktisnya adalah….. (%).
Pekerjaan mandiri№4. kelas 10.
Subjek:Alkana, alkena, alkuna. SAYApilihan.
a) hidrogenasi propena;
b) pembakaran asetilena;
_________________________________________________________________________
Pekerjaan mandiri No.4.kelas 10.
Subjek:Alkana, alkena, alkuna. SAYAIIpilihan.
1. Buatlah rumus struktur zat-zat berikut:
4-metilpentin-2; 3-etilpentena-2.
2. Tunjukkan sudut ikatan, jenis hibridisasi karbon, dan rumus umum alkena.
3. Pilih rumus alkana dari daftar ini:
C6H14, C8H16, C6H6, C3H6, C2H6O, C12H22O11, C5H12, C7H12.
4.Tulis persamaan reaksinya. Beri nama pada zat yang dihasilkan.
a) hidrogenasi propena;
b) pembakaran asetilena;
c) brominasi propuna (tahap pertama).
_________________________________ ____________________________________________
Pekerjaan mandiri No.4.kelas 10.
Subjek:Alkana, alkena, alkuna.IIpilihan.
1. Buatlah rumus struktur zat-zat berikut:
2.5 – dimetilheksin-3; 3,3-dimetilbutena-1.
4.Tulis persamaan reaksinya. Beri nama pada zat yang dihasilkan.
a) hidrogenasi etilen;
b) pembakaran propena;
____________________________________________ _______________________________
Pekerjaan mandiri No.4. kelas 10.
Subjek:Alkana, alkena, alkuna.SAYAVpilihan.
1. Buatlah rumus struktur zat-zat berikut:
2,5 - dimetilheksin-3; 3,3-dimetilbutena-1.
2.Tentukan sudut ikatan, jenis hibridisasi karbon, dan rumus umum alkana.
3. Pilih rumus alkena dari daftar ini:
C 3 H 4, C 6 H 14, C 8 H 16, C 6 H 6, C 3 H 6, C 2 H 4 O 2, C 6 H 12, C 4 H 6.
4.Tulis persamaan reaksinya. Beri nama pada zat yang dihasilkan.
a) hidrogenasi etilen;
b) pembakaran propena;
c) klorinasi etana (tahap pertama).
___________________________________________________________________
Hidrokarbon tak jenuh.
Alkena
KELAS 10
Pembelajaran ini merupakan pembelajaran materi baru berupa ceramah dengan unsur percakapan dan karya mandiri siswa.
Siswa bekerja dalam tiga kelompok. Pada setiap kelompok terdapat seorang guru pendamping yang membagikan pekerjaan kepada setiap siswa dalam kelompok tersebut. Setiap siswa memiliki pengingat.
PENGINGAT
Hasil pembelajaran yang direncanakanTahu: penentuan hidrokarbon tak jenuh deret etilen, rumus umum alkena, empat jenis isomerisme alkena, sifat fisik dan kimianya, cara produksi dan bidang penerapan hidrokarbon deret etilen.
Mampu untuk: jelaskan ciri-ciri pembentukan ikatan - dan -, tuliskan rumus molekul, struktur dan elektronik alkena, tentukan distribusi kerapatan elektron dalam molekul, beri nama zat deret etilen menurut tata nama sistematis dan tuliskan rumusnya menggunakan nama zat, membuat rumus berbagai isomer menggunakan rumus molekul alkena, menuliskan persamaan reaksi yang mencirikan sifat kimia alkena, membandingkan sifat alkena dengan sifat hidrokarbon jenuh, menyelesaikan masalah mencari rumus molekul .
Sasaran. Pendidikan: belajar menyimpulkan rumus umum alkena, mengetahui sifat fisika dan kimianya, mampu menuliskan rumus molekul dan rumus struktur alkena, memberi nama zat menurut sistematika tata nama, mengembangkan keterampilan memecahkan masalah mencari rumus molekul.
Pendidikan: menumbuhkan keinginan untuk belajar secara aktif, penuh minat, menanamkan kesadaran disiplin, kejelasan dan keteraturan dalam bekerja, bekerja dengan semboyan: “Satu untuk semua, dan semua untuk satu.”
Metode dan teknik pembelajaran
- Pekerjaan individu dengan kartu.
- Bekerja dalam kelompok dan berpasangan.
- Demonstrasi percobaan kimia.
- Penggunaan alat peraga teknis.
- Pekerjaan mandiri dalam menyusun rumus zat.
- Jawaban lisan di papan tulis.
- Mencatat dari buku teks di buku catatan.
Rencana topik pelajaran
(tertulis di papan tulis)
1. Struktur molekul etilen C 2 H 4.
2. Isomerisme dan tata nama alkena.
3. Pembuatan alkena.
4. Sifat fisik.
5. Sifat kimia.
6. Aplikasi.
7. Hubungan genetik.
Peralatan dan reagen. Kartu dengan tugas, proyektor grafis dan slide, tripod, alat untuk memperoleh dan mengumpulkan gas, lampu alkohol, tabung reaksi, pasir, sendok kimia; etil alkohol, kalium permanganat, air brom, asam sulfat (conc.).
SELAMA KELAS
Pembelajaran diawali dengan percakapan dalam bentuk jajak pendapat frontal. Tujuan dari bagian pelajaran ini adalah untuk menciptakan “situasi sukses”. Siswa memahami pertanyaan, mengetahui jawabannya dan terlibat aktif dalam pekerjaan.
1. Berapa panjang ikatannya?
(Panjang ikatan adalah jarak antar pusat
inti atom yang terikat dalam suatu molekul.)
2. Apa yang dapat dikatakan tentang panjang ikatan karbon-karbon zat dengan ikatan tunggal (C–C) dan rangkap (C=C)?
(Panjang ikatan tunggal karbon-karbon - 0,154 nm
ikatan rangkap – 0,133 nm, ikatan rangkap lebih kuat dan lebih pendek dari ikatan tunggal.)
3. Berapa banyak ikatan yang dapat timbul antar atom?
4. Apa yang dapat dikatakan tentang kekuatan ikatan tersebut?
(Ini kurang tahan lama dibandingkan single - koneksi.)
5. Ikatan kimia apa yang terbentuk antara awan hibridisasi?
6. Berapa banyak elektron valensi yang dimiliki atom karbon?
Pekerjaan mandiri.
Penurunan rumus molekul
Tugas. Dalam senyawa tersebut, fraksi massa karbon adalah 85,7%, fraksi massa hidrogen adalah 14,3%, massa jenis hidrogen adalah 14. Turunkan rumus molekul hidrokarbon.
(Salah satu siswa memutuskan di papan tulis.)
Diberikan:
(C) = 85,7% (atau 0,857),
(H) = 14,3% (atau 0,143),
D(H2) = 14.
Menemukan:
C X H kamu .
Larutan
M(C X H kamu) = 14 2 = 28 g/mol.
Untuk 1 mol C X H kamu M(C X H kamu) = 28 gram,
M(C) = 28 (g) 0,857 = 24 gram,
N(C) = 24 (g)/12 (g/mol) = 2 mol,
M(H) = 28 (g) 0,143 = 4 gram,
N(H) = 4 (g)/1 (g/mol) = 4 mol.
Rumus hidrokarbonnya adalah C 2 H 4.
Kami menyimpulkan bahwa molekul C 2 H 4 tidak jenuh dengan atom hidrogen.
Struktur molekul etilen C 2 H 4
Kami mendemonstrasikan model molekul hidrokarbon tertentu melalui proyektor grafis.
Molekul C 2 H 4 berbentuk datar, atom karbon yang membentuk ikatan rangkap berada dalam keadaan
sp 2-hibridisasi, sudut ikatan 120°.
Kita buat deret homologis: C 2 H 4, C 3 H 6, C 4 H 8 ... dan turunkan rumus umum C N jam 2 N .
Mari kita simpulkan tahapan yang telah kita lalui.
Isomerisme dan tata nama alkena
Jenis isomerisme
1) Perhatikan rumus struktur alkena linier dan bercabang yang memiliki rumus molekul yang sama C 4 H 8:

Isomerisme seperti ini disebut isomerisme kerangka karbon.
2) Isomerisme posisi ikatan ganda:
3) Isomerisme deret homolog yang berbeda. Rumus umumC N jam 2 N sesuai dengan dua deret homolog: alkena dan sikloparafin. Misalnya, rumus C 4 H 8 mungkin termasuk dalam senyawa dari kelas yang berbeda:

4) Isomerisme spasial atau geometris. Pada butena-2 CH 3 – CH = CH – CH 3, setiap karbon pada ikatan rangkap mempunyai substituen yang berbeda (H dan CH 3). Dalam kasus seperti itu, isomerisme cistrans dimungkinkan untuk alkena. Jika unsur-unsur rantai karbon utama berada pada salah satu sisi ikatan rangkap pada bidang molekul, maka ini adalah cisisomer; jika di sisi yang berlawanan, maka ini isomer trans:

Pekerjaan mandiri menggunakan kartu (5 menit)
Sebutkan zat-zat tersebut.
kelompok pertama:

kelompok ke-2:

kelompok ke-3:

Karya independen yang telah selesai direkam pada film dan diproyeksikan melalui proyektor grafis ke layar. Siswa melatih pengendalian diri.
Persiapan alkena
1) Dehidrasi alkohol (pengalaman demonstrasi memproduksi etilen dari etil alkohol):
![]()
2) Dehidrogenasi alkana:

3) Pirolisis dan perengkahan minyak dan gas alam:
4) Dari alkana terhalogenasi:

Properti fisik
Alkena - etena, propena dan butena - dalam kondisi normal (20 ° C, 1 atm) - gas, dari C 5 H 10 hingga C 18 H 36 - cair, alkena yang lebih tinggi - padatan. Alkena tidak larut dalam air, tetapi larut dalam pelarut organik.
Sifat kimia
Dalam kimia organik, tiga jenis reaksi kimia dipertimbangkan: substitusi, adisi, dan dekomposisi.
1) Alkena dicirikan oleh reaksi adisi.
Penambahan hidrogen (hidrogenasi):
![]()
Penambahan halogen (percobaan laboratorium penghilangan warna air brom):
![]()
Penambahan hidrogen halida:
![]()
Aturan Markovnikov: hidrogen terikat pada lokasi ikatan rangkap pada karbon yang lebih terhidrogenasi, dan halogen pada karbon yang kurang terhidrogenasi.
Misalnya:
Reaksi berlangsung melalui mekanisme ionik.
Penambahan air (reaksi hidrasi):
![]()
2) Reaksi oksidasi.

Pengalaman demonstrasi. Etena mengubah warna larutan kalium permanganat, yang membuktikan sifat etena yang tidak jenuh:
Etilen glikol digunakan sebagai antibeku; serat lavsan dan bahan peledak diperoleh darinya.
Oksidasi etena pada katalis perak menghasilkan etilen oksida:

Etilen oksida digunakan untuk memproduksi asetaldehida, deterjen, pernis, plastik, karet dan serat, serta kosmetik.
3) Reaksi polimerisasi.
Proses penggabungan banyak molekul identik menjadi molekul yang lebih besar disebut reaksi polimerisasi.
 Tentukan rumus molekul hidrokarbon yang mengandung 85,7% karbon dan mempunyai massa jenis hidrogen 21.
Tentukan rumus molekul hidrokarbon yang mengandung 85,7% karbon dan mempunyai massa jenis hidrogen 21.
Diberikan:
(C) = 0,857 (atau 85,7%),
D(H2) = 21.
Menemukan:
Larutan
M(C X H kamu) = D(H2) M(H 2) = 21 2 = 42 g/mol.
Untuk N(C X H kamu) = 1 mol M(C) = 42 0,857 = 36 gram,
N(C) = 36 (g)/12 (g/mol) = 3 mol,
M(H) = 42 – 36 = 6 gram,
N(H) = 6 (g)/1 (g/mol) = 6 mol.
Rumus hidrokarbonnya adalah C 3 H 6 (propena).
Tugas 3.Ketika 4,2 g suatu zat dibakar, 13,2 g karbon monoksida (IV) dan 5,4 g air terbentuk. Massa jenis uap zat ini di udara adalah 2,9. Tentukan komposisi molekul hidrokarbon.
Diberikan:
m(C X H kamu) = 4,2 gram,
M(CO 2) = 13,2 gram,
M(H 2 O) = 5,4 gram,
D(udara) = 2,9.
Menemukan: C X H kamu .
Larutan
M(C X H kamu) = 2,9 29 = 84 g/mol.
Untuk menyelesaikan soal tersebut, mari kita buat persamaan reaksi:
![]()
Mari kita cari massanya X mol CO 2 dan jumlah zat yang sesuai:
m(CO 2) = 84 13,2/4,2 = 264 gram,
N(CO 2) = 264 (g)/44 (g/mol) = 6 mol, X = 6.
Juga M(H 2 O) = 84 5,4/4,2 = 108 gram,
n(H 2 O) = 108 (g)/18 (g/mol) = 6 mol, y = 12.
C 6 H 12 – heksena.
Setiap kelompok menyerahkan tugas yang telah mereka selesaikan pada selembar kertas. Ini diikuti dengan ringkasan pelajaran.
Pekerjaan rumah.Rudzitis G.E., Feldman F.G. Kimia-10. M.: Pendidikan, 1999, bab IV, § 1, hal. 30–38, gbr. 10, hal. 38. Siapkan soal 6, 7 dari rencana pembelajaran topik pelajaran seminar, pelajari materi pelajaran-ceramah.
Pekerjaan mandiri№3. kelas 10.
Subjek:Alkena. SAYApilihan.
3-etilpentena-2; 2,5-dimetilheksena-3.
C6H14, C8H16, C6H6, C3H6, C2H6O, C12H22O11, C5H12, C7H12.
a) hidrogenasi propena;
b) pembakaran etilen;
c) klorinasi butena-1.
_________________________________________________________________________
Pekerjaan mandiri No.3.kelas 10.
Subjek:Alkena. SAYAIIpilihan.
1. Buatlah rumus struktur zat-zat berikut:
3-metilpentena-1; 2,3-dimetilbutena-1.
2. Tunjukkan sudut ikatan, jenis hibridisasi karbon, dan rumus umum alkena.
3. Untuk butena-2, tuliskan rumus struktur isomer cis dan trans.
4.Tulis persamaan reaksinya. Beri nama pada zat yang dihasilkan.
a) hidrogenasi propena;
b) eliminasi hidrogen halida dari 2-klorobutana;
c) polimerisasi etilen.
____________________________________________________________________________
Pekerjaan mandiri No.3.kelas 10.
Subjek:Alkena.IIpilihan.
1. Buatlah rumus struktur zat-zat berikut:
3,3-dimetilbutena-1; 2-metil-3-etilpentena-2.
2. Tunjukkan sudut ikatan, jenis hibridisasi karbon, dan rumus umum alkena.
3. Pilih rumus alkena dari daftar ini:
C 3 H 4, C 6 H 14, C 8 H 16, C 6 H 6, C 3 H 6, C 2 H 4 O 2, C 6 H 12, C 4 H 6.
4.Tulis persamaan reaksinya. Beri nama pada zat yang dihasilkan.
a) hidrogenasi butena-2;
b) pembakaran metana;
c) hidrasi propena.
____________________________________________ _______________________________
Pekerjaan mandiri No.3. kelas 10.
Subjek:Alkena.SAYAVpilihan.
1. Buatlah rumus struktur zat-zat berikut:
2,3,4-trimetilpentena-2; 4,5-dimetilokten-4.
2. Tunjukkan sudut ikatan, jenis hibridisasi karbon, dan rumus umum alkena.
3. Tuliskan rumus struktur semua hidrokarbon dengan komposisi C 4 H 8 dan beri nama.
4.Tulis persamaan reaksinya. Beri nama pada zat yang dihasilkan.
a) hidrogenasi etilen;
b) pembakaran propena;
c) interaksi butena-2 dengan hidrogen bromida.
___________________________________________________________________
Masalah alkena
Sifat kimianya sangat berbeda dengan sifat ikatan rangkap yang menyebabkan reaksi adisi; secara umum alkena merupakan senyawa yang lebih reaktif. Rumus umum senyawa tersebut adalah СnH2n.
Di dalam masalah pada alkena reaksi oksidasi diberikan. Dalam larutan kalium permanganat, KMnO4 dioksidasi menjadi diol - alkohol dihidrat, dan permanganat direduksi menjadi mangan (IV) oksida. Reaksinya akan terlihat seperti ini:
3|СnH2n + 2OH(-) -2e → CnH2n(OH)2
2 |MnO4(-) +2H2O +3e → MnO2 + 4OH(-)
3CnH2n +6OH(-) +2MnO4(-) + 4H2O → 3CnH2n(OH)2 + 2MnO2 + 8OH(-).
Persamaan akhir:
ZS n H 2 n + 2KMnO 4 + 4H 2 O → 3C n H 2 n (OH) 2 + 2MnO 2 ↓ + 2KOH
Endapan yang terbentuk adalah mangan (IV) oksida - MnO2. Mari kita nyatakan massa alkena sebagai X. Maka massa MnO2 akan sama dengan 2,07X
Menurut reaksinya, alkena dan mangan oksida bereaksi 3:2.
Artinya perbandingan mol suatu zat dapat dituliskan sebagai berikut:
X\ 3·(12n +2n) = 2,07x\87·2
dengan 12n+2n adalah massa molar, dan 87 g\mol adalah massa molar MnO2
n= 2
Itu. alkena, yang mengalami oksidasi - etilen - C2H4.
Soal pada alkena No.2

Sifat kimia ditentukan oleh kemampuannya mengikat zat; ikatan rangkap berubah menjadi ikatan tunggal:
nH2n + Cl2 → CnH2nCl2
CnH2n + Br2 → CnH2nBr2
m(CnH2nCl2) = 56,5 g\mol
m(CnH2nBr2) = 101 g\mol
Massa alkena yang masuk ke dalam reaksi adalah sama, yang berarti jumlah molnya sama.
Oleh karena itu, kami menyatakan jumlah mol hidrokarbon - n(CnH2n):
m(CnH2nCl2) \ (12n+2n+71) = m(nH2nBr2) \ (12n+2n+160)
12n+2n+71 adalah massa molar turunan dikloro,
(12n+2n+160) adalah massa molar turunan dibromo.
56,5 \ (12n+2n+71) = 101 \ (12n+2n+160)
n= 3, alkena - C3H6
Sebaliknya, mereka terutama mengalami reaksi adisi. DI DALAM masalah pada alkena semua reaksi sederhana dan biasanya bermuara pada penentuan rumus suatu zat.
Soal pada alkena No.3
Persamaan reaksi:
Alkena hanya bereaksi dengan katalis, jadi hanya akan ada satu reaksi pada soal ini.
m(Br2) = m(larutan) ω = 100 g 0,181 = 18,1 g
Mari kita nyatakan massa brom yang bereaksi sebagai x
Brom dalam larutan akan ditentukan oleh massa brom yang tidak bereaksi
m(Br2) = 18,1 - x.
Massa larutan = 100 + m(C3H6).
- HAARP - senjata psikotronik dan iklim
- Transmigrasi jiwa setelah kematian
- Nyanyian gereja oleh paduan suara Biara Sretensky
- Presentasi tentang bentuk, ukuran dan pergerakan bumi, konsekuensi geografisnya, presentasi untuk pelajaran geografi (kelas 5) dengan topik
- Peter I tidak membawa kentang ke Rusia!
- Arnold Schoenberg malam yang tercerahkan
- Kutipan inspiratif pro dan anti-globalisasi dari para pakar ekonomi
- Yang Mulia Anthony dan Theodosius dari Kiev-Pechersk
- Doa syukur yang kuat kepada Tuhan
- Tahun Orang Baik, atau tentang Kesukarelawanan dan Kesukarelaan
- Perasaan tidak enak. Jijik bagi orang-orang. Jijik adalah perasaan negatif manusia dan kemampuan untuk mengalami permusuhan atau antipati yang tajam, dikombinasikan dengan rasa jijik dan kenyang
- Jam pelajaran “Hidup diberikan untuk perbuatan baik T koti teman baik baca
- Konsep konsekuensi persamaan
- Karya mandiri kimia organik dengan topik: "Alkana", "Alkena", "Alkuna"
- Kumpulan karya independen pada bagian "hidrokarbon tak jenuh"
- Gaya hidup beberapa mamalia
- Burung biru. Blue Bird. Gaya hidup dan habitat burung biru. Lihat apa itu "Burung Biru" di kamus lain
- Cara memasak susu kental di rumah
- Kenari (burung kutilang kenari)
- Burung camar berkepala hitam Burung camar berkepala coklat