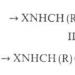Karbonat. Rumus soda kue. Soda kue: formula, aplikasi Keamanan soda kue bagi manusia
Natrium karbonat Na 2 CO 3 . soda abu. Berwarna putih, meleleh dan terurai bila dipanaskan. Sensitif terhadap kelembaban dan karbon dioksida di udara. Membentuk dekahidrat ( soda kristal). Ini sangat larut dalam air, terhidrolisis pada anion, dan menciptakan lingkungan yang sangat basa dalam larutan. Terurai dengan asam kuat. Dipulihkan dengan minuman bersoda. Masuk ke dalam reaksi pertukaran ion.
Reaksi kualitatif ke ion CO 3 2‑ – pembentukan endapan putih barium karbonat, terurai oleh asam kuat (HCl, HNO 3) dengan pelepasan karbon dioksida.
Ini digunakan untuk sintesis senyawa natrium, menghilangkan kesadahan air tawar “permanen”, dalam produksi kaca, sabun dan deterjen lainnya, selulosa, cat mineral, enamel. Di alam ditemukan di air garam tanah dan air garam danau garam.
Persamaan reaksi yang paling penting:

Kuitansi V industri (metode Solvay 1861–1863):
a) campuran NH 3 dan CO 2 dilewatkan melalui larutan NaCl jenuh:
NaCl + NH 3 + H 2 O + CO 2 = NH 4 Cl + NaHCO 3 ↓
(dalam kondisi ini, soda kue sedikit larut);
b) endapan NaHCO 3 mengalami dehidrasi ( kalsinasi):
2NaHCO 3 = Na 2 CO 3+ H 2 O + CO 2
Kalium karbonat K 2 CO 3. Oksol. Nama teknis kalium karbonat. Putih, higroskopis. Meleleh tanpa dekomposisi, dan terurai pada pemanasan lebih lanjut. Sensitif terhadap kelembaban dan karbon dioksida di udara. Sangat larut dalam air, terhidrolisis pada anion, menciptakan lingkungan yang sangat basa dalam larutan. Terurai dengan asam kuat. Masuk ke dalam reaksi pertukaran ion.
Ini digunakan dalam produksi kaca optik, sabun cair, cat mineral, banyak senyawa kalium, sebagai zat dehidrasi.
Persamaan reaksi yang paling penting:

Kuitansi V industri :
a) memanaskan kalium sulfat [bahan baku alami - mineral Kain KMg(SO 4)Cl ZN 2 O dan sekolah K 2 Mg(SO 4) 2 6H 2 O] dengan kapur mati Ca(OH) 2 dalam atmosfer CO (tekanan = 15 atm):
K 2 SO 4 + Ca(OH) 2 + 2СО = 2K(HCOO) + CaSO 4
b) kalsinasi kalium format K(HCOO) di udara:
2K(HCOO) + O 2 = K 2 CO 3 + H 2 O + CO 2
Natrium bikarbonat NaHCO3. Garam okso asam. Nama teknis bubuk soda kue. Serbuk gembur berwarna putih. Ketika dipanaskan sedikit, ia terurai tanpa meleleh, ketika basah, ia mulai terurai pada suhu kamar. Cukup larut dalam air, menghidrolisis anion dalam jumlah kecil. Terurai oleh asam, dinetralkan oleh basa. Masuk ke dalam reaksi pertukaran ion.
Reaksi kualitatif pada ion HCOd - pembentukan endapan putih barium karbonat di bawah aksi air barit dan penguraian endapan oleh asam kuat (HCl, HNO 3) dengan pelepasan karbon dioksida. Ini digunakan dalam industri makanan sebagai obat.
Persamaan reaksi yang paling penting:

Kuitansi: kejenuhan larutan Na 2 CO 3 (lihat) dengan karbon dioksida.
Kalsium karbonat CaCO3. Oksol. Bahan alami yang umum, komponen utama batuan sedimen adalah batu kapur (varietasnya adalah kapur, marmer, tufa berkapur, napal), CaCO 3 murni di alam adalah mineral kalsit. Putih, terurai saat dipanaskan, meleleh di bawah tekanan CO2 berlebih. Tidak larut dalam air (= 0,0007 g/100 g H 2 O).
Bereaksi dengan asam, garam amonium dalam larutan panas, kokas. Ini ditransfer ke dalam larutan melalui aksi karbon dioksida berlebih dengan pembentukan bikarbonat Ca(HCO 3) 2 (hanya ada dalam larutan), yang menentukan kesadahan “sementara” air tawar (bersama dengan garam magnesium dan besi). Penghilangan kesadahan (pelunakan air) dilakukan dengan cara perebusan atau netralisasi dengan kapur sirih.
Digunakan untuk produksi CaO, CO 2, semen, kaca dan pupuk mineral [termasuk kapur nitrat Ca(NO 3) 2 4H 2 O], sebagai bahan pengisi kertas dan karet, batu bangunan (batu pecah) dan komponen beton dan batu tulis, dalam bentuk bubuk endapan - untuk produksi krayon sekolah, bubuk gigi dan pasta, campuran untuk mengapur tempat.
Persamaan reaksi yang paling penting:

Soda kue, atau soda minum, adalah senyawa yang banyak dikenal dalam pengobatan, masakan, dan konsumsi rumah tangga. Ini adalah garam asam, molekul yang dibentuk oleh ion natrium dan hidrogen bermuatan positif, dan anion dari residu asam asam karbonat. Nama kimia soda adalah natrium bikarbonat atau natrium bikarbonat. Rumus senyawa menurut sistem Hill : CHNaO 3 (rumus kotor).
Perbedaan garam asam dan garam sedang
Asam karbonat membentuk dua kelompok garam - karbonat (sedang) dan bikarbonat (asam). Nama sepele karbonat - soda - muncul di zaman kuno. Penting untuk membedakan antara garam sedang dan garam asam berdasarkan nama, rumus dan sifat.
Na 2 CO 3 - natrium karbonat, dinatrium karbonat, soda cuci abu. Berfungsi sebagai bahan baku produksi kaca, kertas, sabun, dan digunakan sebagai deterjen.
NaHCO 3 - natrium bikarbonat. Komposisi tersebut menunjukkan bahwa zat tersebut adalah garam monosodium dari asam karbonat. Senyawa ini dibedakan dengan adanya dua ion positif yang berbeda - Na + dan H +. Secara eksternal, zat putih kristal serupa, sulit dibedakan satu sama lain.
Zat NaHCO 3 dianggap sebagai soda kue bukan karena digunakan secara internal untuk menghilangkan dahaga. Padahal zat ini bisa digunakan untuk membuat minuman bersoda. Larutan bikarbonat ini diminum jika terjadi peningkatan keasaman jus lambung. Dalam hal ini, kelebihan proton H+ dinetralkan, yang mengiritasi dinding lambung, menyebabkan nyeri dan rasa terbakar.
Sifat fisik soda kue
Bikarbonat adalah kristal monoklinik putih. Senyawa ini mengandung atom natrium (Na), hidrogen (H), karbon (C) dan oksigen. Massa jenis zat tersebut adalah 2,16 g/cm3. Titik lebur - 50-60 °C. Natrium bikarbonat adalah bubuk putih susu, senyawa padat kristal halus, larut dalam air. Soda kue tidak terbakar, dan bila dipanaskan di atas 70 ° C, ia terurai menjadi natrium karbonat, karbon dioksida, dan air. Dalam kondisi produksi, bikarbonat butiran lebih sering digunakan.

Keamanan soda kue bagi manusia
Senyawa ini tidak berbau dan rasanya pahit serta asin. Namun, tidak disarankan untuk mencium atau merasakan zat tersebut. Menghirup natrium bikarbonat dapat menyebabkan bersin dan batuk. Salah satu kegunaannya didasarkan pada kemampuan soda kue untuk menetralisir bau. Bedaknya bisa digunakan untuk merawat sepatu olahraga hingga menghilangkan bau tak sedap.
Soda kue (natrium bikarbonat) merupakan zat yang tidak berbahaya jika terkena kulit, namun dalam bentuk padat dapat menyebabkan iritasi pada selaput lendir mata dan kerongkongan. Dalam konsentrasi rendah, larutan tidak beracun dan dapat dikonsumsi secara oral.
Natrium bikarbonat: rumus senyawa
Rumus kasar CHNaO 3 jarang ditemukan dalam persamaan reaksi kimia. Faktanya adalah tidak mencerminkan hubungan antar partikel yang membentuk natrium bikarbonat. Rumus yang biasa digunakan untuk mengkarakterisasi sifat fisika dan kimia suatu zat adalah NaHCO 3 . Susunan relatif atom dicerminkan oleh model molekul bola-dan-tongkat:

Jika Anda mengetahui dari tabel periodik massa atom natrium, oksigen, karbon, dan hidrogen. maka Anda dapat menghitung massa molar zat natrium bikarbonat (rumus NaHCO 3):
Ar(Na) - 23;
Ar(O) - 16;
Ar(C) - 12;
Ar(H) - 1;
M (CHNaO 3) = 84 g/mol.
Struktur materi
Natrium bikarbonat adalah senyawa ionik. Kisi kristal mencakup kation natrium Na +, yang menggantikan satu atom hidrogen dalam asam karbonat. Komposisi dan muatan anionnya adalah HCO 3 -. Setelah pembubaran, terjadi disosiasi parsial menjadi ion yang membentuk natrium bikarbonat. Rumus yang mencerminkan fitur struktural adalah sebagai berikut:

Kelarutan soda kue dalam air
7,8 g natrium bikarbonat dilarutkan dalam 100 g air. Zat tersebut mengalami hidrolisis:
NaHCO 3 = Na + + HCO 3 - ;
H 2 O ↔ H + + OH - ;
Jika persamaan dijumlahkan, ternyata ion hidroksida terakumulasi dalam larutan (reaksi basa lemah). Cairan tersebut mengubah fenolftalein menjadi merah muda. Warna indikator universal berupa potongan kertas dalam larutan soda berubah dari kuning-oranye menjadi abu-abu atau biru.
Tukar reaksi dengan garam lain
Larutan natrium bikarbonat dalam air masuk ke dalam reaksi pertukaran ion dengan garam lain, asalkan salah satu zat yang baru terbentuk tidak larut; atau gas terbentuk, yang dikeluarkan dari bola reaksi. Ketika berinteraksi dengan kalsium klorida, seperti yang ditunjukkan pada diagram di bawah, diperoleh endapan putih kalsium karbonat dan karbon dioksida. Ion natrium dan klorin tetap berada dalam larutan. Persamaan molekul reaksi:

Interaksi soda kue dengan asam
Natrium bikarbonat bereaksi dengan asam. Reaksi pertukaran ion disertai dengan pembentukan garam dan asam karbonat lemah. Pada saat diterima, ia terurai menjadi air dan karbon dioksida (menguap).
Dinding perut manusia menghasilkan asam klorida, yang ada dalam bentuk ion
H+ dan Cl-. Jika Anda mengonsumsi natrium bikarbonat secara oral, reaksi terjadi dalam larutan jus lambung dengan partisipasi ion:
NaHCO 3 = Na + + HCO 3 - ;
HCl = H + + Cl - ;
H 2 O ↔ H+ + OH -;
HCO 3 - + H + = H 2 O + CO 2.
Dokter tidak menganjurkan penggunaan natrium bikarbonat terus-menerus jika terjadi peningkatan keasaman lambung. Petunjuk penggunaan obat mencantumkan berbagai efek samping penggunaan soda kue setiap hari dan jangka panjang:
- peningkatan tekanan darah;
- bersendawa, mual dan muntah;
- kecemasan, kurang tidur;
- penurunan nafsu makan;
- sakit perut.

Mendapatkan Soda Kue
Di laboratorium, natrium bikarbonat dapat diperoleh dari soda ash. Metode yang sama digunakan sebelumnya dalam produksi bahan kimia. Metode industri modern didasarkan pada interaksi amonia dengan karbon dioksida dan kelarutan soda kue yang buruk dalam air dingin. Amonia dan karbon dioksida (karbon dioksida) dilewatkan melalui larutan natrium klorida. Larutan amonium klorida dan natrium bikarbonat terbentuk. Ketika didinginkan, kelarutan soda kue berkurang, kemudian zat tersebut mudah dipisahkan dengan penyaringan.
Di mana natrium bikarbonat digunakan? Penggunaan soda kue dalam pengobatan
Banyak orang mengetahui bahwa atom logam natrium berinteraksi kuat dengan air, bahkan uapnya di udara. Reaksi dimulai secara aktif dan disertai dengan pelepasan sejumlah besar panas (pembakaran). Tidak seperti atom, ion natrium adalah partikel stabil yang tidak membahayakan organisme hidup. Sebaliknya, mereka berperan aktif dalam mengatur fungsinya.
Bagaimana zat natrium bikarbonat, yang tidak beracun bagi manusia dan berguna dalam banyak hal, digunakan? Penerapannya didasarkan pada sifat fisik dan kimia baking soda. Bidang yang paling penting adalah konsumsi rumah tangga, industri makanan, kesehatan, obat tradisional, dan minuman.
Di antara sifat utama natrium bikarbonat adalah netralisasi peningkatan keasaman sari lambung, penghapusan nyeri jangka pendek akibat hiperasiditas sari lambung, tukak lambung dan tukak duodenum. Efek antiseptik larutan soda kue digunakan dalam pengobatan sakit tenggorokan, batuk, mabuk, dan mabuk laut. Cuci rongga mulut dan hidung serta selaput lendir mata dengannya.

Berbagai bentuk sediaan natrium bikarbonat banyak digunakan, misalnya bubuk, yang dilarutkan dan digunakan untuk infus. Solusinya diresepkan untuk diminum pasien, dan luka bakar dicuci dengan asam. Natrium bikarbonat juga digunakan untuk membuat tablet dan supositoria rektal. Petunjuk obat berisi penjelasan rinci tentang tindakan farmakologis dan indikasi. Daftar kontraindikasi sangat singkat - intoleransi individu terhadap zat tersebut.
Menggunakan soda kue di rumah
Natrium bikarbonat adalah "ambulans" untuk sakit maag dan keracunan. Dengan menggunakan baking soda di rumah, Anda dapat memutihkan gigi, mengurangi peradangan pada jerawat, dan menyeka kulit untuk menghilangkan kelebihan minyak. Natrium bikarbonat melembutkan air dan membantu membersihkan kotoran dari berbagai permukaan.
Saat mencuci pakaian rajut wol dengan tangan, Anda bisa menambahkan soda kue ke dalam air. Zat ini menyegarkan warna kain dan menghilangkan bau keringat. Seringkali, saat menyetrika produk sutra, muncul tanda kuning dari setrika. Dalam hal ini, pasta soda kue dan air akan membantu. Bahan-bahan tersebut harus dicampur secepat mungkin dan dioleskan pada noda. Saat pasta mengering, bersihkan dengan sikat dan bilas produk dengan air dingin.
Dalam reaksi dengan asam asetat, natrium asetat diperoleh dan karbon dioksida dilepaskan dengan cepat, sehingga seluruh massa berbusa: NaHCO 3 + CH 3 COOH = Na + + CH 3 COO - + H 2 O + CO 2. Proses ini terjadi setiap kali, dalam pembuatan minuman bersoda dan kembang gula, soda kue “dipadamkan” dengan cuka.

Rasa makanan yang dipanggang akan lebih lembut jika Anda menggunakan jus lemon daripada cuka sintetis yang dibeli di toko. Sebagai upaya terakhir, Anda bisa menggantinya dengan campuran 1/2 sdt. bubuk asam sitrat dan 1 sdm. aku. air. Soda kue dengan asam ditambahkan ke dalam adonan sebagai salah satu bahan terakhir agar makanan yang dipanggang bisa langsung dimasukkan ke dalam oven. Selain natrium bikarbonat, amonium bikarbonat kadang-kadang digunakan sebagai bahan ragi.
Udara, cairan yang disaring dan air pencuci dari bagian dalam drum 7 menuju ke separator 11, dimana udara dipisahkan dari fasa cair dan menuju ke PVFL.
Filtrat dari pemisah (11) melalui pipa barometrik (12) menuju ke pengumpul cairan penyaring (13), kemudian dipompa keluar dengan pompa (14) untuk distilasi.
Ketika drum berputar, lapisan natrium bikarbonat yang menempel pada permukaan filter berada di bawah roller pemeras 6 untuk menghilangkan retakan yang terbentuk pada permukaan sedimen, yang melaluinya udara dan air pencuci dapat masuk ke dalam drum. Setelah roller pemeras, sedimen dicuci dengan cairan lemah atau air yang berasal dari tangki bertekanan 4 untuk membilas air ke dalam bak 3, yang mendistribusikan air dalam aliran yang merata ke seluruh lebar drum. Jumlah air yang disuplai untuk mencuci diatur dengan menggunakan keran yang dipasang di antara tangki tekanan 4 dan bak 3. Air cucian dicampur dengan cairan penyaring di dalam drum dan dialirkan ke separator 11.
Natrium bikarbonat yang telah dicuci dipadatkan kembali dengan roller pemeras kedua (6) searah putaran drum, dikeringkan dengan udara yang dihisap melalui lapisan sedimen dan disuplai melalui pipa 5, dan dipotong dari kain saring dengan pisau 8 ke konveyor 10, yang mana memasok natrium bikarbonat mentah ke oven soda.
Kalsinasi natrium bikarbonat
Kalsinasi - dekomposisi termal natrium bikarbonat - adalah tahap akhir dalam produksi soda abu. Tujuan utama dari bagian kalsinasi adalah untuk memperoleh sejumlah soda ash dalam bentuk aliran material yang kontinyu.
Natrium bikarbonat teknis harus berwarna putih. Munculnya warna menunjukkan korosi pada peralatan baja pada bagian penyerapan dan karbonisasi. Sedimen diwarnai oleh oksida besi yang masuk akibat korosi.
Proses kalsifikasi dapat ditunjukkan dengan persamaan:
2 NaHCO3(padat)=Na2CO3(padat)+CO2(gas)+H2O(uap).
Selain reaksi utama ini, ketika bikarbonat teknis dipanaskan, reaksi tambahan dapat terjadi:
(NH4)2CO3↔2NH3(gas)+СО2(gas)+Н2О(uap),
NH4 HCO3↔2NH3(gas)+СО2(gas)+Н2О(uap).
Amonium klorida bereaksi jika dipanaskan dengan natrium bikarbonat sesuai reaksinya
NH4Cl(pelarut)+ NaHCO3 (pelarut)↔NaCl(pelarut)+ NH3(gas)+СО2(gas)+Н2О.
Natrium karbamat dengan adanya air bila dipanaskan berubah menjadi soda sesuai dengan reaksinya
2NaCO2NH2+ Н2О↔ Na2CO3(padat)+СО2(gas)+2NH3(gas).
Jadi, akibat kalsinasi, Na2CO3 dan NaCl tetap berada dalam fase padat, dan NH3, CO2 dan H2O masuk ke fase gas.
Kehadiran uap air dalam bikarbonat memperumit desain peralatan, karena natrium bikarbonat basah tidak mengalir bebas, menggumpal dan menempel pada dinding peralatan. Yang terakhir ini dijelaskan oleh fakta bahwa uap air, yang merupakan larutan jenuh NaHCO3, menguap secara intensif ketika bersentuhan dengan permukaan yang panas. Fase padat yang dilepaskan, mengkristal, membentuk kerak yang melekat erat pada permukaan.
Lapisan soda padat, yang memiliki konduktivitas termal rendah, mengganggu perpindahan panas, dan pada kompor soda yang dipanaskan dari luar oleh gas buang, hal ini menyebabkan panas berlebih dan terbakarnya dinding tungku. Untuk mengatasi fenomena ini, natrium bikarbonat basah dicampur dengan soda panas (retur). Dalam hal ini, fase padat baru terbentuk - trona (NaHCO3 Na2CO3 2 H2O). Kelembapan bebas terikat menjadi kelembapan kristalisasi, dan produk menjadi mengalir bebas.
Selama kalsinasi natrium bikarbonat dan trona, CO2, NH3 dan uap air dilepaskan ke fase gas. Amonia dan karbon dioksida harus dikembalikan ke produksi. Karbon dioksida digunakan dalam proses karbonisasi air garam amonia, yang berguna untuk memiliki gas dengan kandungan CO2 yang tinggi.
Proses kristalisasi dapat dibagi menjadi tiga periode waktu. Periode pertama ditandai dengan kenaikan suhu yang cepat. Penguraian bikarbonat diamati, dan semua panas digunakan untuk memanaskan bahan, menghilangkan air kristalisasi dari takhta dan menguraikan garam amonium karbonat. Periode kedua ditandai dengan suhu material yang konstan (t~125°C). Panas yang disuplai digunakan untuk dekomposisi termal NaHCO3. Pada periode ketiga, suhu massa reaksi mulai meningkat tajam. Hal ini menunjukkan bahwa proses penguraian bikarbonat telah berakhir dan panas yang disuplai digunakan untuk memanaskan soda yang dihasilkan. Dalam praktiknya, untuk mempercepat proses penguraian NaHCO3, suhu soda di outlet tungku dijaga pada kisaran 140 – 160°C.
Diagram teknologi proses kalsinasi
Beras. 11. Skema pemisahan kalsinasi:
1- kondensor uap; pengaduk 2 umpan; 3.15 – pengumpan sel; 4.10 – konveyor sabuk; 5 – pengumpan bergetar, 6 – saluran-hopper; dumper 7 bajak; 8,9,14,16-pengangkut; 11-siklon; pengumpul gas 12-kalsinasi; 13-pemisah;17-pengumpul kondensat; pompa 18 sentrifugal; 19-kolektor cairan lemah; Pendingin gas kalsinasi 20, unit pendingin pereduksi 21 (ROU); 22 - mesin cuci gas kalsinasi; 23 - pengumpul cairan pencuci.
Natrium bikarbonat basah yang dicuci dalam filter dari konveyor sabuk umum 10 dengan bajak dumper 7 dimasukkan ke dalam hopper 6 dari pengumpan bergetar 5, dari mana pengumpan bergetar dan konveyor sabuk 4 melalui pengumpan sel 3 dimasukkan ke dalam mixer 2. Mixer menerima kembali soda dan soda yang dipisahkan dari gas kalsinasi dalam siklon 11.
Trona yang disiapkan dalam mixer diarahkan ke ruang antar tabung drum kalsiner 1. Sebagai hasil dari perlakuan panas, trona menghasilkan soda abu dan gas kalsinasi. Soda ash dikeluarkan dari calciner melalui cell feeder 15 dan masuk ke sistem conveyor 8, 9, 16. Soda diambil dari conveyor miring 8 melalui feeder ke dalam mixer. Sisa soda diangkut ke gudang melalui konveyor 9 dan 14.
Gas kalsinasi dikeluarkan dari calciner melalui mixer 2, di mana ruang hampa dibuat menggunakan kompresor. Dalam perjalanan menuju kompresor, gas-gas tersebut mengalami pembersihan kering pada siklon 11 dan pembersihan basah pada bengkel manifold gas kalsinasi 12 dan mesin cuci 22. Sebelum mesin cuci, gas kalsinasi didinginkan dalam lemari es 20.
Untuk irigasi, apa yang disebut cairan lemah disuplai ke pengumpul gas kalsinasi, yang dibentuk oleh kondensasi uap air di lemari es gas kalsinasi. Cairan ini, jika bersentuhan dengan gas, menyerap sebagian amonia dan debu soda, kemudian mengalir ke pengumpul 19.
Dalam lemari es (20), gas mengalir dari atas ke bawah melalui ruang antar tabung, dan air pendingin bergerak berlawanan arah di dalam tabung. Untuk mencegah kristalisasi tabung lemari es dan untuk membersihkan gas dari debu soda dengan lebih baik, ruang antar tabung diairi dengan cairan lemah. Di dalam mesin cuci, gas diairi dengan air, sementara itu juga didinginkan dan dicuci seluruhnya dari soda dan amonia.
Untuk memanaskan calciner, disuplai uap air bertekanan tinggi. Sebelum dimasukkan ke dalam kalsiner, ia melewati unit pendingin reduksi (RCU), dimana suhunya diturunkan hingga 270°C dan tekanan menjadi 3 MPa. Uap mengembun di dalam tabung kalsiner, melepaskan panas ke bahan yang dikalsinasi. Kondensat dari calciner dibuang ke pengumpul kondensat (17) dan kemudian ke ekspander, di mana kondensat diubah menjadi uap bertekanan rendah.
Soda
(natron, natrium bikarbonat, natrium bikarbonat) - garam natrium yang menetralkan asam. Soda kue adalah natrium bikarbonat NaHCO 3, natrium bikarbonat Secara umum, "soda" adalah nama teknis untuk garam asam natrium karbonat H 2 CO 3. Tergantung pada komposisi kimia senyawanya, soda kue (soda kue, natrium bikarbonat, natrium bikarbonat, natrium bikarbonat) - NaHCO 3, soda abu (natrium karbonat, natrium karbonat anhidrat) - Na 2 CO 3 dan soda kristal - Na 2 CO Dibedakan 3. 10H 2 O, Na 2 CO 3 .7H 2 O, Na 2 CO 3 .H 2 O. Soda kue buatan (NaHCO3) adalah bubuk kristal putih.
Danau soda modern dikenal di Transbaikalia dan Siberia Barat; Danau Natron di Tanzania dan Danau Searles di California sangat terkenal. Trona, yang memiliki kepentingan industri, ditemukan pada tahun 1938 sebagai bagian dari rangkaian Sungai Hijau Eosen (Wyoming, AS).
Di AS, soda alami memenuhi lebih dari 40% kebutuhan negara akan mineral ini. Di Rusia, karena kurangnya deposit besar, soda tidak diekstraksi dari mineral.
Soda dikenal manusia sekitar satu setengah hingga dua ribu tahun SM, dan mungkin bahkan lebih awal. Itu ditambang dari danau soda dan diekstraksi dari beberapa deposit dalam bentuk mineral. Informasi pertama tentang produksi soda dengan menguapkan air dari danau soda berasal dari tahun 64 Masehi. Hingga abad ke-18, para alkemis di semua negara membayangkannya sebagai zat tertentu yang mendesis dengan pelepasan beberapa jenis gas di bawah pengaruh asam yang dikenal pada saat itu - asetat dan sulfat. Pada masa dokter Romawi Dioscorides Pedanius, tidak ada seorang pun yang mengetahui komposisi soda. Pada tahun 1736, ahli kimia, dokter, dan ahli botani Perancis Henri Louis Duhamel de Monceau pertama kali berhasil memperoleh soda yang sangat murni dari air danau soda. Ia mampu membuktikan bahwa soda mengandung unsur kimia “Natr”. Di Rusia, bahkan pada masa Peter Agung, soda disebut “zoda” atau “gatal” dan hingga tahun 1860 diimpor dari luar negeri. Pada tahun 1864, pabrik soda pertama yang menggunakan teknologi Leblanc Prancis muncul di Rusia. Berkat munculnya pabrik-pabriknya, soda menjadi lebih mudah diakses dan memulai jalur kemenangannya sebagai produk kimia, kuliner, dan bahkan obat-obatan.
Sifat kimia
Natrium bikarbonat adalah garam natrium asam dari asam karbonat.Berat molekul (menurut massa atom internasional 1971) - 84,00.
Reaksi dengan asam
Natrium bikarbonat bereaksi dengan asam membentuk garam dan asam karbonat, yang segera terurai menjadi karbon dioksida dan air:
NaHCO 3 + HCl → NaCl + H 2 CO 3
H 2 CO 3 → H 2 O + CO 2
dalam memasak, reaksi berikut dengan asam asetat lebih sering terjadi, dengan pembentukan natrium asetat:
NaHCO 3 + CH 3 COOH → CH 3 COONa + H 2 O + CO 2
Soda larut dengan baik dalam air. Larutan soda kue dalam air memiliki reaksi yang sedikit basa. Desisan soda merupakan akibat pelepasan karbon dioksida CO2 akibat reaksi kimia.
Dekomposisi termal
Pada suhu 60° C, natrium bikarbonat terurai menjadi natrium karbonat, karbon dioksida dan air (proses penguraian paling efektif pada 200° C):
2NaHCO 3 → Na 2 CO 3 + H 2 O + CO 2
Dengan pemanasan lebih lanjut hingga 1000° C (misalnya, saat memadamkan api dengan sistem bubuk), natrium karbonat yang dihasilkan terurai menjadi karbon dioksida dan natrium oksida:
Na 2 CO 3 → Na 2 O + CO 2 .
indikator fisika dan kimia
Natrium bikarbonat berupa bubuk kristal berwarna putih dengan ukuran kristal rata-rata 0,05 - 0,20 mm. Berat molekul senyawa adalah 84,01, massa jenisnya 2200 kg/m³, dan massa jenisnya 0,9 g/cm³. Panas pelarutan natrium bikarbonat diperkirakan 205 kJ (48,8 kkal) per 1 kg NaHCO 3, kapasitas panasnya mencapai 1,05 kJ/kg.K (0,249 kkal/kg.°C).
Natrium hidrogen karbonat tidak stabil secara termal dan, ketika dipanaskan, terurai menjadi natrium karbonat padat dan melepaskan karbon dioksida, serta air ke dalam fase gas:
2NaHCO 3 (padat) ↔ Na 2 CO 3 (padat) + CO 2 (g) + H 2 O (uap) - 126 kJ (- 30 kkal) Larutan natrium bikarbonat dalam air terurai dengan cara yang sama:
2NaHCO 3 (r.) ↔ Na 2 CO 3 (r.) + CO 2 (g.) + H 2 O (uap) - 20,6 kJ (- 4,9 kkal) Larutan natrium bikarbonat dalam air mempunyai sifat sedikit basa , dan oleh karena itu tidak berpengaruh pada jaringan hewan dan tumbuhan. Kelarutan natrium bikarbonat dalam air rendah dan sedikit meningkat dengan meningkatnya suhu: dari 6,87 g per 100 g air pada 0 °C menjadi 19,17 g per 100 g air pada 80 °C.
Karena kelarutannya yang rendah, massa jenis larutan natrium bikarbonat berair jenuh relatif sedikit berbeda dari massa jenis air murni.
Titik didih (terurai): 851°C;
Titik leleh: 270° C;
Massa jenis: 2,159 g/cm³;
Kelarutan dalam air, g/100 ml pada 20° C: 9.
Aplikasi
Natrium bikarbonat (bikarbonat) digunakan dalam industri kimia, makanan, cahaya, medis, farmasi, metalurgi non-ferrous, dan dipasok ke ritel.
Terdaftar sebagai bahan tambahan makanan E500.
Banyak digunakan di:
- industri kimia - untuk produksi pewarna, plastik busa dan produk organik lainnya, reagen fluorida, bahan kimia rumah tangga, pengisi alat pemadam kebakaran, untuk memisahkan karbon dioksida, hidrogen sulfida dari campuran gas (gas diserap dalam larutan bikarbonat pada tekanan tinggi dan rendah suhu, larutan dikembalikan ketika dipanaskan dan tekanan darah rendah).
- industri ringan - dalam produksi sol karet dan kulit buatan, penyamakan (penyamakan dan penetral kulit).
- industri tekstil (finishing kain sutra dan katun). Penggunaan natrium bikarbonat dalam produksi produk karet juga disebabkan oleh pelepasan CO 2 saat dipanaskan, yang membantu memberikan struktur berpori yang diperlukan pada karet.
- industri makanan - toko roti, produksi gula-gula, persiapan minuman.
- industri medis - untuk persiapan larutan injeksi, obat anti tuberkulosis dan antibiotik.
- metalurgi - selama pengendapan logam tanah jarang dan flotasi bijih.
Memasak
Kegunaan utama soda kue adalah untuk memasak, yang digunakan terutama sebagai bahan ragi utama atau tambahan dalam pembuatan kue (karena melepaskan karbon dioksida saat dipanaskan), dalam pembuatan produk kembang gula, dalam produksi minuman berkarbonasi dan air mineral buatan. , sendiri atau sebagai bagian dari bahan ragi kompleks ( misalnya, baking powder, dicampur dengan amonium karbonat), misalnya, dalam adonan biskuit dan roti pendek. Hal ini disebabkan kemudahan penguraiannya pada suhu 50-100° C.
Soda kue, digunakan terutama dalam pembuatan kue kecil, remah kue, lembaran kue, dan kue kering. Pada kuartal terakhir abad ke-19. Penggunaannya dalam gula-gula dimulai, awalnya hanya di Perancis dan Jerman, dan hanya pada akhir abad ke-19 dan awal abad ke-20 - juga di Rusia.
Penggunaan soda membuka jalan bagi produksi pabrik kue modern - kue bercap. Pada saat yang sama, banyak jenis kue lama - bolu, puff, hancur, roti jahe, kembung, meringue - telah menjadi sesuatu dari masa lalu, menghilang tidak hanya dari penggunaan umum, tetapi juga dari penggunaan di rumah.
Soda adalah asisten sehari-hari yang diperlukan di dapur untuk mencuci piring, wadah pengalengan, dan beberapa buah-buahan dan beri sebelum dikeringkan. Ia memiliki khasiat menetralisir dan membunuh bau.
Salah jika mengira soda hanya sebagai bumbu untuk kembang gula. Selain produksi gula-gula, soda juga digunakan untuk pembuatan selai jeruk Inggris, daging cincang untuk masakan Moldova, Rumania, dan Uzbekistan (soda kalium) dan dalam pembuatan minuman. Jumlah soda yang ditambahkan ke semua produk ini sangat kecil - mulai dari “di ujung pisau” hingga sejumput seperempat sendok teh. Dalam minuman dengan soda, porsinya jauh lebih tinggi - setengah sendok teh penuh per liter cairan. Untuk kembang gula dan keperluan lainnya, soda ditambahkan sesuai resep, biasanya dalam dosis yang sangat kecil. Simpan dalam wadah kedap udara dan bawa bersama benda kering.
Produksi soda secara industri telah memberikan peluang luas bagi penyiapan berbagai jenis produk kembang gula modern di negara-negara Eropa. Untuk waktu yang lama, Rusia mengikuti jalur tradisional, lebih memilih ragi dan jenis adonan lainnya.
Di Rusia, hingga paruh kedua abad ke-19, soda tidak digunakan sama sekali dalam pembuatan kue dan kembang gula. Dan pada akhir abad ke-19, produk semacam ini paling banyak diproduksi di Ukraina dan Polandia, serta di negara-negara Baltik. Penduduk Rusia, yang sejak dahulu kala terbiasa dengan jenis adonan alami - baik ragi, penghuni pertama, atau telur madu, di mana bahan kimia buatan tidak digunakan sebagai bahan pengangkat, tetapi gas yang dihasilkan secara alami selama pemanggangan digunakan sebagai hasil dari interaksi. produk seperti madu (gula), telur, krim asam, alkohol (vodka) atau cuka anggur - kue soda memiliki popularitas yang sangat rendah dan permintaan yang rendah.
Produk kembang gula yang dibuat dengan soda dianggap “Jerman” dan diabaikan baik karena alasan kuliner dan rasa maupun karena alasan “patriotik”.
Selain itu, produk kembang gula nasional Rusia - roti jahe dan roti jahe madu, mutiara berlapis kaca, dan kacang-kacangan yang direbus dalam madu - memiliki rasa yang sangat unik sehingga berhasil bersaing dengan produk Eropa Barat, bentuknya lebih halus, tetapi “tipis” dalam hal rasa kenyang dan kualitas yang baik dan rasa biskuit Perancis, dimana daya tariknya dicapai bukan karena sifat adonan yang istimewa, tetapi dengan penggunaan rempah-rempah yang eksotik, terutama vanila.
Selain kembang gula, soda tidak pernah digunakan dalam masakan Rusia dan sebenarnya tidak digunakan hingga saat ini. Sementara itu, di Baltik, Moldova, Rumania, dan Balkan, soda digunakan sebagai bahan ragi pada sejumlah masakan yang diolah dengan cara digoreng. Jadi, soda ditambahkan ke berbagai masakan goreng setengah adonan: panekuk kentang, yang juga mengandung tepung terigu; aneka pancake, roti pipih krim asam dan donat, kue keju yang terbuat dari kombinasi keju cottage dan tepung, serta daging cincang, jika hanya terdiri dari daging dan bawang bombay, tanpa menambahkan komponen tepung (tepung terigu, roti tawar, remah roti). Daging cincang mentah (daging sapi, babi) dibiarkan dengan bahan tambahan soda di lemari es selama beberapa jam, dan kemudian “sosis” mudah dibentuk dari daging cincang ini, yang dengan cepat (dalam 10-15 menit) dipanggang dalam oven. oven kompor rumah apa pun (gas, kayu atau listrik).
Penggunaan soda serupa dalam daging cincang juga dikenal dalam masakan Armenia, dengan satu-satunya perbedaan bahwa dalam kasus seperti itu daging cincang tidak didiamkan, tetapi segera dikocok secara intensif dengan penambahan beberapa tetes (5-8 ) cognac, dan sebenarnya berubah menjadi souffle daging yang digunakan untuk menyiapkan berbagai hidangan nasional (terutama kalolaks).
Di negara-negara berbahasa Inggris di Eropa dan Amerika (Inggris, Skotlandia, Pantai Timur Amerika Serikat dan Kanada), soda digunakan sebagai bahan tambahan yang sangat diperlukan dalam selai buah jeruk (jeruk, pampelmos, lemon, grapefruits), serta untuk persiapan manisan buah-buahan. Hasilnya, daya rebus khusus buah jeruk dan kulitnya yang keras tercapai, mengubah selai tersebut menjadi semacam selai jeruk yang kental, dan pada saat yang sama tingkat kepahitan tidak menyenangkan yang selalu ada pada kulit buah jeruk berkurang ( tapi tidak hilang sama sekali!). Kulit jeruk, yang bagi kita menjadi semacam pemberat, limbah dari memakan buah-buahan ini, dengan bantuan soda menjadi bahan baku yang berharga untuk menghasilkan selai jeruk yang harum dan bergizi tinggi.
Dalam masakan Asia Tengah, soda digunakan dalam pembuatan adonan sederhana jenis non-gula untuk memberikan elastisitas khusus dan mengubahnya menjadi adonan yang dapat diregangkan tanpa menggunakan minyak sayur, seperti yang biasa dilakukan di masakan Eropa Selatan, Mediterania, dan Balkan. . Di Asia Tengah, potongan adonan sederhana tidak beragi, setelah diistirahatkan selama setengah jam seperti biasanya, dibasahi dengan sedikit air yang kemudian dilarutkan 0,5 sendok teh garam dan 0,5 sendok teh soda, lalu diregangkan dengan tangan hingga menjadi yang paling tipis. mie (disebut mie Dungan), yang memiliki rasa yang lembut, enak dan digunakan untuk menyiapkan masakan nasional (lagman, monpara, shima, dll).
Soda, sebagai bahan tambahan kecil pada makanan apa pun selama proses memasak, dan khususnya selama perlakuan panas, ditambahkan di banyak masakan nasional, mengingat dalam beberapa kasus hal ini tidak hanya memberikan efek rasa yang tidak terduga, tetapi juga biasanya membersihkan bahan mentah makanan dan bahan-bahannya. seluruh hidangan dari berbagai bau dan rasa acak.
Secara umum, peran soda di dapur, bahkan di luar proses kuliner, sangatlah signifikan. Lagi pula, tanpa soda, praktis tidak mungkin untuk membersihkan enamel meja makan dan dapur, porselen, gelas dan gerabah, serta peralatan dan perlengkapan dapur dengan sempurna dari bau asing dan berbagai endapan dan patina. Soda sangat diperlukan dan diperlukan saat membersihkan peralatan teh - teko dan cangkir dari endapan teh dan lapisan tipis yang terbentuk di dindingnya.
Penggunaan soda juga diperlukan saat mencuci piring yang digunakan untuk memasak ikan untuk menghilangkan bau amis. Biasanya mereka melakukan hal berikut: bau amis yang membandel dihilangkan dengan menyeka piring dengan bawang bombay, kemudian bau bawang tersebut dihilangkan (dicuci) dengan membersihkan piring dengan soda.
Singkatnya, soda adalah komponen yang sangat diperlukan dalam produksi dapur, dan dapur yang baik tidak dapat hidup tanpanya. Terlebih lagi, ketidakhadirannya di gudang juru masak atau ibu rumah tangga segera terlihat, karena hal itu mengikat orang yang bekerja di kompor atau di meja potong dalam banyak tindakannya.
Keadaan lingkungan saat ini telah memunculkan penggunaan soda baru di dapur sebagai sarana untuk meningkatkan kualitas bahan baku nabati. Misalnya, Anda dapat merekomendasikan untuk mencuci semua sayuran yang sudah diproses tetapi belum dipotong - sebelum dimasukkan ke dalam kuali atau penggorengan - dalam larutan soda dalam air. Atau tambahkan satu atau dua sendok teh soda ke kentang yang sudah dikupas, diisi dengan air dingin dan dimaksudkan untuk direbus atau dihaluskan. Hal ini tidak hanya akan membersihkan kentang dari bahan kimia yang digunakan selama budidaya, tetapi juga akan membuat produk itu sendiri lebih ringan, lebih bersih, lebih indah, dan akan menghilangkan semua bau yang didapat selama transportasi atau penyimpanan yang tidak tepat, serta pembusukan. Setelah matang, kentangnya sendiri akan menjadi rapuh dan enak. Dengan demikian, penggunaan soda sebelum dimasak, pada saat pengolahan dingin (kemudian produk dicuci bersih dengan air dingin), dapat meningkatkan kualitas bahan baku pangan nabati, khususnya sayuran bertepung, umbi-umbian dan tanaman berdaun (kubis, selada, bayam). , peterseli, dll. .).
Soda telah menggantikan zat basa dengan sangat kuat sehingga tidak ada yang mampu menggesernya dari posisi ini. Soda kue dapat bertindak sebagai bahan ragi dalam dua cara. Pertama, ia terurai ketika dipanaskan menurut reaksi:
2NaHCO 3 (soda) → Na 2 CO 3 (garam) + H 2 O (air) + CO 2 (karbon dioksida).
Dan dalam hal ini, jika Anda menambahkan soda dalam jumlah berlebihan ke dalam adonan roti pendek, dalam waktu singkat adonan tersebut mungkin tidak memiliki waktu untuk terurai secara termal tanpa meninggalkan residu dan kue atau kue tersebut akan mendapatkan rasa “soda” yang tidak enak.
Sama seperti kalium, soda bereaksi dengan asam yang terkandung dalam adonan atau ditambahkan secara artifisial:
NaHCO 3 (soda) + R-COOH (asam) → R-COONa (garam) + H 2 O (air) + CO 2 (karbon dioksida)
Banyaknya tas bermerek yang berbeda dan ketersediaannya tidak menghilangkan kesenangan bagi para ahli kimia muda - membuat baking powder sendiri.
komposisi proporsional dari bedak tradisional tersebut:
2 bagian garam tartar asam,
1 bagian soda kue,
1 bagian pati atau tepung.
Obat
Semua orang tahu seperti apa soda itu - itu adalah bubuk putih yang menyerap air dan larut dengan baik di dalamnya. Namun hanya sedikit orang yang tahu tentang khasiat penyembuhan luar biasa dari zat “sederhana” ini. Sedangkan soda – natrium bikarbonat – merupakan salah satu bahan utama darah kita. Hasil penelitian tentang efek soda pada tubuh manusia melebihi semua ekspektasi. Ternyata soda mampu menyamakan keseimbangan asam basa dalam tubuh, memulihkan metabolisme sel, meningkatkan penyerapan oksigen oleh jaringan, dan juga mencegah hilangnya kalium vital. Soda kue membantu mengatasi mulas, mabuk laut, pilek, penyakit jantung dan sakit kepala, serta penyakit kulit. Seperti yang Anda lihat, soda adalah obat pertolongan pertama.
Larutan soda kue digunakan sebagai antiseptik lemah untuk berkumur, serta obat penetral asam tradisional untuk sakit maag dan sakit perut (pengobatan modern tidak merekomendasikan penggunaannya karena efek samping, termasuk “pantulan asam”) atau untuk menghilangkan asidosis, dll.
Soda kue digunakan untuk mengobati penyakit yang berhubungan dengan keasaman tinggi; larutan soda kue digunakan untuk berkumur dan mencuci kulit jika terkena asam.
Natrium bikarbonat (soda kue) dapat memperlambat perkembangan penyakit ginjal kronis. Kesimpulan ini dicapai oleh para ilmuwan dari Rumah Sakit Royal London, Inggris. Mereka mempelajari 134 orang dengan penyakit ginjal kronis stadium lanjut dan asidosis metabolik.
Satu kelompok subjek menerima pengobatan biasa, dan kelompok kedua, selain pengobatan tradisional, menerima sedikit soda kue setiap hari dalam bentuk tablet. Pada pasien yang meminum natrium bikarbonat, fungsi ginjal memburuk 2/3 lebih lambat dibandingkan pasien lain.
Perkembangan penyakit ginjal yang cepat diamati hanya pada 9% subjek percobaan dari “kelompok soda” dibandingkan 45% subjek yang diobati secara tradisional. Selain itu, mereka yang mengonsumsi soda memiliki kemungkinan lebih kecil terkena penyakit ginjal stadium akhir, yang memerlukan dialisis. Perlu dicatat bahwa peningkatan natrium bikarbonat dalam tubuh tidak menyebabkan peningkatan tekanan darah pada pasien.
Soda kue adalah pengobatan yang murah dan efektif untuk penyakit ginjal kronis. Namun, para peneliti mengingatkan: meminum soda harus di bawah pengawasan dokter, yang harus menghitung dosis pasien dengan benar.
Sifat penyembuhan soda kue
Sebelumnya, natrium bikarbonat digunakan secara luas (seperti alkali lainnya) sebagai antasida untuk keasaman tinggi jus lambung, tukak lambung dan duodenum. Ketika diminum, soda kue dengan cepat menetralkan asam klorida dari jus lambung dan memiliki efek antasida yang nyata. Namun, penggunaan soda tidak hanya tentang mencuci piring dengan cemerlang dan menghilangkan sakit maag. Soda kue menempati tempat yang tepat di lemari obat rumah.
Seperti orang Mesir kuno yang memperoleh soda alami dari air danau melalui penguapan, masyarakat juga memanfaatkan khasiat soda lainnya. Ini memiliki kualitas penetralan dan digunakan dalam praktik medis untuk mengobati gastritis dengan keasaman tinggi. Mampu membunuh kuman, digunakan sebagai desinfektan: soda digunakan untuk inhalasi, pembilasan, dan pembersihan kulit.
Soda juga banyak digunakan dalam perawatan kesehatan.
Pencegahan karies.
Asam yang terbentuk di mulut akibat aktivitas bakteri merusak email gigi. Asam ini dapat dinetralkan dengan berkumur dengan larutan soda kue beberapa kali sehari. Anda dapat melakukannya secara berbeda: basahi sikat gigi dengan air, celupkan ke dalam soda kue, dan gosok gigi. Selain itu, soda kue memiliki sedikit efek abrasif: akan memoles gigi tanpa merusak enamel.
Dari bau kaki yang tidak sedap.
Menambahkan soda ke air rendaman kaki akan menetralkan asam yang dihasilkan oleh bakteri, yang menyebabkan bau tidak sedap pada kaki. Baking soda juga akan membantu menghilangkan bau keringat ketiak yang menyengat.
Untuk gigitan serangga.
Jangan menggaruk bekas gigitan nyamuk dan pengisap darah lainnya hingga berdarah. Lebih baik menyiapkan campuran bubur air dan soda dan mengoleskannya ke tempat gigitan. Bubur soda juga akan menghilangkan rasa gatal akibat cacar air atau kontak kulit dengan hogweed dan jelatang.
Untuk ruam popok.
Lotion soda secara signifikan memperbaiki kondisi bayi yang mengalami ruam popok. Mereka mengurangi rasa gatal dan mempercepat penyembuhan kulit.
Untuk sistitis.
Bakteri patogen hidup di kandung kemih dalam lingkungan yang sedikit asam. Jika kandung kemih Anda terkena infeksi, minuman ideal setelah makan malam untuk Anda adalah campuran soda kue dan air bersoda.
Untuk sengatan matahari.
Tambahkan sedikit soda kue ke dalam bak mandi air hangat; ini akan melunakkan air, mengubahnya menjadi losion yang menenangkan untuk kulit yang teriritasi.
Untuk sakit tenggorokan.
Aduk 0,5 sdt. sendok makan soda dalam segelas air dan berkumur dengan larutan yang sudah disiapkan setiap 4 jam: ini menetralkan asam yang menyebabkan rasa sakit. Membilas mulut Anda dengan larutan ini akan membantu meredakan peradangan pada mukosa mulut.
Untuk bau mulut.
Jika dikombinasikan dengan hidrogen peroksida, soda kue memiliki efek oksidasi yang kuat dan menghancurkan bakteri penyebab bau mulut. Tambahkan 1 meja. sesendok soda kue ke dalam segelas larutan hidrogen peroksida (2-3%) dan bilas mulut Anda.
Untuk pilek.
Berguna untuk melakukan inhalasi. Untuk melakukan ini, Anda bisa mengambil ketel kecil dan merebus 1 gelas air di dalamnya dengan 1 sendok teh. sesendok soda. Buat tabung dari kertas keras, letakkan di cerat ketel dan hirup uapnya selama 10-15 menit. Menghirup ini sangat membantu dalam mengeluarkan lendir.
Untuk mengeluarkan dahak kental, minumlah 1/2 gelas air hangat saat perut kosong, yang dilarutkan 0,5 sendok teh, 2 kali sehari. sendok soda dan sedikit garam.
Untuk sering migrain.
Setiap hari, ambil larutan air matang dan soda kue. Pada hari pertama, 30 menit sebelum makan siang, minum 1 gelas larutan (0,5 sendok teh soda + air), hari ke-2 - 2 gelas, dst, sehingga menjadi 7 gelas. Kemudian kurangi dosisnya dengan urutan terbalik.
Lainnya.
Untuk rinitis, stomatitis, radang tenggorokan, konjungtivitis, gunakan larutan soda 0,5-2%.
Untuk mendisinfeksi mukosa mulut, ada gunanya berkumur dengan larutan lemah (soda - 85 g, garam - 85 g, urea - 2,5 g) setelah makan.
Obat merokok: bilas mulut Anda dengan larutan soda kue (1 sendok makan per 200 ml air).
Untuk kulit kering, dermatitis kering, iktiosis dan psoriasis, mandi obat bermanfaat (soda - 35 g, magnesium karbonat - 20 g, magnesium perborat - 15 g). Suhu air tidak boleh lebih tinggi dari 38-39° C, pertama Anda hanya perlu berendam air hangat, lalu naikkan suhunya secara bertahap. Durasi mandi adalah 15 menit.
Pemadam kebakaran
Natrium bikarbonat adalah bagian dari bubuk yang digunakan dalam sistem pemadam api bubuk, memanfaatkan panas dan menggantikan oksigen dari sumber pembakaran dengan karbon dioksida yang dilepaskan.
Pembersihan peralatan. Teknologi pembersihan ledakan abrasif (ABL)
Peralatan dan permukaan dibersihkan dari berbagai lapisan dan kontaminan menggunakan teknologi abrasive blast cleaning (ABL). Natrium bikarbonat (soda kue, natrium bikarbonat, natrium bikarbonat, NaHCO 3, natrium hidrogen karbonat) digunakan sebagai bahan abrasif.
Teknologi ASO yang menggunakan natrium bikarbonat adalah cara baru yang efektif untuk membersihkan peralatan menggunakan bahan abrasif “lembut”. Bahan abrasif digerakkan oleh udara terkompresi yang dihasilkan oleh kompresor. Metode ini telah diterima secara komersial dan telah digunakan secara luas di Eropa dan Amerika selama 25 tahun karena keserbagunaan dan kelayakan ekonominya.
Perawatan permukaan peralatan mirip dengan sandblasting konvensional. Bedanya, partikel soda merupakan bahan abrasif yang “lembut”, sehingga tidak merusak permukaan itu sendiri.
Prinsip:
Partikel rapuh natrium karbonat asam meledak saat bersentuhan dengan permukaan yang sedang dibersihkan.
Energi yang dilepaskan oleh lampu kilat ini menghilangkan kontaminan dari permukaan yang sedang dibersihkan. Partikel soda abrasif dipecah seluruhnya menjadi debu halus, yang mudah tersebar ke berbagai arah tegak lurus terhadap jatuhnya, sehingga meningkatkan efek pembersihan. Untuk tujuan menekan debu, pembersihan peralatan dengan ledakan soda biasanya dilakukan dengan menggunakan pelembab, yaitu pembersihan ledakan hidro-abrasive (HABL) pada peralatan. Natrium karbonat larut dalam air. Oleh karena itu, bahan abrasif bekas akan larut atau dapat dicuci setelah dibersihkan.
Ini berbeda dengan pasir kuarsa yang memotong lapisannya. Pasir kuarsa juga menghapus sebagian permukaan yang sedang dibersihkan, sehingga soda hampir tidak terluka. Masih banyak perbedaan antara jenis peralatan pembersih ini, tetapi hal tersebut merupakan konsekuensi dari sifat bahan abrasif.
Bahan abrasif natrium bikarbonat larut diformulasikan secara khusus untuk pembersihan peralatan dengan ledakan abrasif. Sifat abrasif yang mengalir bebas mengurangi kepadatan aliran yang terkait dengan buruknya fluiditas natrium karbonat konvensional.
- Mengisolasi kontur tetesan cairan dalam masalah menentukan tegangan permukaan Mengisolasi kontur tetesan
- Metode untuk memproduksi kalsium peroksida
- Warna Feo. Sifat kimia. Bubuk piroforik hitam tahan api, tidak larut dalam air. Metode untuk memperoleh zat besi
- Natrium tiosulfat Natrii tiosulfas (ln) Rumus kimia tiosulfat
- Metode rhodanida untuk menentukan zat besi
- Soda kue: formula, aplikasi
- Karbonat. Rumus soda kue. Soda kue: formula, aplikasi Keamanan soda kue bagi manusia
- Deskripsi penyakit, tanda, pengobatan
- Penyakit Liver: Penyebab, Jenis, Gejala dan Pencegahan Apa itu Virus di Liver
- Infestasi cacing: penyebab, gejala, pengobatan, pencegahan
- Obat tradisional
- Fermentasi makanan dan pentingnya
- Studi farmakokinetik dan bioavailabilitas - jurnal farmakokinetik dan farmakodinamik Kromatografi cair kinerja tinggi
- Uji kerja kloroform Kloroform di rumah
- Gas mulia dan sifat-sifatnya Gas mulia yang menyebabkan kelembaman gas-gas tersebut
- Spektroskopi Raman dan NIR Masalah spektrometri NIR dan cara penyelesaiannya
- Spesialisasi sampingan tantalum
- Apa itu tantalum dan di mana penggunaannya?
- Efek molekuler dari aksi enzim
- Displasia serviks: tanda pertama, gejala dan pengobatan