Warna Feo. Sifat kimia. Bubuk piroforik hitam tahan api, tidak larut dalam air. Metode untuk memperoleh zat besi
68. Senyawa besi
Besi (II) oksida FeO– zat kristal hitam, tidak larut dalam air dan basa. FeO cocok dengan dasarnya Fe(OH)2.
Kuitansi. Besi (II) oksida dapat diperoleh dengan reduksi tidak sempurna bijih besi magnetik dengan karbon (II) oksida:
Sifat kimia. Ini adalah oksida utama. Bereaksi dengan asam membentuk garam:
Besi (II) hidroksida Fe(OH)2- zat kristal putih.
Kuitansi. Besi (II) hidroksida diperoleh dari garam besi divalen melalui aksi larutan alkali:
Sifat kimia. Hidroksida dasar. Bereaksi dengan asam:
Di udara, Fe(OH)2 dioksidasi menjadi Fe(OH)3:
Besi(III) oksida Fe2O3– zat berwarna coklat, terdapat di alam dalam bentuk bijih besi merah, tidak larut dalam air.
Kuitansi. Saat menembakkan pirit:
Sifat kimia. Menunjukkan sifat amfoter yang lemah. Ketika berinteraksi dengan basa, ia membentuk garam:
Besi (III) hidroksida Fe(OH)3– zat berwarna merah kecoklatan, tidak larut dalam air dan alkali berlebih.
Kuitansi. Diperoleh melalui oksidasi besi (III) oksida dan besi (II) hidroksida.
Sifat kimia. Ini adalah senyawa amfoter (dengan dominasi sifat dasar). Endapan di bawah pengaruh alkali pada garam besi besi:
garam besi diperoleh dengan mereaksikan besi logam dengan asam yang sesuai. Mereka sangat terhidrolisis, itulah sebabnya larutan berairnya merupakan zat pereduksi yang energik:
Ketika dipanaskan di atas 480 °C, ia terurai, membentuk oksida:
Ketika basa bekerja pada besi (II) sulfat, besi (II) hidroksida terbentuk:
Membentuk kristal hidrat - FeSO4?7Н2О (besi sulfat). Besi (III) klorida FeCl3 – zat kristal berwarna coklat tua.
Sifat kimia. Mari larut dalam air. FeCl3 menunjukkan sifat pengoksidasi.
Agen pereduksi - magnesium, seng, hidrogen sulfida, teroksidasi tanpa pemanasan.
Tubuh manusia mengandung sekitar 5 g zat besi, sebagian besar (70%) merupakan bagian dari hemoglobin darah.
Properti fisik
Dalam keadaan bebas, besi merupakan logam berwarna putih keperakan dengan warna keabu-abuan. Besi murni bersifat ulet dan memiliki sifat feromagnetik. Dalam praktiknya, paduan besi - besi cor dan baja - biasanya digunakan.
Fe adalah unsur terpenting dan paling melimpah dari sembilan logam d subkelompok Golongan VIII. Bersama dengan kobalt dan nikel, ia membentuk “keluarga besi”.
Saat membentuk senyawa dengan unsur lain, sering kali menggunakan 2 atau 3 elektron (B = II, III).
Besi, seperti hampir semua unsur d pada golongan VIII, tidak menunjukkan valensi lebih tinggi yang sama dengan nomor golongannya. Valensi maksimumnya mencapai VI dan sangat jarang muncul.
Senyawa yang paling umum adalah senyawa yang atom Fe berada pada bilangan oksidasi +2 dan +3.
Metode untuk memperoleh zat besi
1. Besi teknis (paduan dengan karbon dan pengotor lainnya) diperoleh dengan reduksi karbotermik senyawa alaminya sesuai dengan skema berikut:

Pemulihan terjadi secara bertahap, dalam 3 tahap:
1) 3Fe 2 O 3 + CO = 2Fe 3 O 4 + CO 2
2) Fe 3 O 4 + CO = 3FeO + CO 2
3) FeO + CO = Fe + CO 2
Besi cor yang dihasilkan dari proses ini mengandung lebih dari 2% karbon. Selanjutnya, besi cor digunakan untuk memproduksi baja - paduan besi yang mengandung kurang dari 1,5% karbon.
2. Besi yang sangat murni diperoleh dengan salah satu cara berikut:
a) penguraian Fe pentakarbonil
Fe(CO) 5 = Fe + 5СО
b) reduksi FeO murni dengan hidrogen
FeO + H 2 = Fe + H 2 O
c) elektrolisis larutan garam Fe+2 dalam air
FeC 2 O 4 = Fe + 2CO 2
besi(II) oksalat
Sifat kimia
Fe adalah logam dengan aktivitas sedang dan menunjukkan sifat-sifat umum yang khas dari logam.
Fitur uniknya adalah kemampuannya untuk “berkarat” di udara lembab:
Dengan tidak adanya kelembapan dengan udara kering, besi mulai bereaksi secara nyata hanya pada T > 150°C; setelah kalsinasi, “kerak besi” Fe 3 O 4 terbentuk:
3Fe + 2O 2 = Fe 3 O 4
Besi tidak larut dalam air jika tidak ada oksigen. Pada suhu yang sangat tinggi, Fe bereaksi dengan uap air, menggantikan hidrogen dari molekul air:
3 Fe + 4H 2 O(g) = 4H 2
Mekanisme terjadinya karat adalah korosi elektrokimia. Produk karat disajikan dalam bentuk yang disederhanakan. Faktanya, lapisan lepas dari campuran oksida dan hidroksida dengan komposisi bervariasi terbentuk. Berbeda dengan film Al 2 O 3, lapisan ini tidak melindungi besi dari kerusakan lebih lanjut.
Jenis korosi

Melindungi besi dari korosi

1. Interaksi dengan halogen dan belerang pada suhu tinggi.
2Fe + 3Cl 2 = 2FeCl 3
2Fe + 3F 2 = 2FeF 3
Fe + Saya 2 = FeI 2
Senyawa terbentuk di mana jenis ikatan ionik mendominasi.
2. Interaksi dengan fosfor, karbon, silikon (besi tidak langsung bergabung dengan N2 dan H2, tetapi melarutkannya).
Fe + P = Fe x P y
Fe + C = Fe x C kamu
Fe + Si = Fe x Si y
Zat dengan komposisi variabel terbentuk, seperti bertollida (sifat ikatan kovalen mendominasi senyawa)
3. Interaksi dengan asam “non-pengoksidasi” (HCl, H 2 SO 4 dil.)
Fe 0 + 2H + → Fe 2+ + H 2
Karena Fe terletak pada deret aktivitas di sebelah kiri hidrogen (E° Fe/Fe 2+ = -0,44 V), ia mampu menggantikan H 2 dari asam biasa.
Fe + 2HCl = FeCl 2 + H 2
Fe + H 2 JADI 4 = FeSO 4 + H 2
4. Interaksi dengan asam “pengoksidasi” (HNO 3, H 2 SO 4 konsentrasi)
Fe 0 - 3e - → Fe 3+
Besi HNO 3 dan H 2 SO 4 yang pekat “mempasifkan” besi, sehingga pada suhu biasa logam tidak larut di dalamnya. Dengan pemanasan yang kuat, terjadi pelarutan yang lambat (tanpa pelepasan H 2).
Di bagian Besi HNO 3 larut, masuk ke dalam larutan dalam bentuk kation Fe 3+ dan anion asam direduksi menjadi NO*:
Fe + 4HNO 3 = Fe(NO 3) 3 + NO + 2H 2 O
Sangat larut dalam campuran HCl dan HNO 3
5. Kaitannya dengan basa
Fe tidak larut dalam larutan alkali berair. Bereaksi dengan alkali cair hanya pada suhu yang sangat tinggi.
6. Interaksi dengan garam dari logam yang kurang aktif
Fe + CuSO 4 = FeSO 4 + Cu
Fe 0 + Cu 2+ = Fe 2+ + Cu 0
7. Reaksi dengan gas karbon monoksida (t = 200°C, P)
Fe (bubuk) + 5CO (g) = Fe 0 (CO) 5 besi pentakarbonil
senyawa Fe(III).
Fe 2 O 3 - besi (III) oksida.
Bubuk merah-coklat, n. R. dalam H 2 O. Di alam - “bijih besi merah”.
Metode memperoleh:
1) penguraian besi (III) hidroksida
2Fe(OH) 3 = Fe 2 O 3 + 3H 2 O
2) penembakan pirit
4FeS 2 + 11O 2 = 8SO 2 + 2Fe 2 O 3
3) penguraian nitrat
Sifat kimia
Fe 2 O 3 adalah oksida basa dengan tanda-tanda amfoter.
I. Sifat utama diwujudkan dalam kemampuan bereaksi dengan asam:
Fe 2 O 3 + 6H + = 2Fe 3+ + ZH 2 O
Fe 2 O 3 + 6HCI = 2FeCI 3 + 3H 2 O
Fe 2 O 3 + 6HNO 3 = 2Fe(NO 3) 3 + 3H 2 O
II. Sifat asam lemah. Fe 2 O 3 tidak larut dalam larutan alkali berair, tetapi ketika menyatu dengan oksida padat, alkali dan karbonat, ferit terbentuk:
Fe 2 O 3 + CaO = Ca(FeO 2) 2
Fe 2 O 3 + 2NaOH = 2NaFeO 2 + H 2 O
Fe 2 O 3 + MgCO 3 = Mg(FeO 2) 2 + CO 2
AKU AKU AKU. Fe 2 O 3 - bahan baku untuk produksi besi dalam metalurgi:
Fe 2 O 3 + ZS = 2Fe + ZSO atau Fe 2 O 3 + ZSO = 2Fe + ZSO 2
Fe(OH) 3 - besi (III) hidroksida
Metode memperoleh:
Diperoleh melalui aksi basa pada garam Fe 3+ yang larut:
FeCl 3 + 3NaOH = Fe(OH) 3 + 3NaCl
Pada saat pembuatan, Fe(OH) 3 merupakan sedimen amorf lendir berwarna merah-coklat.
Fe(III) hidroksida juga terbentuk selama oksidasi Fe dan Fe(OH) 2 di udara lembab:
4Fe + 6H 2 O + 3O 2 = 4Fe(OH) 3
4Fe(OH) 2 + 2H 2 O + O 2 = 4Fe(OH) 3
Fe(III) hidroksida merupakan produk akhir hidrolisis garam Fe 3+.
Sifat kimia
Fe(OH) 3 adalah basa yang sangat lemah (jauh lebih lemah dari Fe(OH) 2). Menunjukkan sifat asam yang nyata. Jadi, Fe(OH) 3 mempunyai sifat amfoter:
1) reaksi dengan asam mudah terjadi:
2) endapan segar Fe(OH) 3 larut dalam konsentrasi panas. larutan KOH atau NaOH dengan pembentukan kompleks hidrokso:
Fe(OH)3 + 3KOH = K3
Dalam larutan basa, Fe(OH) 3 dapat dioksidasi menjadi ferrat (garam asam besi H 2 FeO 4 tidak dilepaskan dalam keadaan bebas):
2Fe(OH) 3 + 10KOH + 3Br 2 = 2K 2 FeO 4 + 6KBr + 8H 2 O
garam Fe 3+
Yang paling penting secara praktis adalah: Fe 2 (SO 4) 3, FeCl 3, Fe(NO 3) 3, Fe(SCN) 3, K 3 4 - garam darah kuning = Fe 4 3 Biru Prusia (endapan biru tua)
b) Fe 3+ + 3SCN - = Fe(SCN) 3 tiosianat Fe(III) (larutan berwarna merah darah)
Besi membentuk dua oksida, yang masing-masing menunjukkan valensi II dan III serta bilangan oksidasi (+2) dan (+3).
DEFINISI
Besi(II) oksida dalam kondisi normal, itu adalah bubuk hitam (Gbr. 1), terurai pada pemanasan sedang dan terbentuk kembali dari produk dekomposisi pada pemanasan lebih lanjut.
Setelah kalsinasi secara kimia tidak aktif. Piroforik dalam bentuk bubuk. Tidak bereaksi dengan air dingin. Menunjukkan sifat amfoter (dengan dominasi sifat dasar). Mudah teroksidasi oleh oksigen. Direduksi oleh hidrogen dan karbon.
Beras. 1. Besi (II) oksida. Penampilan.
DEFINISI
Ini adalah padatan berwarna merah-coklat dalam kasus modifikasi trigonal atau coklat tua dalam kasus modifikasi kubik, yang merupakan yang paling reaktif (Gbr. 1).
Stabil secara termal. Titik lebur 1562 o C.

Beras. 1. Besi (III) oksida.
Tidak bereaksi dengan air, amonia hidrat. Menunjukkan sifat amfoter, bereaksi dengan asam dan basa. Direduksi oleh hidrogen, karbon monoksida, besi.
Rumus kimia besi oksida
Rumus kimia besi (II) oksida adalah FeO, dan rumus kimia besi (III) oksida adalah Fe 2 O 3. Rumus kimia menunjukkan komposisi kualitatif dan kuantitatif suatu molekul (berapa banyak dan atom apa yang ada di dalamnya). Dengan menggunakan rumus kimia, Anda dapat menghitung massa molekul suatu zat (Ar(Fe) = 56 sma, Ar(O) = 16 sma):
Tuan(FeO) = Ar(Fe) + Ar(O);
Tuan(FeO) = 56 + 16 = 72.
Tuan(Fe 2 O 3) = 2×Ar(Fe) + 3×Ar(O);
Tuan(Fe 2 O 3) = 2×56 + 3×16 = 58 + 48 = 160.
Rumus struktur (grafis) oksida besi
Rumus struktur (grafis) suatu zat lebih visual. Ini menunjukkan bagaimana atom terhubung satu sama lain dalam suatu molekul. Di bawah ini adalah rumus grafik oksida besi (a - FeO, b - Fe 2 O 3):

Contoh pemecahan masalah
CONTOH 1
| Latihan | Setelah dilakukan analisa zat tersebut diketahui bahwa komposisinya meliputi: natrium dengan fraksi massa 0,4207 (atau 42,07%), fosfor dengan fraksi massa 0,189 (atau 18,91%), oksigen dengan fraksi massa 0,3902 (atau 39 . 02%). Temukan rumus senyawanya. |
| Larutan | Mari kita nyatakan jumlah atom natrium dalam molekul dengan “x”, jumlah atom fosfor dengan “y” dan jumlah atom oksigen dengan “z”. Mari kita cari massa atom relatif yang sesuai dari unsur natrium, fosfor, dan oksigen (nilai massa atom relatif yang diambil dari Tabel Periodik D.I. Mendeleev dibulatkan menjadi bilangan bulat). Ar(Na) = 23; Ar(P) = 31; Ar(O) = 16. Kami membagi persentase kandungan unsur menjadi massa atom relatif yang sesuai. Dengan demikian kita akan mencari hubungan antara jumlah atom dalam molekul senyawa: Na:P:O = 42.07/39: 18.91/31: 39.02/16; Na:P:O = 1,829: 0,61: 2,43. Mari kita ambil bilangan terkecil menjadi satu (yaitu membagi semua bilangan dengan bilangan terkecil 0,61): 1,829/0,61: 0,61/0,61: 2,43/0,61; Oleh karena itu, rumus paling sederhana untuk senyawa natrium, fosfor dan oksigen adalah Na 3 PO 4. Ini adalah natrium fosfat. |
| Menjawab | Na3PO4 |
CONTOH 2
| Latihan | Massa molar senyawa nitrogen-hidrogen adalah 32 g/mol. Tentukan rumus molekul suatu zat yang fraksi massa nitrogennya 85,7%. |
| Larutan | Fraksi massa unsur X dalam molekul dengan komposisi NX dihitung menggunakan rumus berikut: ω (X) = n × Ar (X) / M (HX) × 100%. Mari kita hitung fraksi massa hidrogen dalam senyawa: ω(H) = 100% - ω(N) = 100% - 85,7% = 14,3%. Mari kita nyatakan jumlah mol unsur-unsur yang termasuk dalam senyawa sebagai “x” (nitrogen), “y” (hidrogen). Maka rasio molarnya akan terlihat seperti ini (nilai massa atom relatif yang diambil dari Tabel Periodik D.I. Mendeleev dibulatkan menjadi bilangan bulat): x:y = ω(N)/Ar(N) : ω(H)/Ar(H); x:kamu= 85,7/14: 14,3/1; x:kamu= 6,12: 14,3= 1: 2. Artinya rumus paling sederhana untuk menggabungkan nitrogen dengan hidrogen adalah NH 2 dan massa molar 16 g/mol. Untuk mencari rumus sebenarnya suatu senyawa organik, kita mencari perbandingan massa molar yang dihasilkan: M zat / M(NH 2) = 32 / 16 = 2. Artinya indeks atom nitrogen dan hidrogen harus 2 kali lebih tinggi, yaitu. rumus zatnya adalah N 2 H 4. Ini adalah hidrazin. |
| Menjawab | N2H4 |
Oksida besi adalah senyawa besi dengan oksigen.
Yang paling terkenal adalah tiga oksida besi: oksida besi (II) - FeO, besi (III) oksida – Fe 2 O 3 dan besi (II, III) oksida – Fe 3 O 4.
Besi(II) oksida

Rumus kimia oksida besi adalah FeO . Koneksi ini berwarna hitam.
FeO Mudah bereaksi dengan asam klorida encer dan asam nitrat pekat.
FeO + 2HCl → FeCl 2 + H 2 O
FeO + 4HNO 3 → Fe(NO 3) 3 + NO 2 + 2H 2 O
Itu tidak bereaksi dengan air atau garam.
Ketika berinteraksi dengan hidrogen pada suhu 350 o C dan kokas pada suhu di atas 1000 o C, ia tereduksi menjadi besi murni.
FeO +H 2 → Fe + H 2 O
FeO +C → Fe + CO
Besi (II) oksida diperoleh dengan berbagai cara:
1. Akibat reaksi reduksi oksida besi dengan karbon monoksida.
Fe 2 O 3 + CO → 2 FeO + CO 2
2. Memanaskan setrika dengan tekanan oksigen rendah
2Fe + O 2 → 2 FeO
3. Menguraikan besi oksalat dalam ruang hampa
FeC 2 O 4 → FeO +CO + CO 2
4. Interaksi besi dengan besi oksida pada suhu 900-1000 o
Fe + Fe 2 O 3 → 3 FeO
Fe + Fe 3 O 4 → 4 FeO
Di alam, oksida besi ada sebagai mineral wustite.
Dalam industri digunakan dalam peleburan besi cor di tanur sembur, dalam proses penghitaman (kebiruan) baja. Hal ini ditemukan dalam pewarna dan keramik.
Besi(III) oksida

Rumus kimia Fe2O3 . Ini adalah senyawa besi besi dengan oksigen. Ini adalah bubuk merah-coklat. Hematit ditemukan di alam sebagai mineral.
Fe2O3 memiliki nama lain: oksida besi, timbal merah, crocus, pigmen merah 101, pewarna makananE172 .
Tidak bereaksi dengan air. Dapat berinteraksi dengan asam dan basa.
Fe 2 O 3 + 6HCl → 2 FeCl 3 + 3H 2 O
Fe 2 O 3 + 2NaOH → 2NaFeO 2 + H 2 O
Besi (III) oksida digunakan untuk pengecatan bahan bangunan: batu bata, semen, keramik, beton, paving slab, linoleum. Ini ditambahkan sebagai pewarna pada cat dan enamel, dan pada tinta cetak. Oksida besi digunakan sebagai katalis dalam produksi amonia. Dalam industri makanan dikenal sebagai E172.
Besi (II, III) oksida

Rumus kimia Fe3O4 . Rumus ini dapat ditulis dengan cara lain: FeO Fe 2 O 3.
Hal ini ditemukan di alam sebagai mineral magnetit, atau bijih besi magnetik. Ini adalah konduktor arus listrik yang baik dan memiliki sifat magnetik. Terbentuk ketika besi terbakar dan ketika uap super panas bekerja pada besi.
3Fe + 2 O 2 → Fe 3 O 4
3Fe + 4H 2 O → Fe 3 O 4 + 4H 2
Pemanasan pada suhu 1538 o C menyebabkan disintegrasi
2Fe 3 O 4 → 6FeO + O 2
Bereaksi dengan asam
Fe 3 O 4 + 8HCl → FeCl 2 + 2FeCl 3 + 4H 2 O
Fe 3 O 4 + 10HNO 3 → 3Fe(NO 3) 3 + NO 2 + 5H 2 O
Bereaksi dengan alkali pada fusi
Fe 3 O 4 + 14NaOH → Na 3 FeO 3 + 2Na 5 FeO 4 + 7H 2 O
Bereaksi dengan oksigen di udara
4 Fe 3 O 4 + O 2 → 6Fe 2 O 3
Reduksi terjadi melalui reaksi dengan hidrogen dan karbon monoksida
Fe 3 O 4 + 4H 2 → 3Fe + 4H 2 O
Fe 3 O 4 + 4CO → 3Fe +4CO 2
Nanopartikel magnetik oksida Fe 3 O 4 telah ditemukan aplikasinya dalam pencitraan resonansi magnetik. Mereka juga digunakan dalam produksi media magnetik. Besi oksida Fe 3 O 4 termasuk dalam cat yang diproduksi khusus untuk kapal perang, kapal selam dan peralatan lainnya. Elektroda dibuat dari magnetit yang menyatu untuk beberapa proses elektrokimia.
- Valerian selama kehamilan: indikasi, batasan dan petunjuk penggunaan Bisakah wanita hamil mengonsumsi tingtur valerian?
- Valerian selama kehamilan: dosis dan petunjuk penggunaan Tablet Valerian, petunjuk untuk ibu hamil
- Bolehkah minum infus valerian selama kehamilan dan menyusui?Apakah mungkin minum tablet valerian untuk ibu hamil?
- Histeria, neurosis histeris, reaksi konversi Gejala konversi merupakan ciri khas anak yang sakit
- Mengukur waktu reaksi remaja dan dewasa Apa itu reaksi manusia
- Gejala kesehatan mental yang tidak seimbang
- Keadaan mental stres Stres mental
- Sifat dasar dan ciri-ciri sensasi
- Siapa orang yang bertele-tele
- Fpi - Diagnostik psikologis
- Terdiri dari apakah materi putih otak?
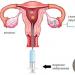
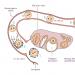
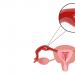
- Bagaimana cara mendeteksi kehamilan ektopik dan apa yang harus dilakukan?
- Pendarahan saat hamil
- Gejala kehamilan ektopik dan akibatnya
- Pinosol: fitur penggunaan pada wanita hamil Pinosol selama pengobatan kehamilan trimester ke-2
- Mlekoin untuk menyusui - petunjuk penggunaan, aplikasi, indikasi, kontraindikasi, tindakan, efek samping, analog, dosis, komposisi
- Apa yang harus dilakukan orang tua jika perut bayi baru lahirnya sakit?
- Semprotan Pinosol: instruksi
- Daun lingonberry selama kehamilan: semua pro dan kontra Berapa banyak minum daun lingonberry selama kehamilan
- Apa arti hijau?