Томуугийн вирүсийн репликаци нь онд тохиолддог. Томуугийн вирус хэрхэн ажилладаг вэ? RTG ашиглан томуугийн вирүсийг тодорхойлох
Эдгээр нь эсийн доторх үүрэг хариуцлагатай шимэгчид бөгөөд тусламжгүйгээр генээ хуулбарлаж, дамжуулж чадахгүй гэсэн үг юм. Ганц вирусын тоосонцор (вирион) нь өөрөө идэвхгүй байдаг. Вирус эсэд халдварлахдаа фермент болон эсийн бүтцийн ихэнх хэсгийг хуулбарлахын тулд ашигладаг.
Бид эсийг хуваах үйл явцаас ялгаатай нь вирусын нөхөн үржихүй нь эзэн эсийг устгаж, улмаар биеийн бусад эсүүдэд халдварладаг олон үр удам үүсгэдэг.
Вирусын генетик материал
Вирус нь нэг хэлхээтэй/хоёр судалтай ДНХ эсвэл РНХ агуулж болно. Тухайн вирусын доторх генетикийн материалын төрөл нь түүний шинж чанар, үйл ажиллагаанаас хамаардаг. Хост халдвар авсны дараа яг юу болох нь вирусын шинж чанараас хамаарч өөр өөр байдаг.
dsDNA, ssDNA, dsRNA болон нэг хэлхээтэй РНХ вирусын хувьд хуулбарлах процесс өөр байх болно. Жишээлбэл, хоёр хэлхээтэй ДНХ-ийн вирусууд хуулбарлахын өмнө ихэвчлэн эзэн эсэд нэвтрэх ёстой. Гэсэн хэдий ч нэг судалтай РНХ-ийн вирүс нь үндсэн эсүүд рүү үрждэг.
Вирус нь эзэнд халдсаны дараа вирусын үр удамын бүрэлдэхүүн хэсгүүдийг эсийн механизмаар үүсгэдэг бөгөөд вирусын капсидыг угсрах нь ферментийн бус процесс юм. Вирус нь ихэвчлэн зөвхөн цөөн тооны хостуудыг халдварладаг. "Цоож ба түлхүүр" механизм нь энэ үзэгдлийн хамгийн түгээмэл тайлбар юм. Вирусын тоосонцор дээрх тодорхой уураг нь тухайн эзний эсийн гадаргуу дээрх тодорхой рецепторын уурагтай таарч байх ёстой.
Вирусууд эсийг хэрхэн халдварладаг вэ?
Вирусын халдвар, хуулбарлах үндсэн үйл явц нь 6 үе шаттайгаар явагддаг.
- Адсорбци - вирус нь эзэн эстэй холбогддог.
- Нэвтрэх - вирус нь геномоо эзэн эсэд нэвтрүүлдэг.
- Вирусын геномын хуулбар - Вирусын геномыг эзэн эсийн бүтцийг ашиглан хуулбарладаг.
- Ассемблей - вирусын бүрэлдэхүүн хэсгүүд, ферментүүд үүсч, угсарч эхэлдэг.
- Боловсруулалт - угсарсан бүрэлдэхүүн хэсгүүдээс вирус үүсдэг.
- Гарах - халдвар авах шинэ хохирогчдыг хайж шинэ вирусууд эзэн эсээс гарч ирдэг.
Вирус нь ямар ч төрлийн эсийг халдварладаг
Ортомиксовирусын гэр бүлд (Грекээр orthos - зөв, туха - салиа) томуугийн A, B, C төрлийн вирусууд багтдаг бөгөөд тэдгээр нь парамиксовирусын нэгэн адил муцинтай холбоотой байдаг. Томуугийн А вирүс нь хүн болон зарим төрлийн амьтан (морь, гахай гэх мэт), шувуунд халдварладаг. Томуугийн В, С төрлийн вирүс нь зөвхөн хүний хувьд эмгэг төрүүлэгч байдаг. Хүний томуугийн анхны вирүсийг 1933 онд В.Смит, К.Эндрюс, П.Ладов (WS омог) нар цагаан гарамыг халдварлах замаар хүнээс ялгаж авчээ. Дараа нь энэ вирүсийг А хэлбэрийн ангилалд оруулсан.1940 онд Т.Франсис, Т.Мегилл нар томуугийн В хэлбэрийн вирүсийг, 1949 онд Р.Тэйлор томуугийн С хэлбэрийн вирусыг илрүүлсэн.Томуугийн вирүсийг ангилахдаа тодорхой хүндрэлүүд байнга гардаг. тулгарсан нь тэдний эсрэгтөрөгчийн хэлбэлзэлтэй холбоотой. Томуугийн вирүсийг А, В, С гэсэн гурван төрөлд хуваадаг. А төрөл нь эсрэгтөрөгчөөрөө бие биенээсээ ялгаатай хэд хэдэн дэд хэв шинжийг агуулдаг - гемагглютинин ба нейраминидаз. ДЭМБ-ын ангиллын дагуу (1980) хүн ба амьтны томуугийн А хэлбэрийн вирүсийг гемагглютинин (H1-H13) дээр үндэслэн 13, нейраминидаза (N1-N10) дээр үндэслэн 10 эсрэгтөрөгчийн дэд төрөлд хуваадаг. Эдгээрээс хүний томуугийн А хэлбэрийн вирүст гурван гемагглютинин (HI, H2 ба NZ) ба хоёр нейраминидаз (N1 ба N2) багтана.А хэлбэрийн вирүсийн хувьд гемагглютинин ба нейраминидазын дэд төрлийг хаалтанд зааж өгсөн болно. Тухайлбал, томуугийн А вирүс: Хабаровск/90/77 (H1N1).Бүтэц ба химийн найрлага
Томуугийн вирүс нь бөмбөрцөг хэлбэртэй, 80-120 нм диаметртэй. Thread шиг хэлбэрүүд нь бага түгээмэл байдаг. Мушгиа тэгш хэмийн нуклеокапсид нь вирионын цөмийг бүрдүүлдэг давхар мушгиа хэлбэрээр байрладаг рибонуклеопротейн (RNP) хэлхээ юм. РНХ полимераз ба эндонуклеазууд (P1 ба P3) үүнтэй холбоотой байдаг. Цөм нь М уургаас бүрдэх мембранаар хүрээлэгдсэн бөгөөд энэ нь RNP-ийг гадна бүрхүүлийн липидийн давхар давхарга, гемагглютинин, нейраминидазаас бүрдэх стилоид процессуудтай холбодог.Вирионууд нь РНХ-ийн 1%, уураг 70%, липидүүдийн 24%, 5. нүүрс ус %. Липид ба нүүрс ус нь гаднах бүрхүүлийн липопротейн ба гликопротеины нэг хэсэг бөгөөд эсийн гаралтай байдаг. Вирусын геном нь хасах хэлхээтэй хуваагдсан РНХ молекулаар илэрхийлэгддэг. Томуугийн А ба В төрлийн вирүс нь РНХ-ийн 8 фрагменттэй.Үүний 5 нь нэг уураг, сүүлийн 3 нь тус бүр хоёр уураг кодлодог.Антигенууд
Томуугийн A, B, C вирүсүүд нь RNP (NP уураг) болон вирионы бүтцийг тогтворжуулдаг M-матрицын уурагтай холбоотой төрлийн өвөрмөц эсрэгтөрөгчөөрөө ялгаатай байдаг.Эдгээр эсрэгтөрөгчийг RSC-д илрүүлдэг. А хэлбэрийн вирусын илүү нарийссан өвөрмөц байдлыг гадаргуугийн хоёр эсрэгтөрөгч - гемагглютинин H ба нейраминидаза N, серийн дугаараар тодорхойлдог.Гемаглютинин нь хамгаалалтын шинж чанартай цогц гликопротейн юм. Энэ нь бие махбодид вирусыг саармагжуулах эсрэгбие үүсэхийг өдөөдөг - RTGA-д илэрсэн антигемагглютининууд. Гемагглютинин (H-эсрэгтөрөгч)-ийн хэлбэлзэл нь томуугийн вирүсийн эсрэгтөрөгчийн шилжилт, шилжилтийг тодорхойлдог. Антигенийн шилжилт гэдэг нь түүний үүсэхийг хянадаг генийн цэгийн мутациас үүдэлтэй Н-эсрэгтөрөгчийн бага зэргийн өөрчлөлтийг хэлнэ. Ийм өөрчлөлт нь эсрэгбие гэх мэт сонгомол хүчин зүйлийн нөлөөн дор үр удамд хуримтлагдаж болно. Энэ нь эцсийн дүндээ гемагглютинины эсрэгтөрөгчийн шинж чанарын өөрчлөлтөөр илэрхийлэгддэг тоон өөрчлөлтөд хүргэдэг. Антигений шилжилтийн үед генийг бүрэн орлуулах бөгөөд энэ нь хоёр вирусын хоорондох рекомбинац дээр үндэслэсэн байж болно. Энэ нь гемагглютинин эсвэл нейраминидазын дэд төрөл, заримдаа эсрэгтөрөгч хоёулаа өөрчлөгдөж, вирусын эсрэгтөрөгчийн үндсэн хувилбарууд гарч ирж, томоохон тахал, тахал үүсгэдэг.Гемагглютинин нь мөн мэдрэмтгий эсүүдэд вирус шингэдэг рецептор юм. , түүний дотор эритроцитууд хоорондоо наалддаг бөгөөд цусны улаан эсийн цус задралд оролцдог.Вирусын нейраминидаз нь субстратаас сиалийн хүчлийг задлах фермент юм. Энэ нь эсрэгтөрөгчийн шинж чанартай бөгөөд нэгэн зэрэг хост эсээс вирионыг ялгаруулахад оролцдог. Нейраминидаз нь гемагглютинин шиг эсрэгтөрөгчийн шилжилт, шилжилтийн үр дүнд өөрчлөгддөг.Тариалалт, нөхөн үржихүй
Томуугийн вирүсийг тахианы үр хөврөл болон эсийн өсгөвөрт тариалдаг. Хамгийн оновчтой орчин бол тахианы үр хөврөл ба амнион ба аллантосын хөндийд вирус нь 36-48 цагийн дотор үрждэг.Томуугийн вирүст хамгийн мэдрэмтгий нь хүний үр хөврөлийн бөөрний эсийн анхдагч өсгөвөр болон зарим амьтдын өсгөвөр юм. Эдгээр өсгөвөрт вирусын нөхөн үржихүй нь аяндаа эсийн доройтлыг санагдуулам зөөлөн CPE дагалддаг. Томуугийн вирүс нь эпителийн эсийн гликопротейн рецепторуудад шингэж, рецепторын эндоцитозоор дамжин нэвтэрдэг. Вирусын геномын транскрипци ба хуулбарлах нь эсийн цөмд тохиолддог. Энэ тохиолдолд уншсан бие даасан РНХ-ийн фрагментүүд м-РНХ хэлбэрээр рибосом руу хөрвүүлэгдэж, вирусын өвөрмөц уургийн нийлэгжилт явагддаг. Вирусын геномыг хуулбарласны дараа вирусын РНХ-ийн сан үүсдэг бөгөөд энэ нь шинэ нуклеокапсидын угсралтад ашиглагддаг.Эмгэг төрүүлэх
Вирусын анхдагч нөхөн үржихүй нь амьсгалын замын эпителийн эсүүдэд тохиолддог. Салст бүрхүүлийн элэгдэлд орсон гадаргуугаар дамжин вирус нь цусанд нэвтэрч, вирусеми үүсгэдэг. Цусан дахь вирусын эргэлт нь цусны хялгасан судасны эндотелийн эсийг гэмтээж, улмаар тэдгээрийн нэвчилтийг нэмэгдүүлдэг. Хүнд тохиолдолд уушиг, зүрхний булчин болон бусад дотоод эрхтнүүдэд цус алдалт ажиглагддаг. Томуугийн вирүс нь тунгалгийн булчирхайд нэвтэрч, лимфоцитыг гэмтээж, улмаар дархлалын олдмол хомсдолд хүргэдэг бөгөөд энэ нь хоёрдогч бактерийн халдвар үүсэхэд хувь нэмэр оруулдаг.Томуугийн үед бие махбодид янз бүрийн зэргийн хордлого үүсдэг.Дархлаа
Томуугийн эсрэг дархлааны механизм нь вирусын эсрэг өвөрмөц бус хамгаалалтын байгалийн хүчин зүйлүүд, голчлон интерферон ба байгалийн алуурчин эсийн үйлдвэрлэлтэй холбоотой байдаг.Өвөрмөц дархлаа нь эсийн болон хомораль хариу урвалын хүчин зүйлүүдээр хангагдана. Эхнийх нь макрофаг ба Т-алуурчидаар төлөөлдөг. Хоёр дахь нь вирусыг саармагжуулах шинж чанартай иммуноглобулинууд, үндсэндээ антигемагглютинин ба антинейроминидазын эсрэгбие юм. Сүүлийнх нь антигемагглютининаас ялгаатай нь томуугийн вирүсийг зөвхөн хэсэгчлэн саармагжуулж, тархахаас сэргийлдэг. Вирусын нуклеопротеины эсрэгбиемийг нөхөх эсрэгбие нь 1.5 сарын дараа ч гэсэн хамгаалалтын шинж чанартай байдаггүй. эдгэрсэн хүмүүсийн цуснаас алга болно.Өвчин эхэлснээс хойш 3-4 хоногийн дараа цусны ийлдсэнд эсрэгбие илэрч, 2-3 долоо хоногийн дараа хамгийн их титрт хүрдэг. Томуугийн халдварын дараа олж авсан өвөрмөц дархлааны үргэлжлэх хугацаа нь өмнөх итгэл үнэмшлээс ялгаатай нь хэдэн арван жилээр хэмжигддэг. 1977 онд А (H1N1) вирүсээр үүсгэгдсэн томуугийн өвчлөлийн насны бүтцийг судалсны үндсэн дээр ийм дүгнэлтэд хүрсэн бөгөөд 1957 оноос хойш гараагүй байсан энэ вирус нь зөвхөн 20-иос доош насныхан өвчилдөг болох нь тогтоогджээ. 1977 онд А хэлбэрийн томуугийн вирүсээр үүсгэгдсэн томуугийн халдвар авсаны дараа түүний үүсэх шалтгаан болсон вирүсийн дэд төрөлд (H ба N-эсрэгтөрөгчөөр) онцгой хүчтэй дархлаа үүсдэг. Харгалзах вирүсийн дэд хэвшинжийн IgG эсрэгбиемүүдээс үүдэлтэй идэвхгүй дархлаа. Дархлаа нь 6-8 сар үргэлжилнэ.Эпидемиологи
Халдварын эх үүсвэр нь өвчтэй хүмүүс, вирус тээгч юм. Өвчин үүсгэгчийг дамжуулах нь агаар дуслын замаар дамждаг. Томуу бол өвөл, өвөл-хаврын улиралд илүү их тохиолддог тархалтын халдвар юм. Ойролцоогоор арван жил тутамд томуугийн тахал тахал болж, янз бүрийн тивийн хүн амд нөлөөлдөг. Энэ нь эсрэгтөрөгчийн шилжилт, шилжилттэй холбоотой А төрлийн вирүсийн H ба N-антигенүүдийн өөрчлөлтөөр тайлбарлагддаг. Тухайлбал, гемагглютинин NSW1 бүхий томуугийн А вирус нь 1918 онд 20 сая хүний амийг авч одсон Испани томууны тахал өвчнийг үүсгэсэн. 1957 онд "Азийн" томуугийн вирүс (H2N2) нь 2 тэрбум гаруй хүнийг хамарсан тахал өвчин үүсгэсэн. 1968 онд томуугийн А (H3N2) вирүс хэмээх тахлын шинэ хувилбар гарч ирсэн бөгөөд энэ нь Хонконгийн вирус гэж нэрлэгддэг бөгөөд өнөөг хүртэл тархсаар байна. 1977 онд А хэлбэрийн вирус (H1N1) нэгдэж, 1947-1957 онд ижил төрлийн вирус тархаж, улмаар "Азийн" дэд төрлөөр бүрэн солигдсон тул энэ нь гэнэтийн байсан юм. Үүнтэй холбогдуулан вирусын шилжилтийн хувилбарууд түүхэн шинэ зүйл биш гэсэн таамаглал гарч ирэв. Эдгээр нь өнгөрсөн жилүүдэд эргэлдэж байсан сероз дэд хэв маягийг төлөөлдөг.Дараагийн тахал үүсгэсэн томуугийн вирүсийн эргэлт зогссон нь эмгэг төрүүлэгчийн энэхүү эсрэгтөрөгчийн хувилбарт бий болсон хүн амын хамтын дархлаатай холбоотой юм. Үүний цаана хамтын дархлаа нь бүрдээгүй байгаа шинэ антигений хувилбаруудын сонголт гарч ирж байна.Идэвхтэй эргэлтээс гарсан томуугийн А вирүсийн эсрэгтөрөгчийн хувилбарууд (серо дэд төрөл) хаана шилжиж байгаа нь одоогоор тодорхойгүй байна. өөр нэг түүхэн үе нь удаан хугацаанд хадгалагдан үлджээ. Ийм вирүсийн оршин тогтнох нөөц нь томуугийн А хэлбэрийн вирүсийн хүний төрөл зүйлээр өвчилсөн зэрлэг болон гэрийн тэжээвэр амьтад, ялангуяа шувууд байж болох ба эргэлтийг удаан хугацаанд хадгалж байдаг. Үүний зэрэгцээ шувууны бие махбодид шувууны болон хүний вирүсийн генетикийн рекомбинаци үүсдэг бөгөөд энэ нь эсрэгтөрөгчийн шинэ хувилбарууд үүсэхэд хүргэдэг.Өөр нэг таамаглалаар бол мэдэгдэж буй бүх дэд хэвшинжийн томуугийн вирүс хүн амын дунд байнга эргэлддэг боловч тархалтын хувьд хамааралтай болдог. зөвхөн хамтын дархлаа буурснаар томуугийн В, С хэлбэрийн вирүс нь эсрэгтөрөгчийн тогтвортой байдал өндөртэй байдаг. Томуугийн В вирүс нь бага эрчимтэй тархалт, орон нутгийн дэгдэлт үүсгэдэг. Томуугийн С төрлийн вирүс нь үе үе өвчлөх шалтгаан болдог.Томуугийн вирүс нь 56°С-аас дээш температур, хэт ягаан туяа, ариутгагч бодис, угаалгын нунтаг зэрэгт хурдан устдаг. Энэ нь 1 өдрийн турш амьдрах чадвартай хэвээр байна. өрөөний температурт, гөлгөр металл болон хуванцар гадаргуу дээр - 2 хүртэл хоног. Томуугийн вирүс бага температурт (-70 ° C) амьдардаг.Тусгай урьдчилан сэргийлэх
Томуунаас урьдчилан сэргийлэхийн тулд томуугийн А хэлбэрийн вирүсийн үржлийг дарангуйлдаг римантадиныг хэрэглэдэг. Идэвхгүй урьдчилан сэргийлэх зорилгоор томуугийн эсрэг вакцинаар дархлаажуулсан донорын цусны ийлдэсээс гаргаж авсан хүний томуугийн эсрэг иммуноглобулиныг хэрэглэдэг. Хүний лейкоцитын интерферон тодорхой нөлөө үзүүлдэг.Вакцинаас урьдчилан сэргийлэхийн тулд амьд болон идэвхгүйжүүлсэн вакциныг хэрэглэдэг. Амьд вакцин хийлгэх үед ерөнхий болон орон нутгийн дархлаа үүсдэг. Үүнээс гадна интерфероны индукцийг тэмдэглэж байна.Одоогоор янз бүрийн төрлийн идэвхгүйжүүлсэн вакциныг олж авсан: вирион, дэд нэгж, хуваагдмал, холимог. Вирионы вакциныг тахианы үр хөврөлд ургасан вирусыг өндөр чанартай цэвэршүүлэх замаар үйлдвэрлэдэг. Дэд бүлгийн вакцинууд нь томуугийн вирүсийн цэвэршүүлсэн гадаргуугийн эсрэгтөрөгч - гемагглютинин ба нейраминидаз юм. Ийм вакцины бэлдмэлүүд нь реактоген чанар багасч, дархлаа өндөртэй байдаг. Хагарсан эсвэл задарсан вакциныг угаалгын нунтагаар боловсруулж, цэвэршүүлсэн вирион суспензээс бэлтгэдэг. Гэсэн хэдий ч эдгээр вакцинуудын аль нэгнийх нь давуу байдлын талаар зөвшилцөлд хүрээгүй байна. Идэвхгүйжүүлсэн вакцинууд нь ерөнхий болон орон нутгийн шингэний дархлааны тогтолцоонд дархлааны хариу урвал үүсгэдэг боловч амьд вакцинтай харьцуулахад интерфероны нийлэгжилтийг бага хэмжээгээр өдөөдөг.Амьд болон идэвхгүйжүүлсэн вакциныг олон жилийн турш хэрэглэсэн туршлагаас үзэхэд вакцины омгуудын эсрэгтөрөгчийн үл нийцэл нь вакцины омгийн эсрэгтөрөгчтэй нийцэхгүй байгааг харуулж байна. Томуугийн эсрэг вакцинаас урьдчилан сэргийлэх үр дүн бага байгаа нь гол боловч цорын ганц шалтгаан биш юм. Сүүлийн жилүүдэд томуугийн эсрэг генийн инженерчлэлийн болон синтетик вакцин бүтээх оролдлого хийгдэж байна.Ханиад томуу
Томуу нь хүний амьсгалын замын цочмог өвчин бөгөөд тархах хандлагатай байдаг. Энэ нь амьсгалын дээд замын катрин үрэвсэл, халууралт, хүнд хэлбэрийн ерөнхий хордлого зэргээр тодорхойлогддог. Томуу нь ихэвчлэн хүнд хэлбэрийн хүндрэлүүд дагалддаг - хоёрдогч бактерийн уушигны үрэвсэл, уушгины архаг өвчний хурцадмал байдал Томуугийн эмгэг төрүүлэгчид нь Orthomyxoviridae гэр бүлд хамаардаг. Үүнд гурван төрлийн вирус багтдаг - A, B, C. Томуугийн вирүс нь бөмбөрцөг хэлбэртэй, хэмжээ нь 80-120 нм. Заримдаа судалтай вирионууд үүсдэг. Геном нь нэг судалтай хасах РНХ-ээр үүсгэгддэг бөгөөд энэ нь найман хэлтэрхийгээс бүрдэх ба уургийн капсидаар хүрээлэгдсэн байдаг. 4 дотоод уурагтай холбоотой РНХ: нуклеопротейн (NP) ба өндөр молекул жинтэй уургууд PI, P2, R3, геномын транскрипц болон вирусын хуулбарлахад оролцдог. Нуклеокапсид нь мушгиа хэлбэрийн тэгш хэмтэй байдаг. Капсидын бүрхүүлийн дээр матрицын уургийн давхарга (M уураг) байдаг. Гаднах, суперкапсид бүрхүүл, гемагглютинин (H) ба нейраминидаза (N) нь нуруу хэлбэрээр байрладаг. Гликопротейн (N ба H) хоёулаа эсрэгтөрөгчийн шинж чанартай байдаг. Томуугийн вирүсийн хувьд 13 төрлийн гемагглютинин (NI-13), нейраминидазын 10 хувилбар (N1-10) илэрсэн байна.Дотоод нуклеопротейн эсрэгтөрөгч дээр үндэслэн томуугийн гурван төрлийн вирүсийг ялгадаг - A, B, C. RSC-д тодорхойлж болно. Хүнд халдварладаг А хэлбэрийн вирус нь гурван төрлийн гемагглютинин (HI, H2, H3) ба хоёр нейраминидаз (N1, N2) агуулдаг. Тэдний хослолоос хамааран томуугийн А вирүсийн хувилбаруудыг ялгадаг - H1N1, H2N2, H3N2. тэдгээр нь зохих ийлдэс бүхий гемагглютинацийг дарангуйлах урвалаар тодорхойлогддог.Томуугийн вирүсийг тахианы үр хөврөл болон янз бүрийн эсийн өсгөвөрт амархан тариалдаг. Вирусын хамгийн их хуримтлал 2-3 хоногийн дараа тохиолддог. Гадны орчинд вирус нь хатаах замаар халдвар авах чадвараа хурдан алддаг. Хөргөгчинд бага температурт долоо хоног, -70 хэмд илүү удаан хадгалагдана. Халаалт нь хэдхэн минутын дараа идэвхгүй болоход хүргэдэг. Эфир, фенол, формальдегидийн нөлөөн дор хурдан устдаг.Вирус судлалын оношлогооны арга
Судалгааны материал нь хамрын хөндийн арчдас, хамрын шүүрэл, өвчний эхний өдрүүдэд хуурай эсвэл нойтон ариутгасан хөвөн арчдас, цэрээр авдаг. Вирусыг цус, тархи нугасны шингэнээс олж болно. Нас барсан тохиолдолд амьсгалын дээд ба доод зам, тархи гэх мэт нөлөөлөлд өртсөн эдүүдийн хэсгүүдийг арилгадаг.Хоосон ходоодонд хамар залгиурын арчдас авдаг. Өвчтөн ариутгасан өргөн хүзүүтэй саванд цуглуулсан давсны натрийн хлоридын ариутгасан уусмалаар (10-15 мл) гурван удаа зайлж угаана. Үүний дараа залгиурын арын хана, хамрын хэсгүүдийг ариутгасан хөвөн ноосоор арчиж, дараа нь саванд хийж зайлж угаана.Та материалыг натрийн хлоридын уусмалд чийгшүүлсэн ариутгасан арчдасаар авч болно. залгиурын арын ханыг сайтар арчина. Материалыг цуглуулсны дараа арчдасыг физиологийн уусмал бүхий туршилтын хоолойд дүрж, 5% идэвхгүйжүүлсэн амьтны ийлдэс нэмнэ. Лабораторид арчдасыг шингэнээр зайлж, хоолойны хажуу талд шахаж, арилгадаг. Ус зайлуулах хоолойг хөргөгчинд байрлуулж, шингэний дунд хэсгийг ариутгасан хоолойд цуглуулдаг. Антибиотик пенициллин (200-1000 IU/мл), стрептомицин (200-500 мкг/мл), нистатин (100-1000 IU/ml) зэргийг дагалдах микрофлорыг устгах материалд нэмж, тасалгааны температурт 30 минут байлгаж, вирусыг тусгаарлах.урьд нь үргүйдэлтэй эсэхийг нь шалгасан.10-11 хоногтой тахианы үр хөврөлд халдварладаг вирүсийг тусгаарлах эмзэг арга. 0.1-0.2 мл эзэлхүүнтэй материалыг амнион эсвэл аллантоисын хөндийд тарьдаг. Дүрмээр бол 3-5 үр хөврөл халдвар авсан байдаг. Үр хөврөлийг 33-34 хэмийн оновчтой температурт 72 цагийн турш өсгөвөрлөнө. Туршилтын материал дахь вирионуудын тоог нэмэгдүүлэхийн тулд үүнийг урьдчилан төвлөрүүлдэг. Үүний тулд тахианы цусны улаан эсэд вирус шингээх, вирусын халдварт шинж чанарыг сайжруулахын тулд 0.2% трипсиний уусмалаар эмчлэх, эсвэл тусгай аргаар тунадасжуулах арга хэрэглэдэг.Инкубацийн дараа тахианы үр хөврөлийг хөргөнө. 2-4 цагийн турш 4 хэмийн температурт байлгана, дараа нь пипеткээр эсвэл тариураар ариутгасан, аллантоик эсвэл амнион шингэнээр сорно. Энэ тохиолдолд халдварт вирус байгаа эсэхийг RGA ашиглан тодорхойлно. Үүнийг хийхийн тулд ижил хэмжээтэй (0.2 мл) вируст тэсвэртэй материал, тахианы улаан эсийн 1% суспензийг холино. Эерэг урвал (материалд вирус байгаа эсэх) эритроцитыг шүхэр хэлбэрээр тунадасжуулах замаар илэрхийлнэ.Хэрэв материалд гемаглютин шинж чанартай вирус байгаа бол түүнийг өргөтгөсөн RGA ашиглан титрлэнэ. гемагглютин үйл ажиллагааны титр. Энэ урвалыг ашиглан гемагглютинацийн вирусын титрийг тодорхойлно - гемагглютинацийн урвалыг өгдөг материалын хамгийн их шингэрүүлэлт. Энэ хэмжээний вирусыг нэг гемагглютин нэгж (HAU) болгон авдаг.RTGA ашиглан томуугийн вирүсийг тодорхойлох
Үүнийг хийхийн тулд эхлээд тодорхой хэмжээгээр вирусын 4 GAO агуулсан вирусын материалын ажлын шингэрүүлэлтийг бэлтгэнэ.Удирдлагын цооногуудад эритроцитуудын тунадас үүссэний дараа урвалыг харгалзан үзнэ. Шинжилгээний цооног дахь гемагглютинацийг удаашруулснаар эерэг хариу үйлдэл үзүүлнэ.Томуугийн вирүсийг янз бүрийн эсийн өсгөвөрийн шугамаар тусгаарлаж болно - хүний үр хөврөл, сармагчингийн бөөр, нохойн бөөрний тасралтгүй эсийн шугам (MDCK) болон бусад. Эсийн өсгөвөрт вирусын цитопатик нөлөө илэрдэг (хүссэн ирмэг бүхий эсүүд, вакуолууд, цөм доторх болон цитоплазмын нэгдлүүд үүсэх) нь эсийн нэг давхаргын доройтолоор төгсдөг.Тусгаарлагдсан вирусыг тодорхойлохын тулд RTGA ашигладаг. (өсгөвөрт шингэний гемагглютинины титр 1:8-аас багагүй байх тохиолдолд). Энэ урвалаас гадна та RGGads хэрэглэж болно, гэхдээ энэ нь бага мэдрэмтгий бөгөөд хамгийн багадаа 1:160 дархлааны сийвэнгийн титр, түүнчлэн RSK, RN, REMA гэх мэтийг шаарддаг.Серологийн судалгаа
Томуугийн оношийг батлахын тулд ийлдэс судлалын шинжилгээг хийдэг. Энэ нь өвчтөний ийлдэс дэх эсрэгбиеийн титрийг 4 дахин ихэсгэхийг тодорхойлоход суурилдаг.Эхний ийлдэсийг өвчний эхэн үед цочмог үед (өвчний 2-5-1 хоног), хоёрдугаарт - 10-аас хойш авдаг. Өвчний 14 дэх өдөр. Ийлдэсийг нэгэн зэрэг хольж болох тул тэдгээрийн эхнийх нь хөргөгчинд -20 ° C-ийн температурт хадгалагддаг. Ихэнх тохиолдолд RTGA, RSK, RNGA хэрэглэдэг. Эдгээр урвалыг стандарт вирусын оношлогооны тусгай багц (янз бүрийн ийлдэс судлалын томуугийн вирүсийн лавлагаа омог) ашиглан гүйцэтгэдэг. Өвчтөний ийлдэс нь өвөрмөц бус гемагглютинацийг дарангуйлагч бодис агуулсан байж болох тул эхлээд 56 хэмийн температурт халааж, тусгай фермент (жишээлбэл, нейраминидаза) эсвэл калийн перидат, риванол, манганы хлорид, цагаан дугуйны суспенз гэх мэт уусмалаар эмчилдэг. тусгай схемийн дагуу. БАГемагглютинацийг дарангуйлах урвал
Гемагглютинацийг дарангуйлах урвалыг туршилтын хуруу шилэнд (макромш тод) эсвэл дархлаа судлалын тусгай ялтсуудад хийж болно.Гөлгөр ирмэг бүхий улаан эсийн нягт, нягт тунадас үүсэх үед урвал эерэг гэж тооцогддог.Экспресс оношлогоо
Энэ арга нь шууд болон шууд бус RIF-д иммунофлуоресценц ашиглан шинжилгээний материалд вирусын өвөрмөц эсрэгтөрөгчийг тодорхойлоход суурилдаг. Салстыг хамрын ишлэлүүд эсвэл залгиурын арын хананаас гаргаж аваад центрифуг хийж, салст бүрхэвчийн булчирхайлаг хучуур эдийн хурдасаас шилэн слайд дээр түрхэц бэлтгэдэг. тэдгээрийг фторохромтой холбосон иммунофлуоресцент ийлдэс, жишээлбэл, FITC (флуоресцеин изотиоцианат) ашиглан эмчилдэг. Эмийг флюресцент микроскопоор шалгаж үзэхэд томуугийн вирүсийн өвөрмөц ногоон шар туяа ажиглагдаж байгаа бөгөөд энэ нь өвчний эхэн үед хучуур эдийн эсийн цөмд нутагшдаг.Сүүлийн үед ELISA, RZNGA, ПГУ-ыг ашиглахыг санал болгож байна. тусгай вирусын эсрэгтөрөгчийг зааж өгөх.Шингээх
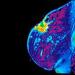
Алдарт "H5N1" гэдэг нь "5 төрлийн гемагглютинин, нэг төрлийн нейраминидаз" гэсэн утгатай - эдгээр хоёр уураг нь томуугийн вирүсийн гадаргуу дээр наалддаг (1-р зурагт гемагглютинин нь ногоон, нейраминидаз нь саарал өнгөтэй).
Гемагглютинины тусламжтайгаар томуугийн вирус нь эсийн гадаргуу дээрх рецепторуудтай холбогддог. Вирусын анхны зорилт нь амьсгалын замын цорго хучуур эдийн эсүүд байдаг, гэхдээ энэ нь бид үүнийг хайрладаггүй: гемагглютинин нь цусны улаан эс зэрэг бусад олон эсийн рецепторуудтай хавсарч чаддаг. Хэрэв нэг вирус хоёр (зэргэлдээх) цусны улаан эсэд нэгэн зэрэг наалдвал цусны улаан эсүүд хоорондоо наалдана! Тиймээс уургийн нэр - "цус наах".
будаа. 1
Хэрэгжилт
Тэнэг эс нь өөрт нь наалдсан вирусыг фагоцитозоор шингээж авдаг - иддэг. Яагаад, яагаад хүүхдүүд дандаа янз бүрийн муухай юм амандаа хийчихдэг юм бэ?! Гэсэн хэдий ч вирус нь эсийн дотор хоол хүнс болгон, фагоцитозын цэврүүт дотор байдаг (Зураг 2 - "эндосом"). Эндосом нь лизосомтой нийлж, хоол боловсруулах вакуоль үүсч, цитоплазмаас протонуудыг шахаж хүчиллэг орчин үүсгэдэг (энэ үйл явцыг 2-р зурагт үзүүлэв) - арай илүү, бид вирусыг шингээх болно (зураг 2-т). "уурагтай хоол, ялгаа нь юу вэ" гэсэн үгс).

будаа. 2
Тууз
Гэхдээ вирус ийм эргэлтэнд бэлэн байна:
 будаа. 3 |
- Гемагглютинин нь хүчиллэг орчны нөлөөн дор өөрчлөгддөг - түүний гадаргуу нь гидрофиль болж хувирдаг бөгөөд энэ нь (өмнө нь эндосомын мембраны дотоод гадаргуу дээрх рецепторт наалддаг байсан) энэ мембран дотор суулгагдсан байдаг.
- Эндосом руу шахагдсан протонууд нь тусгай сувгийн уургуудаар (1-р зураг, 3-р зурагт заасан М2 уураг) вирусын липидийн бүрхүүлээр дамжин вирусын уургийн бүрхүүлд хүрдэг (1-р зурагт - цагаан бөмбөлгүүдийн тойрог) - M1 уураг). Үүнээс болж уургийн бүрхүүл устсан (Зураг 3-т устгасан уургийн бүрхүүлийн M1 уургууд нь улаан од гэж тэмдэглэгдсэн).
- Вирусын липидийн бүрхүүл (гемагглютинины нэвтрэн орох үйл ажиллагааны улмаас) фагосомын (липид) мембрантай нийлдэг; Вирусын РНХ нь эсийн цитоплазмд төгсдөг.
Вирусын хуулбар
Цитоплазмд ялгарсан вирусын РНХ нь өөрөө бүрэн аюулгүй байдаг.
- Үүн дээр уураг үүсгэх боломжгүй, учир нь энэ нь хасах РНХ (уураг нь түүгээр кодлогдохгүй, харин одоохондоо байхгүй нэмэлт нэмэлт хэлхээгээр кодлогддог).
- Үүн дээр РНХ хийх боломжгүй - бидний эсүүдэд РНХ-ийг хоёр дахин нэмэгдүүлэх чадвартай фермент байдаггүй.
"Өө-хо-хо, чамд юу ч байхгүй" гэж томуугийн вирус сахалтай толгойгоо сэгсэрч, "Гэхдээ зүгээр, би бүгдийг нь авчирсан." Вирус нь РНХ-ээс хамааралтай РНХ полимераза үүсгэдэг PB1, PB2, PA уурагуудыг авчирсан бөгөөд энэ нь РНХ-ийг хуулбарлаж чаддаг. Гэхдээ азгүй! Ямар ч полимераза ажиллаж эхлэхийн тулд праймер хэрэгтэй, гэхдээ мартамхай томуу үүнийг авч явсангүй! Бүх зүйл дууссан?!
Тайвшир, бүү сандар! - Эдгээр үгсээр бүхэл бүтэн компани (8 вирусын РНХ, 3 вирусын фермент) эсийн цөм рүү илгээгддэг. Тэнд ханиад бүрэн үйлчилгээ үзүүлдэг:
- вирусын РНХ-ийн хуулбарлах праймерууд (нэмэх РНХ авах) нь эсийн РНХ-ээс хуваагдсан хэсгүүд юм;
- боловсруулалт: РНХ-ийн нийлэгжилтэнд праймер үүрэг гүйцэтгэдэг хэсгүүд - эдгээр нь таг байсан тул 5" төгсгөлийн өөрчлөлтийг хамгийн эхэнд хийсэн; синтезийн төгсгөлд 3" төгсгөлийн полиаделяци үүсдэг;
- залгах: хоёр уургийн мэдээлэл агуулсан зарим вирусын РНХ хоёр хэсэгт хуваагдана.
Ийм байдлаар РНХ-г нэмж нийлэгжүүлдэг бөгөөд энэ нь вирусын уураг ба вирусын хасах РНХ-ийн нийлэгжилтийн загвар болж чаддаг.
Дараа нь бүх зүйл энгийн: тэнэг эс нь өөрийн амин хүчлээс рибосомоо ашиглан вирусын уураг, түүний дотор РНХ-ээс хамааралтай РНХ полимеразаг нэгтгэдэг. Томуугийн эсрэг РНХ нь мөн цөм дотор эрчимтэй үүсдэг. Вирусын хэсгүүдийн цугларалт нь цитоплазмд, эсийн мембраны дотоод гадаргуу дээр үүсдэг. Бэлэн болсон вирус нь экзоцитозоор (нахиалах) эсийг орхиж, нейраминидаз нь эс болон шинэ төрсөн вирусыг холбосон сүүлчийн утсыг хаздаг ... Дэлхий дээр шинэ (муу) бяцхан амьдрал гарч ирэв!

будаа. 4
K. SOLTISSEK болон H.-D. КЛЕНК (СН. ШОЛТИССЕК, Х.-Д. КЛЕНК)
I. ТАНИЛЦУУЛГА
Томуугийн вирүсийг хуулбарлах асуудлын талаар олон тооны тоймууд байдаг. 1968 оноос өмнөх уран зохиолыг Хойл (1968), Шолтиссек (1969) нарын нийтлэлд нэгтгэн харуулсан бол сүүлийн үеийн бүтээлүүдэд Уайт (1973), Компанс, Чоппин (1974) нарын тоймууд багтсан болно.
Репликацийн талаарх ихэнх мэдээллийг томуугийн вирүсийн А хэлбэрийн судалгаагаар олж авсан. Бусад төрлийн томуугийн вирүсийн нөхөн үржихүйн механизмд мэдэгдэхүйц ялгаа хараахан олдоогүй байна.
Дэгдээхэйний үр хөврөлийн фибробласт эсүүдэд томуугийн вирүсийн WSN омгийг MDBK эсэд (Чоппин, 1969) үржүүлэх эсвэл шувууны тахлын вирүс (FPV) үржүүлэх зэрэг репликацийг судлахад тохиромжтой хэд хэдэн эсийн өсгөвөрлөх системүүд өргөн тархсан. Сүүлчийн вирүсийн өсөлтийн муруй нь нэг мөчлөгт 30-д нотлогдсон бөгөөд далд хугацаа нь ойролцоогоор 3 цаг, вирусын үйлдвэрлэл 8-12 цагийн хооронд өндөрлөгт хүрдэг.Ерөнхийдөө ийм эсийн системд өндөр ургац өгдөг. халдварт вирус ажиглагдаж, халдварын дараа эсийн уургийн нийлэгжилтийг маш үр дүнтэй дарангуйлдаг. Тиймээс ийм систем нь биохимийн судалгаа хийхэд маш тохиромжтой.
II. ВИРУС НЭВТГЭХ, НЭВТРЭХ, “ХУУЛАХ”
Вирусын эсийн халдвар нь шингээлтээс эхэлдэг, өөрөөр хэлбэл вирусын тоосонцор эсийн гадаргуу дээр наалддаг. Хавсаргахад хоёр нэмэлт бүтэц шаардлагатай, тухайлбал: эсийн гадаргуу дээрх рецепторын хэсгүүд ба эдгээр рецепторуудыг таних үүрэгтэй вирусын бүрэлдэхүүн хэсэг.Томуугийн вирүс нь янз бүрийн гаралтай эритроцитуудтай харилцан үйлчилж, тэдгээрийг агглютинжуулах чадвар нь олон жилийн туршид мэдэгдэж байсан. (Hirst, 1941; McClelland, Hare, 1941) Гемагглютинацийг томуугийн вирүс эсийн гадаргуутай харилцан үйлчлэх загвар урвал болгон ашигласан бөгөөд “энэ үзэгдлийн талаарх таны ихэнх мэдлэгийг ижил төстэй судалгаанаас авсан болно. Гэсэн хэдий ч эритроцитын гадаргуу болон халдвар авсан эсийн гадаргуу нь огт өөр байж болох тул ерөнхий дүгнэлт хийхдээ маш болгоомжтой байх хэрэгтэй (мөн 3-р бүлгийг үзнэ үү).
A. ГЕМАГГЛЮТИНИНИЙГ АДСОРБЦИНД ГҮЙЦЭТГЭХ ҮҮРЭГ
Холболтод оролцдог вирионын бүрэлдэхүүн хэсэг нь HA* "баяжуулалт" юм. Халдвар эхлэхэд вирусын β-уургийн үүргийг HA* ба NA* гэсэн хоёр гадаргуугийн уургийн өвөрмөц эсрэгбиемүүдийг ашиглан судалсан. Эдгээр эсрэгбиемүүдийг рекомбинант вирус ашиглан олж авч болно. Жишээлбэл, AO болон A2 вирүсийн хоорондох хөндлөн огтлолын үр дүнд HA*, AO, NA* A2-ийг агуулсан рекомбинант X7F1 үүсдэг (Kilbourne et al., 1968). X7F1 вирусын эсрэг ийлдэс нь AO төрлийн томуугийн вирүсийн NA*-ыг дарангуйлдаггүй, харин гемагглютинацийг дарангуйлж, энэ төрлийн вирусын халдварыг саармагжуулдаг. Нэг ийлдэс нь томуугийн A2 вирүстэй харилцан үйлчлэлцэх нь NA* идэвхжилийг саармагжуулж дууссан ч гемагглютинаци болон халдварт өвчнийг саатуулдаггүй. Тиймээс NA* нь халдварын эхлэлд оролцдоггүй бөгөөд зөвхөн NA* нь шингээлтийг хариуцдаг бололтой. Энэ үзэл баримтлалыг протеолитик ферментийн тусламжтайгаар зөвхөн нейраминидазын "баяжуулалт" устгасан вирусын тоосонцор халдвартай хэвээр байна гэсэн мэдээллээр нотлогддог (Schulze, 1970).
Гемагглютинжуулагч хэсэг нь нүүрс усаар баялаг HA* "баяжуулалтын" гадна хэсэгт байршдаг гэсэн нотолгоо байдаг (3-р бүлгийг үз). Гликозилээгүй HA* уураг нь цусны улаан эстэй холбогдож чаддаггүй тул нүүрс ус нь HA* үйл ажиллагаанд зайлшгүй шаардлагатай юм шиг санагддаг (Klenk et al., 1972b).
B. ТОМУУНЫ ВИРУС РЕЦЕПТОР
Нүүрс ус нь зөвхөн гемагглютинин төдийгүй эсийн гадаргуу дээрх вирусын рецепторын чухал бүрэлдэхүүн хэсэг юм.Hirst (1942) вирус-эритроцитын цогцолбор тогтворгүй, эсийн гадаргуу дээрх рецептор нь вирусын ферментийн нөлөөгөөр устдаг болохыг ажигласан. Дараа нь харуулсанчлан, энэ фермент нь нейраминидаз бөгөөд гликопротейноос мэдрэлийн хүчлийг ялгаж салгадаг (Klenk et al., 1955; Klenk, Stoffel, 1956; Gottschalk, 1957). вирусын тоосонцор.Бактерийн нейраминидаза нь томуугийн вирүсийн рецепторыг устгах чадвартай (Бурнет, Стоун, 1947) Иймээс томуугийн вирүсийн рецептор нь нейроминий хүчил агуулсан гликопротейн болох нь тогтоогдсон.
Түүнээс хойш маш их мэдээлэл хуримтлагдсан
миксовирусын рецепторын талаар саяхан тоймлон бичсэн
Хьюз (1973). Хүлээн авсан өгөгдлийг дараах байдлаар товч тоймлон харуулав.
үлээж байна Рецепторын хэсгүүд нь мэдрэлийн эсийн үлдэгдлийг агуулдаг.
нүүрс усны гинжин хэлхээнд байдаг ионы хүчил
гликопротейнууд. Нейроми-ийн исэлдүүлэхгүй терминалын үлдэгдэл
Носнла нь гликопротеины вирустай харилцан үйлчлэхэд шаардлагатай байдаг
Оросын ханиад. Нейраминидазын эмчилгээ нь бүрэн арилдаг
холбох үйл ажиллагаа. -тэй хамт доройтлын судалгаа
periodate ашиглан холбоход зориулагдсан гэж үздэг
үйл ажиллагаа нь бүрэн бүтэн нейрамин молекулыг шаарддаг
хүчил (Суттажит ба Винзлер, 1971). карбоксил бүлэг,
зайлшгүй шаардлагатай тул бас чухал үүрэг гүйцэтгэдэг байх
бололтой, мөн цахилгаан статик хүч (Хуан, 1974).
Зөвхөн сул амтлагч байдаг бололтой
түүнтэй холбоотой бүтэцтэй харьцуулахад бие махбодийн байдал
Энэ нь бүхэлдээ нотлогдсон тул нейроамин хүчил
жаурамины хүчил агуулсан гликопротеины багц;
миксовирустай холбогддог. Түүнчлэн, ганглиозидууд (гли-
энэ талаар идэвхтэй ажиллаж байна (Haywood, 1975).
Хүлээн авагчийн молекулын бүтэц тогтсоны дараа томуугийн вирүстэй холбоотой асуудал тодорхой болно гэж найдаж байна. Эритроцитуудын хувьд энэ нь тодорхой хэмжээгээр аль хэдийн хүрсэн байна (Marchesi нар, 1973). Миксовирусын хиймэл мембранд наалдсан байдлыг судлах замаар нэмэлт мэдээллийг өгч болно (Тиффани ба Блоу, 1971).
B. НЭВТРҮҮЛЭХ, “ХУУРАХ” БОЛОМЖТОЙ МЕХАНИЗМ
Зөвхөн томуугийн вирүс төдийгүй ерөнхийдөө гаднах бүрхүүлтэй вирүсийн "нэвтрэх, тайлах" хоёр өөр механизмыг санал болгосон. Энэ хоёр үзэл бодол нь голчлон электрон микротранч дахь судалгаанд тулгуурладаг. Эдгээр механизмын нэг нь: Виронексис нь ппноцитозын үйл явц гэж үздэг бөгөөд энэ нь вирусын тоосонцор нь пиносомтой нийлж, улмаар лизосомтой нийлж, лизосомын ферментүүд нь вирусыг "тайлахад" хүргэдэг (Фазекас де Сент Грот, 1948) Электрон микроскопоор баталгаажуулсан процесс юм. Энэ үзэл бодлыг Дэйлс, Чоппин (1962), Дурмашкин, Тиррел (1970) нарын бүтээлээс олж авсан. Халдвар авснаас хойш 10 минутын дараа вирусын тоосонцор эсийн гадаргуутай шууд харьцаж, 20 минутын дараа тоосонцор нь харагдах болно. цитоплазмын вакуоль дотор олддог.Морган, Роуз (1968) нарын энэхүү судалгаанаас ялгаатай нь вирусын дугтуйг эзэн эсийн мембрантай нийлүүлсний үр дүнд нэвтэрч болно гэж үзэж байна.Тиймээс томуугийн вирүс нэвтрэх механизмын талаар одоогоор зөвшилцөлд хүрээгүй байна.
Бүлэгт тайлбарласны дагуу. 5, томуугийн вирүсийн вирионууд нь рибонуклеопротеины бүрэлдэхүүн хэсгүүдтэй холбоотой РНХ полимеразыг агуулдаг.Иймээс "хувцас тайлах" үйл явц нь рибонуклеопротейн ялгарах үйл явцаас орон зайн хувьд тусгаарлагдахгүй байх магадлал багатай. Мөн энэ үе шат нь эсийн гадаргуу дээр, механизмын дагуу явагддаг. мембраны нэгдэл, фагоцитийн цэврүүтүүдэд вирохексийн механизмын дагуу.
III. ТРАНСКРИПЦИЯ A. РНХИЙН НИЙГЛЭЛИЙН ДАРААЛ
"Хувцсаа тайлсны" дараа вирионын sRNA нь нэмэлт РНХ болон хувирах ёстой.Халдвар үүсгэгч бөөмстэй хамт нэвтрүүлсэн РНХ полимераз нь вирусын тархалтын эхний үе шатанд ажиллах ёстой (5-р бүлгийг үзнэ үү). Томуугийн вирүсийн геномыг зөвхөн хэлбэрээр нь вирионоос тусгаарлаж болно
салангид хэсгүүд (6-р бүлгийг үзнэ үү). Түүгээр ч зогсохгүй энэ нь тусдаа фрагмент хэлбэрээр үйлчилдэг нь генетикийн шинжилгээ (7-р бүлэг) болон халдварт вирусыг үе шаттайгаар идэвхгүйжүүлэх (Шолтиссек, Ротт, 1964) -ээр тодорхойлогддог. Үүнтэй холбогдуулан полимераз нь синтезийг эхлүүлдэг гэж үзэх нь зүйтэй. Хувь хүний фрагмент бүрийн РНХ РНХ нь эсэд чөлөөт молекул хэлбэрээр байдаггүй, харин үргэлж уургаар бүрхэгдсэн байдаг тул репликацийн явцад вирусын РНХ ямар уурагтай холбоотой вэ гэсэн асуулт гарч ирнэ.
Томуугийн вирүсийн РНХ-ийн нийлэгжилтийг судлах туршилтууд нь ихээхэн бэрхшээлтэй тулгардаг, учир нь актиномицин D нь эсийн РНХ-ийн нийлэгжилтийг дарангуйлах үед вирусын РНХ-ийн нийлэгжилтийг илрүүлэхэд ашиглах боломжгүй, учир нь энэ антибиотик нь томуугийн вирүсийн нөхөн үржихүйг дарангуйлдаг. Barry et al., 1962; Rott, Scholtissek, 1964; Barry et al., 1965; Pons, 1967). Энэ шалтгааны улмаас РНХ-ийн нийлэгжилтийн цаг хугацааны дарааллыг тодорхойлохын тулд халдварын дараа янз бүрийн цэгүүдэд импульсийн шошготой РНХ-ийн өвөрмөц эрлийзжүүлэлт, шошгогүй vRNA эсвэл vcRNA-ийн аль нэгээр нь илүүдэлтэй, дараа нь RNase-ийн эмчилгээг ашигласан (Scholtissek and Rott, 1970). Халдварт мөчлөгийн эхний үе шатанд vcRNA-ийн нийлэгжилт давамгайлж, халдвар авснаас хойш ойролцоогоор 2 цагийн дараа дээд хэмжээндээ хүрч байсан бол хожуу үе шатанд вирусын өвөрмөц РНХ-ийн ихэнх нь vRNA үүсдэг. Круг (1972) өөр аргыг ашиглан халдвар авснаас хойш 4 цагийн дараа BIKRNA синтез бараг бүрэн зогсдог болохыг харуулсан. Фенолыг олборлосны дараа харьцангуй бага хэмжээний lncRNA илэрдэг (Scholtissek and Rott, 1970).
Нэг буюу өөр төрлийн вирусын РНХ нь мэдээллийн1 !! Энэ нь вирусын уургийн нийлэгжилтийн загвар болгон ашиглагддаг (IVA хэсгийг үзнэ үү) вирусын РНХ-ийн дифференциал катаболизмын түвшинд зарим орчуулгын хяналт байж болно. Тиймээс томуугийн вирүсийн РНХ-ийн тогтвортой байдлыг судлахын тулд импульсийн хөөх туршилтыг in vivo хийсэн. Вирусын РНХ нь эсийн РНХ-ээс ялгаатай нь 90 хоногийн хугацаанд бүрэн тогтвортой байдаг нь тогтоогдсон (Scholtissek et al., 1972).
Өмнө нь вирусын РНХ-ийн нийлэгжилтийг in vivo судлахдаа халдварын мөчлөгийн хожуу үе шатанд актиномицин D нэмсэн үед (Duesberg and Robinson, 1967; Nayak, 1970; Ma-hy, 1970) тэд үүнийг анхаарч үзээгүй. антибиотик нь in vivo нэмэлт РНХ-ийн нийлэгжилтийг тусгайлан дарангуйлдаг (Scholtissek and Rott, 1970; Pons, 1973). lncRNA нь халдвар авсан эсүүдээс дор хаяж таван тусдаа фрагмент хэлбэрээр ялгардаг тул вирусын РНХ нь фрагмент хэлбэрээр нийлэгждэг гэж дүгнэсэн (Понс ба Хирст, 1968).
B. ВИРУСИЙН РНХИЙН НИЙГЛЭЛИЙГ БАЙГУУЛЛАГЧ ЭСИЙН ДОТОР БАЙГУУЛАЛТ
Авторадиографийн аргаар олж авсан мэдээллээс үзэхэд вирусын РНХ-ийн нийлэгжилтийн газар нь эсийн цөм юм гэж дүгнэсэн (Scholtissek et al., 1962; Barry et al., 1974). Эдгээр судалгаанд ашигласан импульсийн хугацаа хэтэрхий урт хэвээр байсан тул вирусын РНХ нь эсийн цитоплазмд нийлэгжиж, улмаар цөмд шилжиж, хуримтлагдах боломжтой гэдгийг үгүйсгэх аргагүй юм. Үүнээс гадна vRNA болон cRNA нь эсийн өөр өөр газарт нийлэгжиж болно.
B. ВИРУС РНХИЙН НИЙГЛЭЛИЙГ ДАРАН АВАХ 1. Актимомицин D, митрамицин, а-аманитин.
Вирусын РНХ-аас хамааралтай РНХ полимераза аль хэдийн байгаа үед (жишээлбэл, халдвар авснаас хойш 2 цагийн дараа) ДНХ-ийн загварт саад учруулдаг актиномицин D эсвэл митрамициныг халдвар авсан эсүүдэд нэмэхэд vRNA ойролцоогоор 2 дахин нийлэгдэнэ. Харин VcRNA үйлдвэрлэл шууд зогсдог. Дараа нь vRNA-ийн нийлэгжилт мөн буурч байгаа нь vRNA-г тасралтгүй үүсгэх шаардлагатайг харуулж байна (Rott et al., 1965; Scholtissek and Rott, 1970; Scholtissek et al., 1970; Pons, 1973). Грегориадес (1970) актиномицин D нь халдварын мөчлөгийн сүүлээр нэмэгдэхэд vRNA нийлэгжилтэнд хүчтэй нөлөө үзүүлдэг болохыг харуулсан. Эдгээр туршилтуудаар вирусын РНХ-ийн нийлэгжилтийг халдвар авсан эсийн нийт РНХ-д шошготой уридиныг нэгтгэх замаар тодорхойлсон. Энэ өсөлтийг актиномицин D нэмснээр арилгаж болно. Гэсэн хэдий ч томуугийн вирүсийн халдвар нь халдварын дараа эсэд шошготой uridine-ийн нийлэгжилтийг ихэсгэдэг (Scholtissek et al., 1967) ба актиномицин D гэдгийг анхаарах хэрэгтэй. Энэ нэгдэлд дарангуйлах нөлөө үзүүлдэг (Scholtissek et al., 1967). ., 1969). СиАманитин нь ДНХ-тэй ямар ч хамааралгүй бөгөөд эсийн РНХ полимеразуудын аль нэгнийх нь идэвхжилд нөлөөлдөг (РНХ подимераз II), мөн халдварын дараа шууд өсгөвөрийн шингэнд нэмэхэд кРНХ-ийн нийлэгжилтийг дарангуйлдаг (Rott and Scholtissek, 1970; Mahy et бусад, 1972).
Эдгээр антибиотикууд cfRNA нийлэгжилтийг дарангуйлах механизм нь бүрэн тодорхойгүй, учир нь тэдгээр нь in vitro cfRNA үүсэхэд нөлөөлдөггүй.Иймээс эдгээр антибиотикууд нь зөвхөн in vivo үйлчилдэг боловч cfRNA-г нийлэгжүүлдэг ферментийг тэдгээр эсээс тусгаарлаж болно. Халдвар авснаас хойш 2 цагийн дараа актиномицин D нэмсэн (Scholtissek and Rott, 1969a).
Томуугийн вирүсийн нөхөн үржихүйг эзэн эсийн ДНХ-д үзүүлэх бусад нөлөөлөл - митомцин С-ийг нэвтрүүлэх, хэт ягаан туяагаар урьдчилан эмчлэх, эсвэл халдвар авахаас өмнө эсийн цөмийг зайлуулах зэргээр дарангуйлж болно (Barry, 1964; Rott et al., 1965; Nayak, Расмуссен, 1966; Фол-Летт нар, 1974; Келли нар, 1974). Эдгээр үр нөлөө нь томуугийн вирүсийн нөхөн үржихүйд нөлөөлөх механизм нь бусад антибиотикуудын үйл ажиллагааны механизмтай ижил байж болох юм.Эдгээр судалгаанаас үзэхэд цорын ганц таамаглал бол "функциональ" идэвхтэй эсийн цөм, хэрэгцээ юм. (эсвэл) томуугийн вирүсийг тараах эсийн ДНХ-ээс хамааралтай үйл ажиллагаанд. Эдгээр функцууд нь юу болохыг хэлэх боломжгүй юм.
2. Циклогексимид
Амьтны эсийн уургийн нийлэгжилтийг тусгайлан саатуулдаг циклогексимидийг томуугийн вирүсээр халдварласнаас хойш 2 цагийн дараа нэмэхэд vRNA үүсэх нь шууд зогсдог бол vRNA үүсэх нь дор хаяж 2 цаг үргэлжилдэг (Шолтиссек ба Ротт, 1970; Понс. , 1973). "vRNA-г нийлэгжүүлдэг полимеразын чанар/кофактор" болгон ашигладаг вирусын болон эсийн уургийн тасралтгүй нийлэгжилт шаардлагатай эсэх, эсвэл шинээр нийлэгжсэн vRNA-г тогтворжуулахад зарим "уураг (жишээ нь, NP уураг) шаардлагатай эсэх нь одоогоор тодорхойгүй байна. эсвэл тодорхой вирусын "уургийн нийлэгжилтийг дарах нь кРНХ тасралтгүй үүсэхэд хүргэдэг бөгөөд нийлэгжилт нь халдвар авснаас хойш 3 цагийн дараа унтардаг. Энэ унтрах нь vRNA нийлэгжилтийг өдөөх шаардлагатай байж магадгүй. Температурт мэдрэмтгий мутантуудтай хийсэн судалгаа нь эдгээр асуултын заримд нь хариулах ёстой.
Bean, Simpson (1973) нарын туршилтууд нь in vivo анхдагч транскрипцийг (халдвар үүсгэгч бөөмийн полимеразыг ашиглан РНХ загварт cRNA-ийн нийлэгжилт) циклогексимидээр дардаггүй, харин актиномицин D нь транскрипцийг бүрэн дардаг болохыг харуулсан. Тиймээс циклогексимид нь халдварт тоосонцортой хамт нэвтэрч, cfRNA-г нийлэгжүүлдэг полимеразын идэвхжилд in vivo нөлөөлдөггүй боловч cfRNA үйлдвэрлэхэд шаардлагатай шинэ полимеразын нийлэгжилтийг дарангуйлдаг.
3. Глюкозамин
Глюкозамин нь UTP-]M-ацетилглюкозамин үүсгэн дэгдээхэйний үр хөврөлийн эс дэх UTP санг шавхдаг нь мэдэгдэж байна (Scholtissek, 1971). Глюкоз агуулсан Earl-ийн уусмалыг өсгөвөрлөх тэжээл болгон ашиглах үед энэ
Энэ нь зөвхөн вирусын глнкопротеины нийлэгжилтэнд нөлөөлдөг (V хэсгийг үз). Гэсэн хэдий ч эрчим хүчний эх үүсвэр болох глюкозыг лируват эсвэл фукозоор сольсон бол эдгээр амин элсэн чихэрээр UTP усан санг шавхах нь ойролцоогоор 10 дахин илүү идэвхтэй явагддаг. Ийм нөхцөлд эзэн эсийн UTP сан нь vРНХ-ийн нийлэгжилтийн хурдыг тодорхой хязгаарлагч болж, харин эсийн РНХ-ийн нийлэгжилтэнд хараахан нөлөөлөөгүй байна (Шолтиссек, 1975) Вирусын РНХ-ийн нийлэгжилтийг дарангуйлсны үр дүнд вирусын уураг үүсэх нь бас байхгүй.
Эдгээр өгөгдлийг хоёр янзаар тайлбарлаж болно: вирусын РНХ-аас хамааралтай РНХ полимераза нь эсийн ДНХ-аас хамааралтай ба RIC полимеразуудтай харьцуулахад UTP-д бага хамааралтай эсвэл эсэд UTP-ийн бие даасан хоёр ба түүнээс бага усан сан байдаг. Энэ нь "вирусын РНХ-ийн нийлэгжилтэд ашиглагдах боломжтой бөгөөд бусад усан сангаас илүү глюкозаминд нөлөөлдөг бөгөөд РНХ полимеразын субстрат болгон ашиглаж болно.
D. ВИРҮСИЙН РНХИЙГ VITRO-Д ХИЙХ
Томуугийн вирүсээр халдварласан эсүүдэд хэд хэдэн судлаачид РНХ-аас хамааралтай РНХ полимеразыг илрүүлсэн (Хо, Уолтерс, 1966; Scholtissek, Rott, 1969a; Skehel, Burke, 1969; Ruck et al., 1969; Mahy, Bromley, 1970; Compans, Caligui). , 1973). Ферментийн ихэнх идэвхжил нь халдвар авсан эсийн микросомын фракцаас илэрсэн. In vitro системд энэ үйл ажиллагааг RNase устгадаг боловч ДНХ-ээр арилгадаггүй. Энэ нь дотоод загвар нь РНХ гэсэн үг юм- Урвал нь бүх дөрвөн нуклеозид трифосфат байх шаардлагатай бөгөөд актин-ицин D-д мэдрэмтгий байдаг. In vitro урвалын үйлдвэрлэлийн ихэнх нь харьцангуй бага молекул жинтэй байдаг. Horisberger, Guskey (1973) нарын өгөгдлөөс үзэхэд цитоплазмд хоёр өөр ферментийн үйл ажиллагаа байдгийг харуулж байна: нэг нь Mg++-аас хамааралтай ба давсны концентраци харьцангуй өндөр байснаас дарангуйлагддаг, нөгөө нь Mn++ хамааралтай ба давсанд илүү тэсвэртэй байдаг. Сүүлчийн ферментийн идэвхжил нь вирусийн бөөмс дотор байдаг (5-р бүлгийг үз).
In vitro систем дэх цитоплазмын ферментийн бүтээгдэхүүний талаар зөрчилтэй үр дүн гарсан. Рак ■болон бусад. (1969) тэдний гарт энэ фермент нь дор хаяж "вирион төрлийн РНХ-ийн заримыг (14-19S) нийлэгжүүлдэг" гэж мэдээлсэн. Зохиогчид микросомын инкубацийн дараа in vitro системд бүтээгдэхүүний үндсэн найрлагыг тодорхойлохдоо ийм дүгнэлтэд хүрсэн байна. Мэдэгдэж буй өвөрмөц цацраг идэвхт дөрвөн шошготой нуклеозид трифосфаттай фракц. Гэсэн хэдий ч хамгийн ойрын судалгааны мэдээлэл
[(a-32P]ATP ашиглан ижил ажилд олж авсан аденилийн хүчлийн хөршүүд нь Scholtissek (1969)-ийн олж авсан хамгийн ойрын хөршийн шинжилгээний өгөгдөлтэй нийцэж байгаа бөгөөд үүний үр дүнд in vitro систем дэх бүтээгдэхүүн нь бүтэцтэй гэсэн дүгнэлтэд хүрсэн. Махи, Бромли нар (1970) анхны хэвлэлдээ цитоплазмын ферментээр үүсгэгдсэн in vitro систем дэх бүтээгдэхүүний зарим хэсэг нь "vRNA байх" ёстой гэж тэмдэглэсэн байдаг. болон Өвөрмөц эрлийзжүүлэлт нь цитоплазмын ферментийг бараг зөвхөн cRNA-аас бүрдүүлдэг болохыг анх Scholtissek (1969) харуулсан. Калигуири, Компанс (1973) мөн томуугийн вирусээр халдварласан эсийн цитоплазмаас РНХ полимеразыг тусгаарлаж, РНХ-д нийлэгждэг. in vitro систем нь 90% -иас багагүй нь hsRNA-д нэмэлт суурь дараалалтай байдаг.Hastie and Mahy (1973) "актиномицин D-ийн оролцоотойгоор цөмийн ферментээр нийлэгжүүлсэн in vitro систем дэх бүтээгдэхүүний ихээхэн хувь нь "боломжтой" болохыг тогтоожээ. шошгогүй vRNA-тай пибридизаци хийх боломжгүй.Ямар төрлийн РНХ ийм эрлийзжүүлэх чадваргүй болох нь одоогоор тодорхойгүй байна. Эдгээр нөхцөлд нийлэгжсэн РНХ-ийн маш бага хэсэг нь шошгогүй aRNA-тай эрлийзждэг (Шолтиссек, хэвлэгдээгүй өгөгдөл).
Вирусын РНХ-д шошготой GTP-ийг оруулах кинетикийг in vitro системд РНХ-ийн синтез дахин эхлүүлэхгүй байгааг харуулж байна гэж тайлбарлаж болно. Хэрэв түүхий ферментийн бэлдмэлийг давсны бага концентрацид өсгөвөрлөсөн бол шинээр нийлэгжсэн бараг бүх РНХ нь нэг судалтай байдаг. Гэсэн хэдий ч фенолоор олборлосны дараа "РНХ-ийн ихээхэн хувь нь РНХ-д тэсвэртэй болдог. Фенол нь нэг судалтай загвар ба шинээр нийлэгжсэн кРНХ-ээс бүрдэх завсрын репликацын бүтцийг полимеразын молекулаар репликацын талбайд нэгтгэж, хувиргадаг. хэсэгчлэн давхар судалтай бүтэц (Feix нар, 1967; Oberg, Philipson, 1971). In vitro систем дэх томуугийн вирусын ферментийн бүтээгдэхүүний талаарх эдгээр өгөгдлийг полимераз нь зөвхөн полимержилтийг эхлүүлж, үргэлжлүүлээд зогсохгүй шинээр нийлэгжсэн гинжийг загвараас нь салгаж байна гэсэн үг юм. Үгүй бол биологийн ямар ч үүрэг гүйцэтгэдэггүй хоёр судалтай РНХ-ийн бүтэц үүсдэг (Paffenholz, Scholtissek, 1973) Хэрэв инкубацийг давсны өндөр концентрацитай эсвэл цэвэршүүлсэн ферментээр явуулбал бүтээгдэхүүний томоохон хувь нь аль хэдийн хоёр судалтай РНХ байдаг. фенол олборлохоос өмнө (Schwartz, Scholtissek, 1973).
Томуугийн вирүсийн РНХ полимеразагийн энэхүү шинж чанарыг зөвхөн cfRNA-г in vitro системд нийлэгжүүлэх зорилгоор ашигласан.
Энэ нь томуугийн вирүсийн өөр өөр омгийн генетикийн хамаарлыг тэдгээрийн хоорондын үндсэн дарааллаар гомологи тодорхойлох замаар тогтоох гэж нэрлэдэг (Scholtissek, Rott, 1969b; Hobson, Scholtissek, 1970; Anschutz et al., 1972).
IV. ВИРУС УУРАГНЫ НИЙСЛЭЛ
A. IN VITRO ОРЧУУЛГА
Вирусын уургийн нийлэгжилтэнд ямар төрлийн РНХ-вирионы ион эсвэл нэмэлт болох тухай асуудал хараахан шийдэгдээгүй байна.Полисомтой холбоотой вирусын өвөрмөц РНХ-ийн төрлийн талаар зөрчилтэй үр дүн гарсан.Наяк (1970) полисомын бүсэд сахарозын градиент, голчлон vRNA, харин Понс (1972) зөвхөн vcRNA-г полисагаас тусгаарласан. Сүүлийнх нь актиномицин D-ийг нэмсний дараа vcRNA-ийн нийлэгжилтэд илүү нөлөөлдөг болохыг ажигласнаар нотлогдсон (III, B хэсгийг үзнэ үү). 1), халдвар авснаас хойш 2 цагийн дараа халдвар авсан эсийн полисомд cfRNA илрээгүй (Pons, 1973).
Siegert нар (1973) E. coli болон томуугийн вирүсийн vRNA-ийн уургийн синтезийн системийг загвар болгон ашиглаж, вирусын NP уураг үүсэхийг нээсэн. Энэ шошготой NP уураг нь Ouchterlony тестийг ашиглан гель тунадасжилтаар тодорхойлогддог. , Kingsbury and Webster (1973) нар туулайн ретикулоцитээс гаргаж авсан уургийн нийлэгжилтийн системийг ашиглан vRNA-тай вирусын уургийн нийлэгжилтийг ажиглаагүй. Гэсэн хэдий ч ижил системд тэд РНХ дээр вирусын М уургийн нийлэгжилтийг (om. 2-р бүлэг) илрүүлсэн. халдвартай эсээс тусгаарлагдсан загвар.Иймээс одоогоор зөвхөн вириоп уу эсвэл зөвхөн нэмэлт үү, эсвэл нэг төрлийн РНХ-ийн фрагмент ба өөр төрлийн РНХ-ийн фрагментийг уургийн нийлэгжилтэнд загвар болгон ашиглаж байна уу гэсэн асуултад одоогоор хариулах боломжгүй байна. Балтимор (1971)-ийн санал болгосны дагуу томуугийн вирүс "сөрөг" эсвэл "эерэг" вирусын гинжин хэлхээний тодорхойлолтыг хэрэглэхэд одоогоор хэцүү байна.
B. ВИРУС УУРАГНЫ НИЙСЛЭЛИЙН АМЬД БАЙДАЛ
Вирусын "уураг" -ын нийлэгжилтийг судлах нь халдвар авсан эсэд эсийн полипептидийн нийлэгжилтийг вирусын өвөрмөц синтезээр сольсонтой холбоотой юм. ХПВ-ээр халдварласан тахианы үр хөврөлийн фибробласт эсүүдэд (Joss et al., 1969; Skehel, 1972; Klenk, Rott, 1973) болон WSN томуугийн вирүсээр халдварласан BHK 2IF эсүүдэд (Lasarowitz et al., 1971) Халдвар авснаас хойш бараг 4 цагийн дараа нийлэгждэг
зөвхөн вирусын уураг (31). Хэсэг хугацааны өмнө судлаачид халдвар авсан хачигт гурав, дөрвөн полипептидийн нийлэгжилтийг ажигласан (Taylor et al., 1969; Joss et al., 1969; Holland, Kiehn, 1970; White et al., 1970). Дараа нь бусад полипептидүүдийг илрүүлсэн (Lazorowitz et al., 1971; Skehel, 1972; Klenk et al., 1972b; Krug, Etkind, 1973). Ерөнхийдөө бүх бүтцийн β-уургууд нь халдвар авсан эсүүдэд илэрсэн: нэг буюу хоёр Р-уураг, нуклеокапоидын дэд нэгж NP, мембраны уураг M, задралгүй (HA) болон хуваагдсан (HA1 ба HA2) хэлбэрийн гемагглютиниум гликопротейн, NA дэд нэгж. .
Вирионы уургуудаас гадна нэг буюу хоёр бүтцийн бус уураг (NS) гэж тодорхойлсон байдаг.
Мэдэгдэхүйц ялгаа бий<в уровнях синтеза отдельных вирусных полипептидов. NP- и NS-полипептиды обычно первыми обнаруживаются в зараженных «летках. Skehel (1973) предположил, что полипептиды Р2, NP и NS, которые первыми обнаруживаются в «клетках, зараженных ВЧП, являются
вирусын геномын гурван фрагментийн вирион полимеразаар сонгомол транскрипцийн явцад үүссэн РНХ-ийн хэсгүүдийн бүтээгдэхүүн. Циклогексимидын дэргэд эсүүд халдварлаж, антибиотикийг зайлуулсны дараа импульсийн тэмдэг нэмэхэд зөвхөн эдгээр гурван полипептид илэрсэн. Үүний үндсэн дээр эдгээр бүрэлдэхүүн хэсгүүдийн РНХ молекулууд нь анхдагч транскрипцийн явцад нэвтрүүлсэн вирион лолимеразын тусламжтайгаар үүссэн гэж үзсэн. ХПВ-тэй тахианы фибробласт халдвар авснаас хойш 4-6 цагийн хооронд М-уургийн нийлэгжилтийн түвшин нэмэгдэж, NS-лолилептидийн нийлэгжилт буурдаг (Skehel, 1972, 1973). Тиймээс иолипептидийн нийлэгжилтийн түвшинг дангаар нь хянах боломжтой бөгөөд өсөлтийн мөчлөгийн явцад өөр өөр байж болно.
HA полипептидийг HA1 ба HA2 болгон задлахаас гадна томуугийн томуугийн вирүсийн вирүсийн өвөрмөц полипептидүүдийг том прекурсоруудын задралын үр дүнд олж авсан гэсэн нотолгоо байхгүй байна (Taylor et al., 1969; Lazarowitz et al., 1971, Skehel, Skehel). , 1972; Кленк, Ротт, 1973).
Авторадиографи (Бехт, 1971) эсвэл эсийн фракц, гель электрофорезийн техник (Taylor нар, 1969, 1970) ашиглан халдвар авсан эсэд вирусын бүрэлдэхүүн хэсгүүдийг нутагшуулах талаар саяхан шинэ мэдээлэл олж авсан. Эдгээр судалгаагаар вирусын бүх уургийн нийлэгжилт нь цитоплазмд тохиолддог. Нуклеотидын эсрэгтөрөгчийг иммунофлуоресценцээр нутагшуулах тухай өмнөх судалгаанууд нь цөмд нийлэгжилт явагдаж, улмаар антиген нь цитоплазмд ялгардаг болохыг харуулж байна гэж тайлбарласан (Liu, 1955; Breitenfeld and Schafer, 1957; Holtermann et al., 1960). Гэсэн хэдий ч иммунофлуоресценци нь түүний синтезийг бус харин эсрэгтөрөгчийн хуримтлалыг тодорхойлдог нь тодорхой байна (IV, B, 2 хэсгийг үзнэ үү).
1. РНХ полимераз
Томуугийн вирүсээр халдварлагдсан эсүүдэд РНХ-аас хамааралтай РНХ полимеразагийн вирусын өвөрмөц идэвхжилийг ашиглаж буй эсийн системээс хамаарч халдвар авснаас хойш 13-3 цагийн хооронд илрүүлж болно (Scholtissek and Rott, 1969a; Skehel and Burke, 1969; Ruck et al. бусад, 1969; Махи, Бромли, 1970). Энэ нь халдварын дараа илрэх анхны вирусын өвөрмөц үйл ажиллагаа юм. Вирусын лолимеразын ихэнх үйл ажиллагаа нь микросомын фракцид илэрдэг; Энэ үйл ажиллагааны зарим хэсэг нь цөмд үлддэг бөгөөд үүнийг эрчимтэй угаахад ч арилгах боломжгүй юм. Цөмийн болон микросомын ферментүүдийн хоорондын илрэлийн кинетик эсвэл шаардлагатай кофакторуудад үндсэн ялгаа байхгүй (Scholtissek and Rott, 1969a; Mahy et al., 1975).
Калигуири ба Таммын (1970) аргыг ашиглан цитоплазмыг шаталсан сахарозын градиентээр хуваахад барзгар мембранд полимеразын идэвхжил илэрдэг (Compans and Caliguiri, 1973; Klenk et al., 1974a).
Вирусын полимеразын идэвхжил нь цэвэршүүлсэн вирүсийн хэсгүүдэд илэрсэн тул (5-р бүлгийг үзнэ үү) энэ нь вирусын уургийн аль нь байж болох вэ гэсэн асуулт гарч ирнэ.Томуугийн вирүсээр халдварласан эсээс тусгаарлагдсан полимеразыг ойролцоогоор 200 дахин цэвэршүүлсэн байна. Полимеразын идэвхжилтэй холбоотой цорын ганц вирусын өвөрмөц бүтээгдэхүүн нь RNP эсрэгтөрөгч (БЦГ-ын уураг ба вирусын vRNA, нэмэлтийг тогтоох аргаар тодорхойлсон) байв. Энэхүү цогцолбороос РНХ-г арилгах бүх оролдлого нь ферментийн үйл ажиллагааг бүрэн алдагдуулжээ (Schwarz and Scholtissek, 1973). P уураг нь вирусын полимеразын үүрэг гүйцэтгэх нэр дэвшигчээр тавигдсан (Kilbourne et al., 1972). Томуугийн вирүсээр халдварласан эсээс амин хүчлээр тэмдэглэсэн ферментийн цогцолборыг ялгаж, ойролцоогоор 35 дахин цэвэршүүлэхэд электрофорезийн шинжилгээгээр анх энэ цогцолбороос зөвхөн HP-белоа илэрсэн.< (Compans, Caliguiri, 1973). Впоследствии, однако, при других условиях введения;метки удалось обнаружить и Р-белок (Caliguiri, Compans, 1974). С другой стороны, Klenk и соавт. (1974) обнаружили Р-белок в цитоплазматическом золе, "который не обладает полимеразной активностью (Scholtissek, Rott, 1969a; Skehel, Burke, 1969). Эти наблюдения могут означать, что Р-белок осуществляет свою (Предполагаемую активность ферментов только при связывании с РНП-антигеном.
RNP антиген нь өөрөө полимеразын идэвхжилтэй байх магадлал багатай, учир нь RNP эсрэгтөрөгчийн эсрэг гипериммун ийлдэс нь полимеразын үйл ажиллагааг дарангуйлдаггүй, харин полимеразын эсрэгбие агуулсан эдгэрэлтийн ийлдэс нь идэвхждэг (Scholtissek et al., 1971). Энэхүү эдгэрэх ийлдэс нь (томуугийн А вирүсээр өвчилсөн малаас авсан) судлагдсан томуугийн А вирүсийн бүх омгийн полимеразын идэвхийг дарангуйлдаг боловч томуугийн В вирүсийн полимеразын идэвхийг дарангуйлдаггүй.Эдгээр бүх ажиглалт нь RNP- гэсэн санаатай нийцэж байна. антиген (BPHK + NP = уураг) нь cRNA-ийн синтезийн загвар болж чаддаг.
2. Нуклеокапсидын уураг
NP уураг нь вирусын РНХ-тэй холбогдож RNP эсрэгтөрөгчийг үүсгэдэг.Энэ нь зөвхөн вирионоос төдийгүй халдвартай эсээс тусгаарлагдсан NP уургийн хувьд ч үнэн юм (Schafer, 1957).“Үүнийг анх удаа илрүүлж болно. ийлдэс судлалын арга хэрэгсэл, хэзээ
халдварын дараа ойролцоогоор 3 цагийн дараа, гемагглютинин үүсэхээс нэг цагийн өмнө (Брейтенфельд, Шафер, 1957). Энэ хугацааны дараа RNP эсрэгтөрөгчийн титр мэдэгдэхүйц нэмэгдэхгүй. Энэ нь шинэ нийлэгжилт болон боловсорч гүйцсэн хэсгүүдэд нэгдэх хоорондын тэнцвэрт байдлаас болж үүсч болно. Тэмдэглэгээ хийснээр NP уураг "халдвар авснаас хойш 2 цагийн дотор халдвар авсан эсүүдэд илрэх боломжтой (Scholtissek and Rott, 1961; Krug, 1972).
Флюресцент эсрэгбиеийн тусламжтайгаар RNP эсрэгтөрөгчийг эхлээд бөөмөөс илрүүлдэг. Хожим нь цитоплазмд гарч ирдэг (Breitenfeld and Schafer, 1957). Үр хөндөлтийн халдвар (Франклин, Бритенфельд, 1959), р-фторфенилаланин (Zimmermann, Schafer, 1960), эсвэл фон Магнус үзэгдлийн нөхцөлд (Rott, Scholtissek, 1963), RNP -antigen зэрэг тодорхой нөхцөлд. цөмд үлддэг.
Халдвар авсан эсийн цөмд RNP антиген эрт хуримтлагдсан нь NP уураг мөн бөөм дотор нийлэгждэг гэсэн үг биш юм. Авторадиографийн судалгаа, эсийг хуваах аргыг ашиглах нь энэ болон өөр нэг аргининаар баялаг уургийн цитоплазмын нийлэгжилт, тэдгээрийг цитоплазмаас цөм рүү хурдан зөөвөрлөж байгааг харуулж байна (Taylor et al., 1969, 1970; Becht, 1971).
Халдвар авсан эсийн ханданд RNP эсрэгтөрөгчийн тодорхой хэсэг нь vRNA агуулдаг (Pons, 1971; Krug, 1972; Krug, Etkind, 1973), гэхдээ вирусын хэсгүүдэд зөвхөн нэг төрлийн РНХ байдаг (энэ нь ямар ч байхгүйгээс үүсдэг). vRNA-ийн өөрөө эрлийзжих) (Scholtissek, Rott, 1971; Pons, 1971). cfRNA агуулсан RNP антиген нь вирусын тархалтын үйл явцад тодорхой үүрэг гүйцэтгэдэг эсэх, эсхүл эсийн хуваагдлын явцад гарч ирдэг олдвор уу гэдгийг шийдэх боломжгүй юм. РНХ-ийн хэлхээ хоёулаа in vitro NP уурагтай адилхан сайн холбогддог болохыг харуулсан (Scholtissek and Becht, 1971). Тиймээс хэрэв чөлөөт NP уураг болон чөлөөт cRNA байгаа бол нэгэн төрлийн болгох процессын явцад харгалзах RNP эсрэгтөрөгч нэн даруй үүсдэг. Вирионы РНХ-ийг RNP эсрэгтөрөгчөөс поливин "Илсульфат" M (Pons et al., 1969) -ээр нүүлгэн шилжүүлж болно. Тиймээс RNP антиген дэх өөр өөр вирусын РНХ-ийг солих нь эсийн гомогенатуудад боломжтой эсэхийг шалгаж болно. Цитоплазмын RNP эсрэгтөрөгчөөс тусгаарлагдсан вирусын РНХ-ийн суурь найрлагад янз бүрийн хугацаанд 32P тэмдэглэгдсэн өөрчлөлтөөс үзэхэд Круг (1972) cfRNA-ийн зарим нь RNP эсрэгтөрөгчтэй нэгдэхээс өмнө чөлөөт хэлбэрээр байдаг гэж дүгнэжээ. NP-аас хэрэм. Амьтны цэврүүтрийн РНХ-д 32P-ийг оруулах нь нуклеозидын трифосфатын х байрлалд шошготой фосфорыг нэлээд удаан оруулдагтай холбоотойгоор ихээхэн хоцрогдолтой явагддаг (Шолтиссек, 1965) Найрлагын өөрчлөлтийг тооцоолоход зохих тохируулга хийх хүртэл.
ямар ч үндэслэл тогтоогдоогүй тул Круг (1972)-ийн өгөгдлийг болгоомжтой тайлбарлах хэрэгтэй.
Круг (1972) хийсэн "Цөм болон цитоплазмд RNP эсрэгтөрөгчийн харагдах байдал"-ын кинетик шинжилгээ нь цөмд хуримтлагдаж буй RNP эсрэгтөрөгч нь цитоплазмд байдаг RNP эсрэгтөрөгчийн урьдал зүйл биш гэдгийг харуулж байна.
3. Бүтцийн бус уураг
Халдвар авсан эсүүдэд үл мэдэгдэх функцтэй хэд хэдэн бүтцийн бус вирусын өвөрмөц уургийг тодорхойлсон байдаг. Тэдгээрийн нэг нь харьцангуй молекул жинтэй 25000, их хэмжээгээр хуримтлагддаг, NS гэж томилогдсон (Lazarowitz et al., 1971) Полиакриламид гель нь М уургийн хөдөлгөөнтэй ойролцоо шилжилт хөдөлгөөнтэй байдаг. уураг хоёулаа бие биенээсээ хамааралгүй мэт харагддаг нь тэдний пептидийн зураглалын ялгаанаас харагдаж байна.Их хэмжээний NS уураг цөмд агуулагддаг (Lazarowitz et al., 1971; Krug, Etkind, 1973) Энэхүү мэдээлэл. Энэ нь Дим-мок (1969)-ын хийсэн иммунофлуоресценцийн судалгааны өмнөх өгөгдөлтэй нийцэж байгаа бөгөөд тэрээр "Бүтцийн бус вирусын эсрэгтөрөгчийн эсрэг ийлдэс бүхий цөмийг тод будсан" гэж ажигласан бөгөөд энэ будалт нь NS уураг байгааг илтгэж магадгүй юм. халдвартай эсээс тусгаарлагдсан чөлөөт ба мембрантай холбоотой рибосомын фракц дахь вирусын өвөрмөц уураг байх болно (Pons, 1972; Compans, 1973; Klenk et al., 1974a). NS-ийн рибосомтой холбоо нь дууны хүчнээс хамаардаг бололтой (Круг ба Эткинд, 1973). Ионы хүч багатай буферт ЭНЭ нолипаптид нь рибосомын хоёр дэд хэсэгт шингэж, харин давс нэмснээр тэдгээрээс салгагдсан.
Саяхны судалгаагаар (Грегориадес, 1973) NS-ийг вирион полипептид М-ээс ялгаатай бүтцийн бус полипептид гэж тодорхойлоход эргэлзээ төрүүлэв. Вирионоос М-полипептидийг хүчиллэг хлороформметанол болон уурагаар гаргаж авах боломжтой болсон. ижил электрофорезын хөдөлгөөнөөр халдвар авсан бүхэл эс, цөм эсвэл полисомоос гаргаж авах боломжтой.М уураг, түүнчлэн цөмийн болон рибосомтой холбоотой уургуудын триптик боловсруулалтын бүтээгдэхүүнд хийсэн шинжилгээ нь M болон NS уургууд нь адилхан боловч эдгээр үр дүнгийн талаар үнэмшилтэй тайлбар өгөхийн тулд нэмэлт мэдээлэл шаардлагатай.
NS-ээс гадна вирусын өвөрмөц бус бүтцийн бүрэлдэхүүн хэсгүүд байж болох ч тэдгээрийн аль нь ч байхгүй. хангалттай тодорхойлогдоогүй байна. Бүтцийн бус вирусын эсрэгтөрөгчийн эсрэг чиглэсэн антисерум хэрэглэх;
Диммок ба Ватсон (1969) халдвар авсан эсүүдээс цацрагийн шошготой полипептидүүдийг тунадасжуулсан. Полиакриламидын гель дэх электрофорезийн шинжилгээ нь NS-д тохирох үндсэн бүрэлдэхүүн хэсэг бүхий хэд хэдэн бүтцийн бус полипептид байгааг харуулж байна. Үлдсэн бүтцийн бус бүрэлдэхүүн хэсгүүдийн нэг нь илүү хурдан шилжиж, Skehel (1972) болон Krug and Etkind (1973) нарын тодорхойлсон 10,000-15,000 молекул жингийн бүрэлдэхүүн хэсэгтэй тохирч болно.
4. Мембран М уураг
Дугтуйны липидийн давхар давхаргын дотоод гадаргууг бүрхэж, вирионоор баялаг М уураг нь халдвар авсан эсүүдэд харьцангуй бага хэмжээгээр агуулагддаг.Энэ нь М уургийн нийлэгжилтийг хянах боломжтойг харуулж байгаа төдийгүй энэ нь синтез нь вирусын нөхөн үржихүйн хурдыг хязгаарлах үе шат юм (Lazarowitz et al., 1971) Энэхүү үзэл баримтлал нь 29 хэмийн температурт вирусын үйлдвэрлэл дарангуйлагдах үед М уураг нь зөвхөн вирусын өвөрмөц шинж чанартай байдаг гэсэн мэдээлэлд тулгуурладаг. халдвартай эсэд илрэхгүй уураг (Klenk, Rott, 1973).
М уураг (халдвартай эсийн гөлгөр ба плазмын мембранаас олж болно (Lazarowitz et al., 1971; Cornpans, 1973a; Klenk et al., 1974a). Эдгээр өгөгдөл нь энэ уургийн мембрантай холбоотой болохыг харуулж байна.
5. Гемагглютинин
Гемагглютинин нь том гликопротейн хэлбэрээр нийлэгждэг - HA-ийн урьдал үүсгэгч бөгөөд дараа нь HAi ба HA2 гэсэн хоёр жижиг гликопротейнд хуваагддаг (Lazarowitz нар, 1971). Протеазын дарангуйлагчид дарангуйлдаг хуваагдлыг (Klenk17, Rott13) ), эзэн эсийн протеолитик ферментээр явагддаг (Lazarowitz et al., 1973). Хагарлын зэрэг нь вирусын омог, эзэн эсийн хэмжээ, цитотоксик нөлөөний түвшин, байгаа эсэхээс хамаарна. дунд дахь ийлдэс (Lazarowitz et al., 1971, 1973a, b; Klenk, Rott, 1973; Stanley et al., 1973) Тиймээс дэгдээхэйний үр хөврөлийн фибробластын өсгөвөрт ургуулсан WSN нь зөвхөн задарсан гемагглютнин гялалзсан уураг агуулдаг. Хэрэв байхгүй ийлдэс дэх MDBK эсүүдэд WSN вирионууд ургасан бол хуваагдал бараг байхгүй болно.Гэвч ийлдэс байгаа тохиолдолд WSN гемагглютинин мөн хуваагдана.Үүнд хуваагдана.
систем нь плазмын мембран дээр явагддаг (Lazaro-witz et al., 1973a). VChP системд ийм хуваагдлын механизм нь өөр өөр байдаг. Хагарал "эсийн доторх мембранд үүсдэг бөгөөд энэ тохиолдолд плазминоген шаардлагагүй (Shchepk et al., 1974a). Хагалах зэрэг нь 25 ° C-д огцом буурдаг (Klenk and Rott, 1973).
HA-ийн задрал нь гемагглютинжуулах үйл ажиллагаа эсвэл вирион угсралтад тавигдах шаардлага биш (La-zarowitz et al., 1973a; Stanley et al., 1973), гэхдээ сүүлийн үеийн судалгаагаар энэ нь халдварт өвчин үүсгэхэд шаардлагатай болохыг тогтоосон (Klenk et al., 1975b). Эдгээр өгөгдлүүд нь шингээх үүргээс гадна HA* нь халдварын процесст өөр үүрэг гүйцэтгэдэг бөгөөд энэ үйл ажиллагаанд задрал зайлшгүй шаардлагатай гэсэн таамаглалтай нийцэж байна.Үндэслэн HA-ийн задрал нь " эзэн эсээс хамааралтай үзэгдэл юм" , мөн задлагдаагүй HA агуулсан тоосонцор нь бага халдвартай байдаг нь томуугийн вирүсийн халдварын тархалт, тархалт нь идэвхжүүлэгч фермент болох хост эсийн протеазаас хамаардаг болохыг харуулж байна.
“Vi-ээр халдварласан летлетүүдийг хуваах туршилтанд
Оросын томуугийн үед HA гликопротеинууд үргэлж байдаг нь тогтоогдсон
мембрантай холбоотой байдаг (Compans, 1973a; Klenk et al.,
1974a). Эдгээр уургийн эсийн доторх нутагшуулалт ба тэдгээрийн мөч
барзгар мембранаас гөлгөр эндоплазмын мембран хүртэл walkie-talkie
тэнгэрийн торлог бүрхэвч болон плазмын мембранууд нь де болно
VII, В хэсэгт дэлгэрэнгүй тайлбарласан болно. .,
6. Нейраминидаза
Идэвхтэй фермент болох вирусын NA* илэрсэн
Chorionic allantoic мембранд халдвар авснаас хойш 3 цагийн дараа
нах бөгөөд экстраполяциар түүний син эхлэл болох нь тогтоогдсон
халдварын дараа 1-2 цагийн дараа диссертаци үүсдэг (Noll et al.,
1961). NA*-ийн эсийн доторх локалчлалыг ашиглан судалсан
дараа нь эсийн хуваагдал, тэр нь бололтой гэдгийг олж мэдсэн
mu, HA*-ийн нутагшуулалттай төстэй (Compans, 1973a; Klenk et al.,
1974a). NA* нь мембрантай холбоотой байдаг.
гөлгөр эндоплазмын торлог бүрхэвчээс олж авсан;
биологийн идэвхжил, шинжилгээгээр тодорхойлохдоо
полиажриламидын гель дэх зу. Ферментийн идэвхжил өндөр байсан
дена мөн барзгар мембран агуулсан фракцуудад
бид. Эдгээр өгөгдөл нь олж авсан өгөгдөлтэй нийцэж байна
иммунофлуоресценц (Maeno, Kilbourne, 1970). 4 цагийн дараа
халдварын дараа цитоплазмд нейраминидазыг илрүүлж болно
плазм; Дараа нь тэр пери дээр анхаарлаа төвлөрүүлдэг бололтой
эсийн фериа.
V. НҮҮРС СУУРЫН НИЙГВЭЛ
Нүүрс ус нь томуугийн вирүсийн бүрхүүлийн гликопротейн ба гликолид үүсэхэд оролцдог (Klenk et al., 1972a). Миксовирусын гликолипидүүд (эзэмшигч эсийн сийвэнгийн мембранаас гаралтай (Кленк, Чоппин, 1970), гэхдээ вирионын аль нь голчлон агуулагддаг нь тогтоогдоогүй байна: урьд өмнө нь байгаа эсвэл шинээр нийлэгжсэн гликолипидүүд.
Глюкозамин, манноз, галактоз, фукоз зэрэг цацраг идэвхит прекурсоруудыг вирусын глюкопелтидэд тусгайлан оруулснаар эдгээр гликопептидийн нүүрс усны хажуугийн хэлхээ нь халдварын үед дахин нийлэгждэг болохыг харуулсан (Haslam et al., 1970; Cornpans et al., 1970a; Шварц ба Кленк, 1974). Эсийн фракцын туршилтууд нь вирусын гликопротеины гликозиляцийн байршлын талаар нэмэлт мэдээлэл өгсөн.Глюкозамин нь цитоплазмын гөлгөр ба барзгар хэсгүүдийн аль алинд нь HA полипептидтэй холбоотой байдаг ч фукоз нь гөлгөр боловч барзгар биш мембраны HA-тай холбоотой байдаг (Compans, 1973b). .Пуромицинтэй уургийн нийлэгжилтийг дарах нь глюкозаминыг нэгтгэхийг бараг тэр даруй зогсоодог бол фукоз нь ойролцоогоор 10-15 минутын турш үргэлжилдэг (Stanley et al., 1973). Эцэст нь, FPV-д гликопротейн нь HA болон задралын урьдал юм. HAj-ийн бүтээгдэхүүн<и НА2 содержат, по-видимому, полный состав маннозы « глюкозамина, тогда как содержание фукозы и галактозы значительно выше в продуктах расщепления (Klenk et al., 1975a; Schwarz, Klenk, 1974). Эта наблюдения предполагают, что биосинтез углеводных боковых целей гликопротеинов НА осуществляется по стадиям с различными остатками Сахаров, добавляемыми в разных участках клетки. Глюкозамин и манноза (присоединяются, по-видимому, к полипептидам НА на шероховатых мембранах вскоре после или даже в процессе синтеза поляпептида, в то время как фукоза, вероятно, прикрепляется позже с помощью трансфераз, присутствующих в гладких мембранах.
Эдгээр гликозилтрансферазууд нь эсийн ферментүүд байж магадгүй юм. Тиймээс нүүрс ус (гликопротеины нэг хэсэг нь эзэн эсээр тодорхойлогддог бололтой. Гэсэн хэдий ч эдгээр эзэн эсийн ферментүүдээс гадна вирүсийн NA* нүүрсустөрөгчийн хажуугийн гинж үүсэхэд чухал үүрэг гүйцэтгэдэг гэсэн нотолгоо байдаг. Мицеовирусын бүрхүүлийн гадаргууд нейроминий хүчил дутагдаж байгааг тогтоосон (Кленк, Чоппин, 1970b; Klenk нар, 1970), харин энэ фермент агуулаагүй вирусын бүрхүүлд ийм нүүрс ус нь нийтлэг бүрэлдэхүүн хэсэг болдог (Klenk, Choppin, 1971). ; McSharry, Wagner, 1971; Renkonen et al., 1971) Эдгээр өгөгдөл нь
Нейрамин хүчлийн нөлөө нь миксовирусын зайлшгүй шинж чанар юм. NA* нь томуугийн вирүсийн бүрхүүлээс нейромины хүчлийг зайлуулах үүрэгтэй бөгөөд ингэснээр вирусын дугтуйнд рецептор үүсэхээс сэргийлж, вирусын бөөмсийн том бөөгнөрөл үүсэхээс сэргийлдэг болохыг саяхан харуулсан (Palese et al., 1974). Эдгээр өгөгдөл нь үндсэн гадаргуугийн гликопротейн болох NA*-ийн нүүрсустөрөгчийн хэсэг нь (Үүрэн трансфераза ба вирусийн NA*-ийн хосолсон үйл ажиллагааны бүтээгдэхүүн юм гэсэн ойлголтыг баталж байна. Түүний үйл ажиллагааны ачаар вирус нь вирусыг нэвтрүүлэх чадвартай байдаг. өвөрмөц өөрчлөлт (Эхэндээ, нүүрс усны өөрчлөлт нь эзэн өвөрмөц, цогц бүтэц, -ийн дагуу - бололтой вирусын биологийн идэвхжилд зайлшгүй шаардлагатай.
D-глюкозамин ба 2-деокси-О-глюкоз нь биологийн идэвхит HA*, NA* болон халдварт вирус үүсэхийг саатуулдаг (Kilbourne, 1959; Kaluza et al., 1972). Биохимийн судалгаагаар эдгээр сахар нь вирусын гликопротеины биосинтезтэй өрсөлддөг болохыг тогтоосон (Ghandi et al., 1972; Klenk et al., 1972b). Эдгээр дарангуйлагчтай үед гликопротейн NA-ийн хэмжээ багасна.Багарах зэрэг нь тунгаас хамаарна.Иймд сахарын концентраци ихсэх тусам харьцангуй молекул жинтэй 76000 гликопротейн НА аажмаар нэгдэл болж хувирдаг. молекулын жин 64,000 байсан бөгөөд үүнийг HA0 гэж тодорхойлсон (Klenk нар, 1972b; Schwarz and Klenk, 1974). Молекулын жингийн өөрчлөлт нь нүүрс усны агууламж буурахтай зэрэгцэж байгаа бөгөөд HA0 уураг нь нүүрс усгүй бараг л илэрсэн байна (Шварц). болон Klenk, 1974).Эдгээр үр дүн нь HA0 нь HA гликопротеины бүрэн бус гликозилжсэн эсвэл "гликозилжсэн полипептидийн гинж бөгөөд D-глюкозын амин а ба 2-деокси-О-глюкозын дарангуйлах нөлөө нь гликозилжилтийн гэмтэлтэй холбоотой болохыг харуулж байна. HA0 полипептид нь ердийн HA шиг мембрантай холбоотой. Мөн барзгар хэсгээс гөлгөр торлог бүрхэвч рүү шилжиж, HA01 ба HA02 полипептидүүдэд хуваагддаг.Иймээс нүүрс ус нь мембрантай энэ полипептидийн ойр дотно байдлыг хангахад чухал биш юм. Гэсэн хэдий ч халдвар авсан эсэд гемагглютинжуулах үйл ажиллагаа байхгүй байгаа нь гликозилээгүй уураг нь рецепторуудтай холбогдож чадахгүй байгааг харуулж байна.
VI. ЛИПИДИЙН СИНТЕЗ
Бүх бүрхүүлтэй вирусын нэгэн адил томуугийн вирус нь эзэн эсийн липидийг дахин боловсруулах замаар липидээ олж авдаг. Энэ байр суурийг дараах ажиглалтууд баталж байна.
Дениа. Томуугийн вирүсийн липидийн найрлага нь эзэн эсийнхтэй төстэй болохыг тогтоожээ (Ambruster and Beiss, 1958; Frommhagen et al., 1959). Халдвар авахаас өмнө цацраг идэвхт байдлаар тэмдэглэсэн хост эсийн липидүүд нь вирусийн тоосонцоруудад нэгддэг (Wecker, 1957). Вирусыг янз бүрийн хост эсүүдэд ургуулах үед вирусын липидийн өөрчлөлтийг илрүүлдэг (Kates et al., 1961, 1962). Ерөнхийдөө вирусын липидүүд (эсийн гадаргуугаас нахиалах нь эзэн эсийн плазмын мембраны липидийн найрлагыг нарийн тусгадаг (Klenk, Choppin, 1969; 1970a, b; Renko-nen et al., 1971). Дэгдээхэйний үр хөврөлийн фибробласт эсүүд дэх ф-осфолилидын де ново синтезийн түвшин томуугийн вирүсийн халдвараас хойш 7 цагийн турш өөрчлөгдөөгүй бөгөөд үүний дараа бүх липидийн нийлэгжилт дарагдсан (Blough et al., 1973). РНХ эсвэл уургийн нийлэгжилтийг дарангуйлах эсвэл “биологийн бусад нөлөөлөлтэй холбоотой хоёрдогч.
Тиймээс өнөөг хүртэл олж авсан үр дүнд үндэслэн вирусын липидийн нийлэгжилт нь эсийн липидийн биосинтезийн хэвийн үйл явцаар явагддаг бөгөөд вирусын бүрхүүл нь эзэн эсийн плазмын мембранаас липидүүдийг нэгтгэснээр үүсдэг гэж үзэж болно.
VII. УГСРАЛТ (мөн 2-р бүлгийг үзнэ үү)
A. НУКЛЕОКАПСИД ҮҮСЭХ
Өмнө дурьдсанчлан нуклеокапсидын уураг цитоплазмд нийлэгждэг байх магадлалтай. Энэ нь тэнд богино хугацаанд чөлөөт хэлбэрээр оршдог бөгөөд дараа нь вирусын РНХ-тэй холбогдож нуклеокапсид үүсгэдэг (Klenk et al., 1974; Compans and Caliguiri, 1973). NP уураг нь яуклеокапсид хурдан шингэдэг тул шинэчлэгдсэн сангаас РНХ-ийг сонгож болно (Krug, 1972). Томуугийн вирүсийн нуклеокапсидын хэмжээ бага учир халдвар авсан эсүүдэд электрон микроскоп ашиглан нарийн тодорхойлох боломжгүй. Цитоплазмд ажиглагдсан 5 нм диаметртэй утас эсвэл утаснуудын бөөгнөрөл нь вирусын рибонуклеопротеиныг төлөөлдөг (Апостолов нар, 1970; Компанс нар, 1970b).
Томуугийн вирусын вирионуудын РНХ-ийн геном нь 5-7 фрагментээс бүрддэг (6-р бүлгийг үзнэ үү).
Тиймээс аливаа халдварт тоосонцор нь фрагмент бүрийн дор хаяж нэг хуулбарыг шаарддаг. Хирст (1962) өмнөх
эсийн доторх цөөрмийн нуклеокапсидыг (вирионууд санамсаргүй байдлаар. Дундаж вирионд нэмэлт РНХ-ийн хэлтэрхий оруулах замаар Е популяци дахь халдварт вирионуудын эзлэх хувийг нэмэгдүүлэх боломжтой) (Compans et al., 1970). Жишээ нь, хэрэв таван Халдвартай өөр өөр РНХ-ийн хэсгүүдэд шаардлагатай байдаг бөгөөд вирной бүр нь вирнойд санамсаргүй байдлаар орсон нийт 7 фрагментийг агуулдаг бөгөөд вирионуудын ойролцоогоор 22% нь халдвартай байх ёстой. РНХ-ийн хэсгүүдийг санамсаргүй байдлаар оруулсан нотлох баримтыг Хирст сүүлийн үеийн ажиглалтаар бэхжүүлсэн. 1973) вирусын популяцид товруу үүсгэдэггүй хэсгүүдийн хооронд рекомбинац үүсдэг. Ийм бөөмсийн рекомбинацад оролцох чадварыг бөөмсүүдэд нэг буюу хэд хэдэн хэлтэрхий байхгүй, дутуу фрагментүүд нь нэг бөөмсөөс өөр өөр байдагтай холбон тайлбарлаж болно. нөгөө рүү, ингэснээр согогтой вирусын тохиромжтой хэсгүүд нь рекомбинант үүсгэдэг.
B. ВИРУС НЭГДЭХ ПРОЦЕСС
Ихэнх бүрхүүлтэй вирүсийн нэгэн адил томуугийн вирүс нь урьдчилан бүрдсэн эсийн мембран дээр цуглардаг; угсралт нь плазмын мембранаас нахиалах замаар үүсдэг. Лизисгүй процессоор эсээс вирус ялгардаг анхны жишээг Мерфи, Бэнг (1952) нар томуугийн вирүсээр халдварласан эсийг электрон микроскопоор хийсэн анхны судалгаанд гаргажээ.Судаслаг ба ■ бөөрөнхий бүтэц. Халдварт вирус үүсэх үед эсийн дотор вирусын тоосонцор харагдахгүй байсан тул вирусын тоосонцор эсийн гадаргуу дээр үүсч байгаа нь тодорхой байсан.Ферритинээр тэмдэглэгдсэн эсрэгбиемүүдийг ашиглан Морган нар (1961) эсийн гадаргууд вирус агуулагдаж байгааг ажигласан. вирус үүссэн хэсгүүдэд антиген.Сүүлийн электрон микроскопийн судалгаагаар нахиалж буй вирүсийн гадаргуу нь гаднах гадаргуу дээрх вирусын "баяжуулалт"-д тохирсон проекцын давхарга бүхий эзэн эсийн ижил мембраныг агуулдаг болохыг харуулсан.Дотоод Вирусын мембраны гадаргуу дээр эсийн гадаргуу дээр байхгүй нэмэлт электрон нягт давхарга байдаг бөгөөд энэ нь М-олипептидүүдээс бүрддэг (Bachi et al., 1969; Compans, Dimmock, 1969; Apostolov et al., 1970).
Электрон микроскопын судалгаагаар вирусын бүрэлдэхүүн хэсгүүдийн дарааллыг санал болгох үндэслэлийг өгсөн.
эсийн мембран дээр холбогддог (Бачи нар, 1961; Компанс ба Диммок, 1969; Компанс нар, 1970б).
Вирусын дугтуйны уураг нь хэвийн морфологитой байх ёстой мембраны зарим хэсэгт орсон байдаг; гэхдээ мембраны эдгээр хэсгүүдэд эритроцитуудын өвөрмөц шингээлт ажиглагдаж байгаа нь энд HA уураг байгааг харуулж байна. Дараа нь М уураг нь мембраны ийм хэсгүүдийн дотоод гадаргуутай холбогдож электрон нягт давхарга үүсгэдэг.Дараа нь рибонуклеопротейн нь эдгээр хэсгүүдийн мембрантай тусгайлан холбогдож, мембраныг нугалж, цухуйх замаар нахиалах процесс явагддаг. сегмент болон холбогдох рибонуклеопротеины эргэн тойронд. Полиакриламидын гель электрофорезийн өгөгдөл нь дугтуйны уураг нь RNP-ээс илүү хурдан плазмын мембрантай холбогддог гэсэн санааг дэмждэг (Lazarowitz et al., 1971). Ийм полипептид нь цэвэршүүлсэн вирионуудад байдаггүй тул вирусын дугтуйнд байдаг. Өмнө дурьдсанчлан нейрамин хүчлийн үлдэгдэл нь томуугийн вирүсийн нахиалах хэсгүүдийн дугтуйнд байхгүй боловч эсийн мембраны зэргэлдээ хэсгүүдэд байдаг (Klenk et al., 1970) .
Эдгээр өгөгдлүүд нь нахиалж буй вирусын тоосонцор болон зэргэлдээх эсийн мембраны хооронд химийн найрлагад огцом шилжилт хийснийг нотолж байна.
Гэсэн хэдий ч нөгөө талаас, нахиалах үйл явцын нэг чухал шинж чанар нь вирусын бүрхүүл нь эзэн эсийн плазмын мембрантай үргэлжилдэг бөгөөд морфологийн хувьд түүнтэй төстэй байдаг (Compans and Dimmock, 1969). Дээр дурдсанчлан эдгээр мембран дахь липидүүд нь эзэн эсийн мембраны липидүүдтэй маш төстэй байдаг. Эдгээр ажиглалтууд нь бүрэн бүтэн плазмын мембран дахь липидүүд нь радиаль тархалтаар нахиалах вирусын тоосонцор дахь липидүүдтэй амархан солилцдог болохыг харуулж байна.
Үүний үр дүнд нахиалах вирионы дугтуй нь вирион бүрхүүлийн уургийг оруулснаар өөрчлөгдсөн эсийн мембраны жижиг хэсгээс үүсдэг. Мэдээжийн хэрэг, энэ ойлголт нь плазмын мембран дээр мембраны бүх бүрэлдэхүүн хэсгүүдийг нэгтгэх шаардлагатай гэсэн үг биш юм.
Үнэн хэрэгтээ мембраны бүрэлдэхүүн хэсгүүд биосинтезийн талбайгаас мембран угсралтын газар руу очихын тулд эсийн нэг хэсгээс нөгөө рүү нэлээд зайд шилжих ёстой гэдгийг эрт дээр үеэс мэддэг байсан. Breitenield and Schafer (1957) томуугийн вирүсээр халдварласан эсүүдэд HA* анх илэрч болохыг харуулсан.
эсийн бүх хэсэгт тохиолддог бөгөөд энэ нь ихэссэн концентрацитай перинуклеар бүсэд байршдаг. Хожим нь HA* нь галын "захын бүс" -д хуримтлагддаг бөгөөд мөн дөлийн мембранаас цухуйсан нимгэн утаснуудад илэрч болно.
Дугтуйны бүрдэл хэсгүүд нь эсийн дотроос гадаргуу руу шилждэг гэсэн санаа нь эсийн хуваагдал, эсийн өөр өөр фракц дахь вирусын уургийн шинжилгээг ашиглан хэд хэдэн судалгаагаар батлагдсан бөгөөд өргөжсөн. Эдгээр судалгаагаар HA гликопротейн, магадгүй бусад бүрхүүлийн уургууд нь барзгар эндоплазмын торлог бүрхэвч дээр нийлэгждэг болохыг харуулж байна (Compans, 1973a; Klenk et al., 1974). Пульс хөөх туршилтаас харахад хэдхэн минутын дараа ГА нь гөлгөр эндоплазмын торлог бүрхэвч (Compans, 1973a; Stanley нар, 1973; Klenk et al., 1974) болон плазмын мембранаас (Stanley et al., 1974) олддог. бусад, 1974). ., 1973). Гөлгөр эндоплазмын торлог бүрхэвчээс плазмын мембран руу хөөх туршилт хийгдээгүй ч ХА нь барзгар эндоплазмын торлог бүрхэвчээс плазмын мембран руу шилжиж, гөлгөр эндоплазмын торлог бүрхэвчийг тойрч гардаг нь үнэмшилтэй юм шиг санагдаж байна. Ийм шилжилтийн бүх хугацаанд HA болон бусад мембраны уураг нь тэдгээрийн дагуу хөдөлдөг мембрануудын салшгүй хэсэг гэдгийг тэмдэглэх нь зүйтэй; OBI нь ууссан уураг хэлбэрээр хэзээ ч олддоггүй.
Гол төлөв эндоплазмын торлог бүрхэвчээс гаралтай гэж үздэг гөлгөр мембраны хэсгүүдэд бүх гол бүрхүүлийн уургууд байдаг (Compans 1973a; Klenk et al., 1974). Гэсэн хэдий ч тэдгээрийн харьцангуй хэмжээ нь плазмын мембран ба вирион дахь хэмжээнээс ялгаатай (Stanley et al., 1973; Klenk et al., 1974). М уураг ба гликопротейн HA-ийн харьцаа нь эндоплазмын торлог бүрхэвчтэй харьцуулахад боловсорч гүйцсэн вирионы дугтуйнд өндөр байдаг. Эдгээр өгөгдөл нь зөвхөн HA гликопротейн агуулсан мембраны багахан хэсгийг вирусын бүрхүүлд, тухайлбал нүүрс усгүй уураг агуулсан мембраны фракцуудад хувирдаг болохыг харуулж байна. Өмнө дурьдсанчлан, M уургийн нийлэгжилт нь вирусын угсралтын үйл явцыг хязгаарлах үе шат байж болно.
Төрөл бүрийн дугтуйны уургийн нийлэгжилтийн хурдны ялгаа нь дугтуйг угсрах нь олон үе шаттай үйл явц гэсэн таамаглалыг баталж байна.Энэ ойлголт нь нүүрсустөрөгчийн хэсэг болон нүүрсустөрөгчийн хэсгийг дараалан нэмэх зэрэг HA* үүсэх үйл явцын асуудалтай нийцэж байна. анхдагч генийн бүтээгдэхүүнийг шилжүүлэх явцад уураг задлах задрал.
VIII. ХАМУУНУУДЫН ВИРУС ГАРСАН
Томуугийн вирусыг эзэн эсээс ялгаруулах асуудал,
вирусын үйл ажиллагааны асуудалтай нягт холбоотой юм шиг харагдаж байна
Өмнө нь нарийвчлан авч үзсэн NA * (харна уу
тохиолдол V ба ch. 4). Энэ фермент чухал үүрэг гүйцэтгэдэг
эсрэг чадвараас үүдэлтэй вирусыг ялгаруулах үүрэг
NA*-ийн өвөрмөц бие нь ийм ялгаралтыг дарангуйлдаг (Se-
Ротт, 1966; Вебстер нар. G968). Түүнээс гадна ийм эсрэгбие
эритроцитоос вирус ялгарахаас сэргийлнэ (Браун, Лавер,
1968). Бактерийн NA*, эсрэгбиемүүд дарангуйлдаггүй
лами нь вируст NA*, эсээс вирусыг ялгаруулах чадвартай,
ийм эсрэгбиемүүдээр эмчилсэн (Compans et al., 1969;
Вебстер, 1970). Нөгөө талаас, хоёр валент эсрэгбие
to NA нь мөн вирусын бөөгнөрөлийг үүсгэдэг (Seto and Chang, 1969;
Compans et al., 1969; Webster, 1970) ба моновалент эсрэг
бие махбодь нь вирусыг дарангуйлдаг хэдий ч ялгарахаас сэргийлдэггүй
нейраминидазын үйл ажиллагааны 90 гаруй хувь (Becht et al., 1971).
Эдгээр бүх тоо баримтыг нэгтгэсэн нь үүнийг харуулж байна
Хоёр валентын эсрэгбие нь вирусыг ялгаруулахад саад болдог
дээр байгаа эсрэгтөрөгчтэй холбох замаар
эсийн гадаргуу, ферментийн үйл ажиллагааг саатуулах замаар
цагдаа. Дэлгэцийн вирусыг ялгаруулахад нейраминидазын үүрэг
эсвэл Palese et al. (G974), хэн энэ fer гэдгийг тогтоосон
VI-аас нейроамилийн хүчлийг зайлуулахад шаардлагатай
Вирионыг нэгтгэхээс зайлсхийхийн тулд Оросын гадаргуу - дараа нь -
kov эсийн гадаргуу дээр.
IX. НӨХӨН ҮРЖИХИЙН Хэвийн бус хэлбэрүүд
A. ЭЗЭГДСЭН ЭСЭЭС ХАМААРАЛ АЖИЛ АВСАН НӨХӨЛТ
Томуугийн вирус нь олон төрлийн эзэн эсийг халдварладаг. Гэсэн хэдий ч халдвар авсан олон эсүүдэд халдварт үр хөврөлийн гарц маш бага буюу илрэх боломжгүй байдаг ч вирусын бүрэлдэхүүн хэсгүүдийг хэвийн титрээр илрүүлдэг.Халдварын мөчлөгийн эзэн эсээс хамааралтай ийм төрлийн тасалдлыг үр хөндөлтийн халдвар гэж нэрлэдэг. халдварт циклийг анх томуугийн вирүсийн нейротроп бус омгуудаар тархинд халдварласан хулгануудад ажиглагдсан (Шлесингер, 1953). Вирусын тун өндөр байх тусам шинээр нийлэгжсэн гемагглютинины хэмжээ ихэсдэг. Бусад хэд хэдэн хост эсүүд- Томуугийн А вирүсийн системийг зөвхөн RNP-^ антиген ба гемагглютинин үйлдвэрлэсэн боловч халдварт вирүс биш гэдгийг тодорхойлсон.Одоогоор судлагдсан эдгээр бүх чих хамар хоолойн системд RNP эсрэгтөрөгч цөмд хуримтлагдсан бөгөөд илрээгүй байна.
цитоплазм дахь флюресцент эсрэгбиемүүдийн тусламжтайгаар зэвсэглэсэн (Henle et al., 1955; Franklin, Breitenfeld, 1959; Ter Meulen, Love, 1967; Fraser, 1967).
Б.ВОН МАГНУСЫН ҮЗЭГДЭЛ
Томуугийн вирүс 1-ээс дээш олон давтамжтайгаар (Barry, 1961) дараалсан дамжих явцад эзэн эсээс гарч ирдэг бүрэн бус вирус улам бүр нэмэгддэг (фон Магнус, 1951, 1952).Эдгээр вирусын тоосонцор нь гадаргуугийн бүтэцтэй маш төстэй байдаг. халдварт вирусын бүтэц нь дархлаа үүсгэгч бөгөөд гомолог интерференц үүсгэдэг. Эдгээр нь РНХ ба RNP эсрэгтөрөгчийг бага агуулдаг, халдварын гемагглютинжуулах үйл ажиллагаатай харьцуулахад бага харьцаатай бөгөөд вирусын бүрэн хэсгүүдээс илүү их липид агуулдаг (фон Магнус, 1954; Исаакс, 1959; Паукер нар, 1959; Ротт ба Шафер, 1961; Ротт ба Шолтиссек, 1963).
Хэсэгчилсэн вирусын РНХ-д шинжилгээ хийхдээ харьцангуй өндөр молекул жинтэй вирусын РНХ байхгүй эсвэл бага хэмжээгээр агуулагддаг бол бага молекул жинтэй РНХ-ийн хэмжээ нэмэгддэг болохыг тогтоожээ (Duesberg, 1968; Pons, Hirst, 1969; Наяк, 1969).
Томуугийн вирүсийн хоёр дахь шингэрүүлээгүй халдвараар халдварлагдсан эсүүдэд эдгээр эсээс тусгаарлагдсан cfRNA нь эрлийзжүүлсний дараа халдварт вирусээс тусгаарлагдсан шошготой РНХ-ийг бүрэн РНХ-ийн азоз тэсвэртэй хэлбэрт хувиргах чадвартай тул вирусын бүх генетикийн мэдээлэл байдаг. (Шолтиссек, Ротт, 1969б). Ийнхүү бүрэн бус тоосонцор дахь бага молекул жинтэй РНХ-ийн хэмжээ ихсэх нь өндөр молекул жинтэй РНХ-тэй холбоотой байж болох бөгөөд тэдгээр нь устгагдсан, тиймээс ажиллахгүй молекулууд хэлбэрээр эдгээр хэсгүүдэд багтаж болно. Энэ санааг шингэрүүлээгүй цангах үед халдварт вирус үүсгэх чадвар буурч, дараа нь гемагглютинин, нейраминидаза, эцэст нь RNP антигенийн нийлэгжилт буурдаг гэсэн тоо баримтаар нотлогддог (Scholtissek et al., 1966).
Наяк (1972) анх удаа гарч ирсэн вирус нь бүрэн халдвартай байсан бөгөөд сахарозын градиент дахь халдварт вирүсийн РНХ-ийн фрагментийн хэвийн хэв маягийг үүсгэсэн бол хожим гарч ирсэн вирус нь бүрэн бус РНХ-ийн дүр төрхтэй болохыг олж мэдсэн. дэвсгэр) -Magnus) вирус1.
- Хэрэглэхийн эсрэг заалтууд
- Мэдрэлийн импульс дамжуулах замууд Мэдрэлийн импульс дамжуулах үйл явцыг хэн судалсан бэ
- Чихээ хэрхэн зөв цоолох вэ (зүүний цэгүүд)
- Шизофрени өвчний хурцадмал байдлыг цаг алдалгүй хүлээн зөвшөөрч сурах нь хаврын хурцадмал байдал яагаад үүсдэг вэ?
- Миний хөх өвдөж байна, би яах ёстой вэ?
- Сэтгэл дэх хоосон байдал - энэ нь яагаад үүсдэг, түүнээс хэрхэн ангижрах вэ
- Угаалгын өрөөнд уураар жигнэх ашиг тус: эмчийн дүгнэлт
- Нэг настай хүүхдийн тахир хөл, шалтгаан, эмчилгээ
- Таны хөл яагаад хүйтэн байдаг вэ, үүнийг хэрхэн шийдвэрлэх вэ?
- Мэнгэний нууцлаг нууцууд
- Харааны эрхтнүүдийн эрүүл ахуй. Харааны эрүүл ахуй. Нүдний өвчнөөс урьдчилан сэргийлэх - Мэдлэг гипермаркетийн өвчин, харааны эрхтнүүдийн эрүүл ахуй
- Гиперкалиемийн шинж тэмдгийг мэдэх нь яагаад чухал вэ?
- Хөхний хорт хавдрын ангилал, түүний төрөл, үе шатууд ICD 10-ийн дагуу хөхний өвчний код
- Дархлаа судлалын цитокинууд Үрэвслийн эсрэг цитокинууд
- Ханиалгах, гэдэсний эмгэгийн үед зефир үндэс хэрэглэх
- Салицилийн хүчил ба түүний деривативууд (ацетилсалицилын хүчил, фенил салицилат), n-амин-бензайны хүчил ба түүний деривативууд: новокаин, анестезин
- Үтрээний гель Lactagel: хэрэглэх заавар, хямд аналоги, тойм
- Гиперхолестеролеми гэж юу вэ - өвчний шалтгаан ба шинж тэмдэг Цусан дахь холестерины хэмжээ ихсэх UCD 10
- Пропилийн спирт (1-пропанол, этилкарбинол) Пропанол пропилийн спирт
- Шүүмжийг үзсэн бүх хүмүүст энэ өдрийн мэндийг хүргэе!